Первичная гипоплазия воротной вены представляет собой врожденную микрососудистую аномалию печени у собак.
Эмбриональное развитие портальной вены происходит из желточных вен. Чрезмерная инволюция перидуоденальных желточных вен и неспособность сформировать критический анастомоз с печеночными синусоидами приводит к полному или частичному отсутствию портальной венозной системы. У собак аплазия и гипоплазия портальной вены часто связаны с аномальными сосудистыми соединениями между портальной и системными венозными системами12. Данная патология характеризуется уменьшением размеров внутрипеченочной, а иногда и внепеченочной части портальной вены, что приводит к снижению перфузии печени и развитию портальной гипертензии. Сама по себе портальная гипертензия создает угрозу развития асцита и множественных приобретенных портосистемных коллатералей. Поскольку болезнь является врожденной, то чаще всего она регистрируется у молодых животных3.
Клинические признаки и диагностика
Владельцы в основном жалуются на отставание в росте и развитии питомца, отмечают нарушения в его поведении (вялость, агрессия, апатия, судороги, хождение по кругу) и симптомы расстройств желудочно-кишечного тракта (диарея, рвота, отказ от пищи), а также увеличение размеров живота.При клиническом осмотре таких пациентов на приеме у врача и в результате диагностики выявляются отставание в росте, дефицит мышечной массы, признаки печеночной энцефалопатии, такие как снижение активности, атаксия, хождение по кругу, ступор, вокализация, гиперсаливация и кома. Также могут наблюдаться расстройства со стороны ЖКТ (рвота, диарея и анорексия) и внезапно развившийся асцит.
Лабораторные исследования позволяют обнаружить повышение гепатоцеллюлярных ферментов (АЛТ, АСТ), холестатических ферментов (ЩФ, ГГТ), снижение синтетической функции печени (показателей концентраций мочевины, альбумина, глюкозы, холестерина), повышение уровней билирубина, желчных кислот и аммиака в крови. В некоторых случаях может наблюдаться микроцитарная анемия.
Ультразвуковая диагностика часто выявляет асцит, микрогепатию, реномегалию и приобретенные портосистемные коллатерали1. В современной ветеринарной практике КТ-ангиография является предпочтительным методом диагностики и мониторинга аномалий портальных сосудов. Этот метод позволяет комплексно оценить взаимодействие между портальной и системной венозными системами, визуализировать портальную сосудистую сеть и другие несосудистые структуры брюшной полости. Тем не менее КТ-ангиография имеет ограничения, в частности гипоплазия портальной вены может не визуализироваться, особенно при снижении портального кровотока из-за портосистемного шунтирования.
Интраоперационная мезентериальная портография, выполняемая после временной окклюзии шунтирующего сосуда, имеет преимущества перед КТ-ангиографией, поскольку она позволяет дифференцировать истинную аплазию портальной вены от гипоплазии или атрезии, а также улучшает визуализацию портальной сосудистой сети.
Окончательный диагноз «аплазия воротной вены» подтверждается интраоперационной мезентериальной портографией и дополнительным гистологическим анализом печеночной паренхимы12.
В гистологическом анализе образцов печени часто выявляются следующие изменения: гепатоцеллюлярная атрофия, снижение плотности портальной сосудистой сети, сопровождающееся гиперплазией портальных артериол (или без нее), а также гипертрофия паренхиматозных артериол печени.
Несмотря на то что не существует достоверных данных о наличии генетического фактора развития этого заболевания у собак, все же отмечается, что первичная гипоплазия воротной вены чаще встречается у собак той-пород1.
К основным осложнениям можно отнести портальную гипертензию и печеночную энцефалопатию8.
В настоящее время не разработаны эффективные методы лечения данного заболевания. Основными задачами врача являются контроль над течением болезни и предотвращение возможных осложнений. Это включает мониторинг и управление такими состояниями, как портальная гипертензия, печеночная энцефалопатия и риск возникновения желудочно-кишечного кровотечения.
Клинический случай
Пациент: 6-месячная собака породы цвергшнауцер (некастрированная самка) поступила на прием к неврологу по причине частого тремора передней правой конечности. Владелица также отметила недостаточный набор массы тела, небольшое отставание в росте, периодические расстройства стула, рвоту и избирательный аппетит. Рацион собаки, составленный ветеринарным диетологом, включает рис, вареную индейку и тыкву и считается сбалансированным.На момент осмотра масса тела собаки составила 3,0 кг. Видимые слизистые оболочки розовые, сознание и черепно-мозговые рефлексы находились в пределах нормы, проприорецепция не была нарушена, болезненность при пальпации отсутствовала.
Диагностика
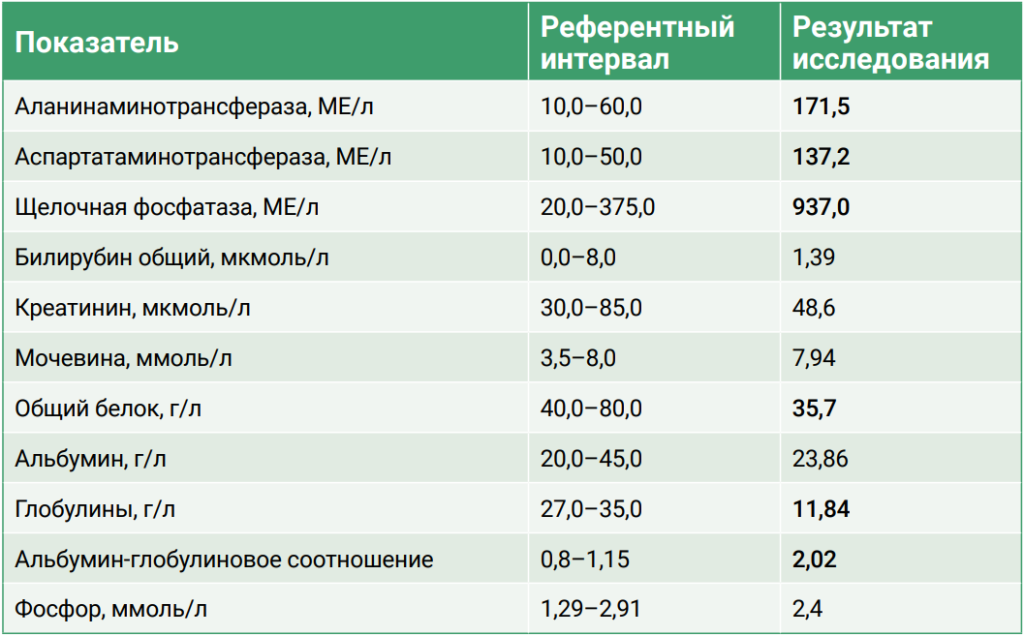
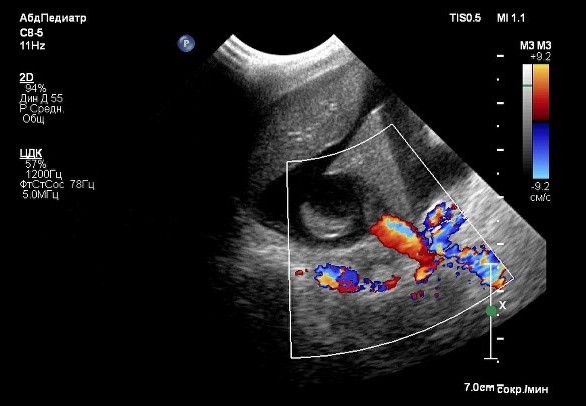
Были проведены лабораторные исследования крови, включающие биохимический и клинический анализы. В результате проведения биохимического анализа было выявлено умеренное повышение гепатоцеллюлярных ферментов (табл. 1), в то время как результат клинического анализа показал легкую анемию без признаков регенерации. Дополнительно были измерены уровни желчных кислот методом парных проб (до и после кормления). Результаты показали выраженное повышение, что свидетельствует о синтетической дисфункции печени (табл. 2). Уровень глюкозы в крови составил 3,4 ммоль/л при норме 3,5–6,1 ммоль/л, что указывает на наличие легкого уровня гипогликемии.Ультразвуковое исследование органов брюшной полости выявило признаки микрогепатии, нефролитиаза, уролитиаза и асцита (скопление жидкости в брюшной полости) в небольшом количестве (до 2 мм на просвет; фото 1).
Сочетание лабораторных данных анализов крови и ультразвуковых изменений позволило предположить наличие врожденной сосудистой аномалии – портосистемного шунта. Для подтверждения (или опровержения) диагноза пациента отправили на проведение КТ-ангиографии.
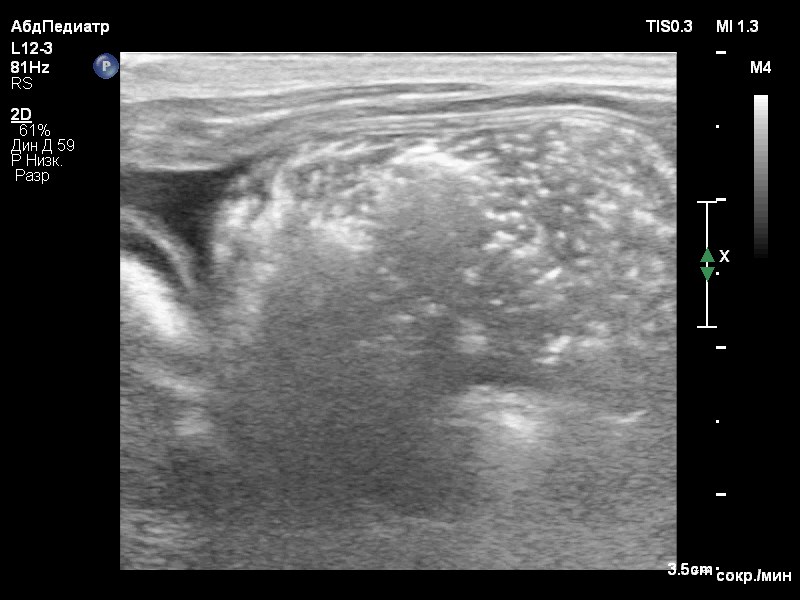
По результатам КТ-ангиографии выявлены следующие изменения (фото 2):
- множественные портокавальные анастомозы, предположительно, приобретенного характера;
- микрогепатия и отек стенки желчного пузыря;
- отек паренхимы поджелудочной железы;
- изменения в стенках желудка и тонкого кишечника, вероятно, обусловленные венозным застоем или воспалительными процессами;
- наличие асцита.
Портальная гипертензия возникает из-за повышенного сосудистого сопротивления в системе воротной вены. Обычно она наблюдается у пациентов с тяжелым приобретенным поражением печени или врожденной микрососудистой аномалией внутри печени.
Для уточнения диагноза необходимо было проведение дополнительной диагностики, включающей лапаротомию с целью получения биопсийного материала печени для гистологического исследования, а также выполнение интраоперационной мезентериальной портографии.
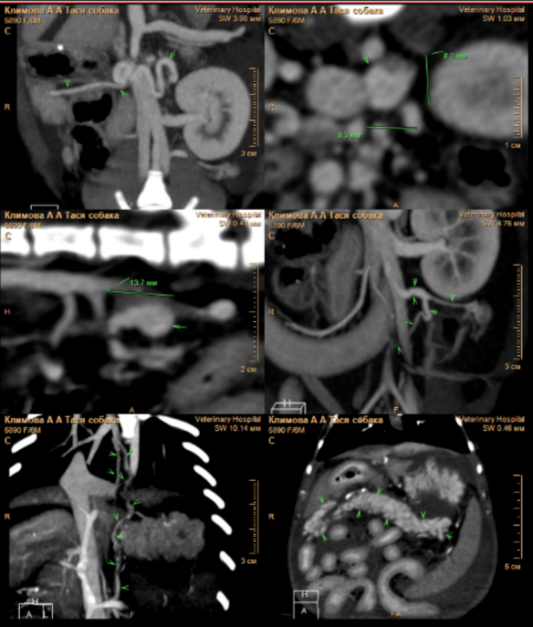
В этот период состояние пациента ухудшилось (фото 3), прогрессировал более выраженный асцит. Это привело к затруднению двигательной активности собаки, и владельцы приняли решение о повторном проведении ультразвукового исследования брюшной полости.
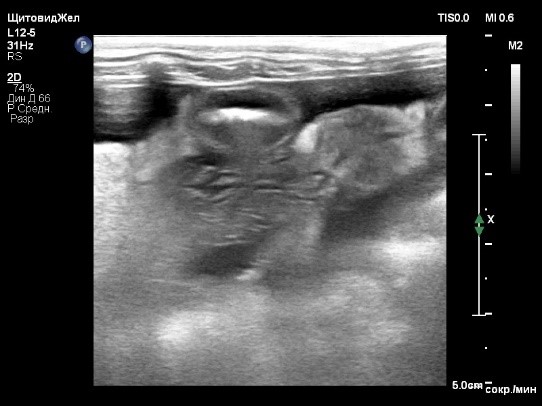
В ходе проведения УЗИ выявлена отрицательная динамика в отношении количества свободной жидкости в брюшной полости (до 6 см на просвет). Также обнаружены увеличение отека паренхимы поджелудочной железы, характеризующееся появлением признаков, известных как «тигровая поджелудочная железа», и нефролитиаз (фото 4). Данные изменения свидетельствуют о развитии тяжелой портальной гипертензии, что требует проведения незамедлительной диагностики для установления причин и разработки плана лечения.
Лечение
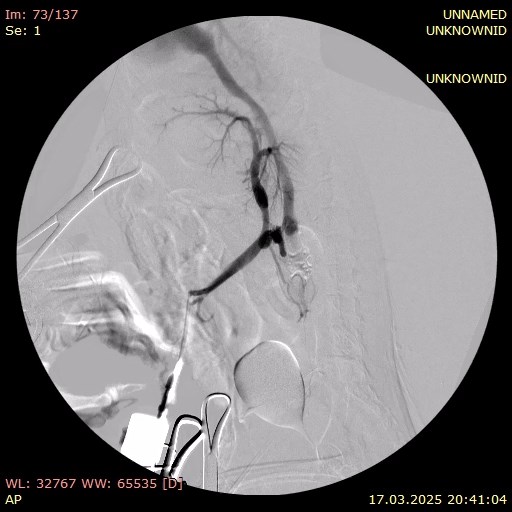
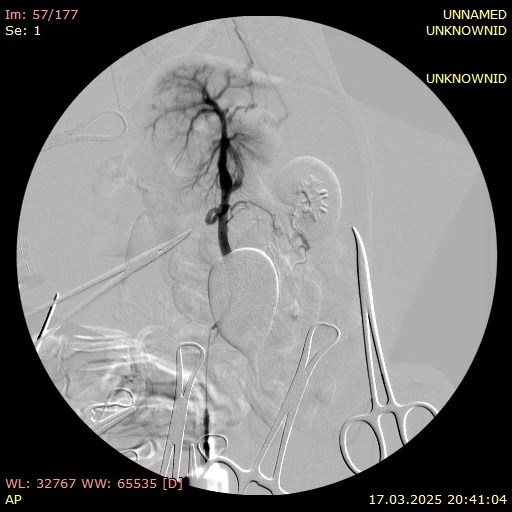
В этот же день пациенту были проведены хирургическое лечение (лапаротомия с аспирацией 800 мл прозрачной жидкости) и портография. Органы брюшной полости расположены анатомически правильно, висцеральный жир умеренно выражен. Сосуды брюшной полости расширены, селезенка умеренно увеличена. Печень значительно уменьшена в размерах, имеет желто-коричневый цвет и сглаженную зернистость. В паренхиме выявлены множественные включения светлого цвета. Желчный пузырь слабо наполнен, мягкий при пальпации. Желудок и кишечник без особенностей, перистальтика выражена хорошо. Измерение давления в портальной вене показало 20 мм вод. ст.Портография выявила множественные шунты: между портальной веной и каудальной полой веной, а также два спленоазигональных шунта (фото 5).
На основании результатов проведенной лапаротомии и портографии была подтверждена выраженная портальная гипертензия. Для снижения давления в системе воротной вены была выполнена спленэктомия с использованием УЗ-скальпеля. Также была проведена биопсия печени для последующего гистологического исследования.
Спленэктомия является доказанно эффективным методом лечения пациентов с портальной гипертензией, так как она снижает давление в системе воротной вены и улучшает гемодинамику за счет уменьшения артериального и, соответственно, венозного кровотока в спланхническую область2.
Послеоперационный период прошел без осложнений.
Результаты гистологического исследования
Морфологический диагноз: неравномерная гипоплазия портальных вен, пролиферация артериол и билиарных протоков, атрофия гепатоцитов.Диагноз: признаки снижения портального кровотока.
Комментарий. Наблюдаются сосудистые изменения печени, которые являются неспецифичными и могут быть характерны для различных патологических состояний, таких как наследственный портосистемный шунт (внутрипеченочный или внепеченочный), приобретенный портосистемный шунт, дисплазия сосудов печени (HVD), наследственная внутрипеченочная артериовенозная фистула и другие. Само по себе гистопатологическое исследование не позволяет установить окончательный диагноз, требуются дополнительные клинические и визуализирующие исследования, чтобы дифференцировать эти сосудистые аномалии.
Таким образом, был поставлен окончательный диагноз «первичная гипоплазия портальных вен с развитием дисфункции печени и портальной гипертензии».
К сожалению, на данный момент не существует методов лечения этой болезни. Задача лечащего врача заключается в коррекции возможных пагубных последствий данного заболевания. Обязательны контроль портальной гипертензии (так как спленэктомия является лишь одним из вариантов контроля) и коррекция возможного развития печеночной энцефалопатии, гипоальбуминемии, анемии, гипернатриемии.
Для коррекции асцита требуется выявление натрийуреза. Начальным терапевтическим шагом является ограничение натрия. Назначается диета, обеспечивающая менее 0,05 г натрия на 100 ккал. При отсутствии ответа на ограничение натрия добавляются диуретики. Препаратом выбора является антагонист альдостерона спиронолактон, который действует на почечные собирательные протоки, увеличивая экскрецию натрия и сохраняя калий. Начальная дозировка составляет 1–2 мг/кг/сутки и может постепенно увеличиваться в течение 3–5 дней.
Модуляция кишечной продукции и снижение всасывания токсинов являются основой лечения печеночной энцефалопатии. Энтеральное и парентеральное введение неабсорбируемых дисахаридов (например, лактулозы) подкисляет просвет толстой кишки, что приводит к конверсии NH3 в NH4+, который является непроницаемым для мембран клеток кишечника и выводится из организма в виде солей аммония. Начальная дозировка составляет 0,25–0,5 мл/кг перорально каждые 12–8 часов, но дозировка должна быть скорректирована таким образом, чтобы достичь 2–3 эпизодов дефекации мягким калом в сутки.
В связи с венозным застоем в органах брюшной полости, включая ЖКТ, эти пациенты могут быть предрасположены к развитию гастропатии, а именно к эрозивно-язвенному повреждению слизистой оболочки желудка. Использование цитопротекторных препаратов или ингибиторов протонной помпы может быть полезным5.
Пациенту был назначен спиронолактон в дозе 2 мг/кг/сутки, которая впоследствии была скорректирована до эффективной дозы 3 мг/кг/сутки. Также пациенту были назначены лактулоза («Дюфалак» или «Лактусан») в дозе 4 мл каждые 8 часов, сукральфат в дозе 250 мг на собаку каждые 12 часов и коррекция диеты под руководством врача-диетолога. Диета включала ограничение натрия и оптимальное содержание высокоусвояемого белка. Все назначенные препараты рекомендованы для постоянного применения.
На текущий момент пациент находится под наблюдением терапевта-гастроэнтеролога. Общее самочувствие животного стабильное, а показатели лабораторных анализов крови удовлетворительные.
Заключение
Гипоплазия воротной (портальной) вены – редкая аномалия, обусловленная дефектным развитием портальной венозной системы у эмбриона.Основные клинические проявления включают портальную гипертензию, обусловленную нарушением гемодинамики в системе воротной вены, и нейроповеденческий синдром, связанный с гипераммониемией. Также у таких пациентов могут наблюдаться симптомы желудочно-кишечных расстройств вследствие дисфункции печени.
Диагностика данного заболевания требует комплексного подхода, включающего лабораторные и визуализирующие исследования, а также интраоперационную мезентериальную портографию.
Окончательный диагноз ставится на основании комплексного анализа полученных данных, в том числе результатов гистологического исследования паренхимы печени.
В настоящее время проблема заключается в отсутствии эффективных методов лечения, направленных на полное излечение заболевания. Основные задачи врача – контроль и профилактика возможных осложнений, связанных с развитием патологического процесса.
Список литературы:
- Makoto Akiyoshi, Masaharu Hisasue, Masami Akiyoshi. Clinicopathological Findings and Prognosis in Canine Cases Diagnosed As Primary Hypoplasia of the Portal Vein. Front Vet Sci, 21:4:224, Dec 2017. doi: 10.3389/fvets.2017.00224.
- Philipp Schwab, Berit Anna Seeland, Florian Riedl, et al. Splenectomy ameliorates portal pressure and anemia in animal models of cirrhotic and non-cirrhotic portal hypertension. Adv Med Sci, 67(1): 154–162, Mar 2022. doi: 10.1016/j.advms.2022.02.005.
- Portal Vein Hypoplasia in Dogs and Cats – Veterinary Partner – VIN; ссылка
- Angelo Luca, Roberto Miraglia, Settimo Caruso, et al. Effects of splenic artery occlusion on portal pressure in patients with cirrhosis and portal hypertension. Liver Transpl, 12(8): 1237–43, Aug 2006. doi: 10.1002/lt.20762.
- Buob S., Johnston A. N., Webster C. R. L. Portal hypertension: pathophysiology, diagnosis, and treatmen. J Vet Intern Med, 25(2):169–86, Mar-Apr 2011.
- Hess P. R., Bunch S. E. Management of portal hypertension and its consequences. Vet Clin North Am Small Anim Pract, 25(2): 461–83, Mar 1995.
- Anand V. Kulkarni, Atoosa Rabiee, Arpan Mohanty. Management of Portal Hypertension. J Clin Exp Hepatol, 12(4): 1184–1199, Jul-Aug 2022.
- Robert J. Washabau, Michael J. Day. Canine and Feline Gastroenterology, July 2012.
- Jaime Bosch, et al. The management of portal hypertension: Rational basis, available treatments and future options. J Hepatol, 48 Suppl 1(1): S68–92, 2008.
- Jonathan Lidbury. Complications of Liver Disease. Vet Clin North Am Small Anim Pract, 2025.
- Glińska K., Skrzypczak P., et al. Portography in dogs.September. Medycyna Weterynaryjna, 64(9): 1112–1114, 2008.
- Mu-Young Kim, Ji-Hyun Kim, Kyu-Chang Kim, Hun-Young Yoon. The effectiveness of intraoperative mesenteric portography for preventing misdiagnosis of congenital absence of the portal vein in dog with extrahepatic portosystemic shunt: a case report, 2022.



 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург