ВК Сложного случая, г. Санкт-Петербург.
Цель статьи – представить описание клинических симптомов, диагностики, лечения и краткосрочных исходов артропатии, ассоциированной с применением препарата «Левофлоксацин», на примере конкретного клинического случая. Дополнительно будет описан патогенез изменений хрящевой ткани суставов у молодых животных вследствие использования фторхинолонов на основе анализа литературных данных.
Вторичная цель статьи – привлечь внимание к проблеме антибиотикорезистентности, которая все больше внедряется в повседневную ветеринарную практику и оказывает значительное влияние на здравоохранение в целом.
Левофлоксацин относится к группе фторхинолонов третьего поколения и является антибактериальным препаратом широкого спектра действия. Его активность распространяется на грамположительные бактерии и атипичные внутриклеточные патогены1, что отличает его от препаратов предыдущих поколений. Левофлоксацин включен в Перечень основных лекарственных средств Всемирной организации здравоохранения2. В странах Европейского союза (ЕС) Европейским медицинским агентством все неветеринарные фторхинолоны запрещены к использованию у животных (они включены в «ограниченную» категорию B). Эти ограничения направлены на борьбу с бактериальной устойчивостью к антимикробным препаратам3. В Соединенных Штатах Америки Закон о разъяснении использования лекарственных препаратов для животных 1994 года разрешает применение левофлоксацина в ветеринарной практике при условии, что здоровье животного находится под угрозой, а также когда отсутствие лечения может привести к страданиям или смерти4. В Российской Федерации левофлоксацин зарегистрирован как ветеринарный препарат под различными торговыми наименованиями, такими как «Лексофлон», «Левоксивет», «Левофлоксацин-О 150» и «Ветфлоксацин». Препарат доступен в виде инъекций, таблеток и растворов для перорального применения. Вариативность ограничений на использование антибактериальных препаратов в разных странах может свидетельствовать о степени осознания и формирования соответствующих политик для борьбы с такой серьезной угрозой для здоровья человека, как антибиотикорезистентность, при лечении бактериальных инфекций.
Левофлоксацин был впервые запатентован в 1985 году японской фармацевтической компанией Daiichi Seiyaku Pharmaceutical Co., Ltd. Однако его коммерческое использование для лечения людей началось только в 1993 году, когда препарат был выпущен в форме пероральных таблеток под торговой маркой Gravit®. В том же году Daiichi Sankyo заключила лицензионное соглашение с компанией Sanofi-Aventis, что позволило расширить доступность левофлоксацина на международном рынке под брендом Tavanic®. С 2010 года на фармацевтическом рынке появились дженерические версии препарата5.
Левофлоксацин – оптический S-изомер офлоксацина. Его антибактериальная активность в два раза выше, чем у рацемического офлоксацина, и в 128 раз превосходит активность (R)-антипода11. В сравнении с офлоксацином левофлоксацин демонстрирует улучшенный фармакологический профиль, меньшую частоту побочных эффектов и лучшую переносимость. Для достижения аналогичного терапевтического эффекта требуется примерно половина дозы офлоксацина, что сопровождается снижением профиля токсичности1. Данный препарат эффективен при лечении различных инфекционных заболеваний. Спектр его действия включает грамположительные и грамотрицательные аэробные бактерии, некоторые анаэробные бактерии и другие микроорганизмы, включая Chlamydia spp., Mycoplasma spp. и Mycobacterium spp.1 В медицине человека он считается одним из «респираторных фторхинолонов» из-за его широкого спектра действия против грамположительных, грамотрицательных и анаэробных бактерий6.
Левофлоксацин, как и другие фторхинолоны, ингибирует бактериальную ДНК-гиразу (фермент, участвующий в репликации, транскрипции, репарации и рекомбинации ДНК) и топоизомеразу IV. Этот механизм ингибирования предотвращает репликацию и транскрипцию бактериальной ДНК, что приводит к бактерицидному эффекту1. Микробная резистентность к фторхинолонам может быть результатом мутаций в определенных областях ДНК-гиразы или топоизомеразы IV (т. е. в областях, определяющих резистентность к хинолону (QRDR) – gyrA и parC). Исследования, проводимые на животных, ограничены, однако существует значительный объем данных, полученных в ходе клинических испытаний с участием людей.
Мутации в микробных генах, выделенных от животных, связанные с повышенной устойчивостью к левофлоксацину, такие как увеличение экспрессии эффлюксного насоса, были задокументированы в молекулярных исследованиях на различных микроорганизмах, включая Escherichia coli1.
У собак наблюдается почти полное пероральное всасывание левофлоксацина с биодоступностью около 100%. Период полувыведения препарата у собак составляет 5,6 часа, а связывание с белками – 22–27%. У кошек после введения дозы 10 мг/кг период полувыведения составляет 7–8 часов с высокой пероральной биодоступностью (86%) и пиковой концентрацией в плазме 4,7 мкг/мл6.
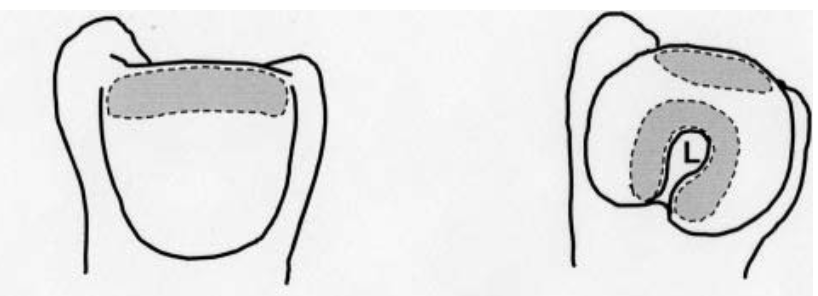
Все фторхинолоны, включая левофлоксацин, могут вызывать артропатию у молодых животных6. Считается, что среди экспериментальных животных, таких как мыши, крысы, морские свинки, кролики, собаки и нечеловекообразные приматы, молодые собаки (как правило, крупных, быстрорастущих пород6) в возрастной группе 4–28 недель наиболее восприимчивы к артропатии, вызванной хинолонами6-7. Участки повреждения, наиболее подверженные макроскопическим изменениям, согласно некоторым исследованиям, – дорсальная область головок плечевой и бедренной костей, а также зоны вокруг места прикрепления круглой связки (рис. 1).
В настоящее время не существует единой теории, объясняющей патогенез развития изменений на суставных поверхностях вследствие применения фторхинолонов, несмотря на попытки объяснить их на животных моделях. Тем не менее данные исследования демонстрируют ряд общих закономерностей7. В качестве примера можно привести исследование с участием трех щенков породы бигль в возрасте 3 месяцев и двух взрослых собак той же породы в возрасте 3 лет. Исследование включало использование двух моделей: in vivo и in vitro.
В модели in vivo щенкам перорально вводили офлоксацин в дозе 20 мг/кг массы тела 1 или 2 раза в сутки. Затем головки плечевых и бедренных костей собак подвергались патоморфологическому исследованию для выявления ранних признаков артропатии. Макроскопически на суставных поверхностях молодых собак были обнаружены заполненные жидкостью везикулы: у одного щенка через 24 часа после однократного введения офлоксацина, при двукратном введении антибиотика аналогичные поражения наблюдались у всех щенков. Микроскопическое исследование выявило трещины или полости в средней зоне суставного хряща у молодых собак. Кроме того, хрящевой матрикс от аномальной области до здоровой суставной поверхности демонстрировал снижение интенсивности окрашивания сафранином-O, что указывало на истощение протеогликанов. У взрослых собак подобные изменения в суставном хряще отсутствовали.
В рамках эксперимента in vitro были выделены хондроциты из суставного хряща здоровых молодых собак, которые затем подвергли воздействию различных концентраций офлоксацина (6,3–100 мкг/мл) в течение 24 часов. В результате наблюдалось дозозависимое снижение синтеза протеогликана – ключевого фактора целостности хряща. При этом синтез ДНК и белка оставался неизменным.
Вывод из вышесказанного заключается в том, что офлоксацин вызывает ранние артропатические изменения у молодых собак, ингибируя синтез протеогликана в хондроцитах. Это приводит к морфологическим изменениям, таким как образование заполненных жидкостью пузырьков на поверхности суставного хряща, появление трещин или полостей в хряще и истощение протеогликана, которые не наблюдаются у взрослых собак. Результаты исследования подтверждают, что подавление синтеза протеогликана офлоксацином в значительной степени способствует раннему развитию артропатии у молодых собак.
Еще одно исследование8, сравнивающее применение фторхинолонов у молодых собак породы бигль (возраст 3 месяца), выявило, что такие антибиотики, как офлоксацин и ципрофлоксацин,вызывают образование пузырьков и эрозию хряща на суставных поверхностях, в то время как грепафлоксацин продемонстрировал относительно меньший потенциал токсичности для суставов. Гистопатология выявляла потерю хрящевого матрикса и хондроцитов.
Другое исследование9 показало, что пероральное введение офлоксацина в дозе 20 мг/кг в день в течение 7 дней у молодых собак вызывало артропатию, обнаруживаемую с помощью МРТ. На изображениях МРТ наблюдались неровные суставные поверхности и поражения, соответствующие многоочаговым волдырям на суставном хряще.
На основании результатов многочисленных ветеринарных исследований можно сделать вывод, что фторхинолоны могут вызывать у щенков артропатию с характерным повреждением поверхности сустава, особенно в суставах, несущих весовую нагрузку. Степень токсичности этих препаратов зависит от возраста животного. Незрелый хрящ поражается во время фаз роста, что требует тщательной оценки клинической необходимости применения данных препаратов у молодых животных.
В настоящее время существует определённое понимание патогенеза данного вида артропатии, однако литературные данные о диагностике, лечении и прогнозах уже возникшей артропатии у щенков отсутствуют.
Клинический случай
Представленный в данной статье клинический случай описывает симптомы, диагностику, лечение и краткосрочный прогноз артропатии вследствие применения фторхинолонов.В отделение реанимации нашей ветеринарной клиники поступил трехмесячный щенок восточноевропейской овчарки. Пациент был доставлен из сторонней клиники транспортировочной ветеринарной службой на аппарате ИВЛ в связи с тяжелым повреждением легких. В стороннюю клинику животное поступило с клиническими признаками дыхательной недостаточности. В анамнезе пациента зафиксировано резкое развитие диспноэ после того, как животное подавилось сухим кормом.
Щенок был приобретен в питомнике и в течение двух недель находился на содержании у текущих владельцев. Клинических признаков заболеваний или отклонений в состоянии здоровья в этот период не наблюдалось. Вакцинация и обработка от экто- и эндопаразитов не проводилась. Рацион щенка состоял из промышленного сухого корма. Условия содержания были домашними, без постоянного доступа на улицу.
Со слов владельцев, питомец подавился утром при поедании корма, что привело к появлению тяжелого дыхания. Через короткий промежуток времени щенок откашлял корм, однако дыхательные нарушения сохранялись, что послужило поводом для обращения в стороннюю клинику.
С учетом наличия острой дыхательной недостаточности, возникшей после откашливания/срыгивания корма, а также прогрессирования симптомов после очередного кормления в сторонней клинике был поставлен предварительный диагноз «аспирационная пневмония». В связи с этим пациенту была назначена комбинированная антибиотикотерапия, включающая амоксиклав и левофлоксацин. Из-за прогрессирования дыхательной недостаточности щенок был переведен на аппарат ИВЛ, а в конце первых суток после госпитализации его транспортировали в нашу клинику.
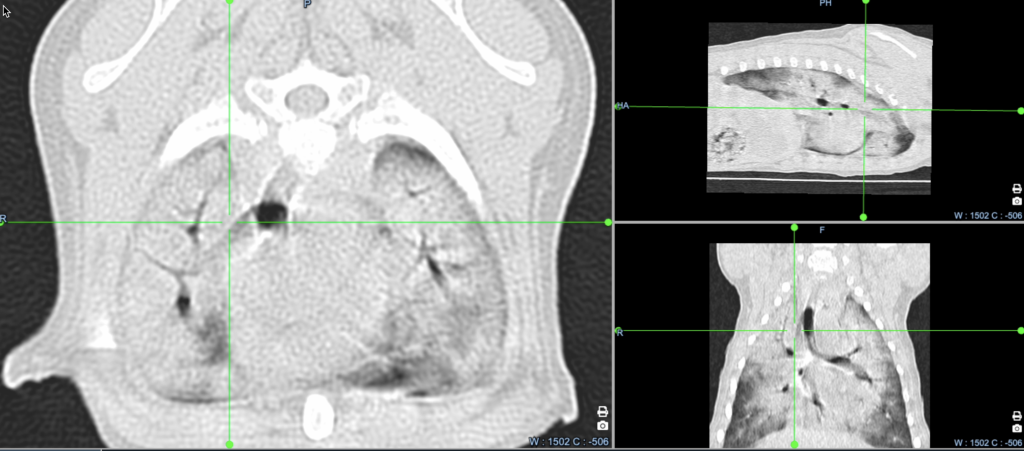
Диагностика. В ОРИТ нашей ветеринарной клиники пациенту была проведена компьютерная томография (КТ), а также был выполнен бронхоальвеолярный лаваж (полученный материал был направлен на цитологическое и бактериологическое исследования). На КТ наблюдалась почти полная консолидация около 90% площади легочной паренхимы (рис. 2).
Цитологическое исследование БАЛ выявило нейтрофильное воспаление, а бактериологический посев (впоследствии) не показал роста патогенной микрофлоры.
Щенок был отключен от аппарата ИВЛ спустя примерно 36 часов после появления симптомов.
На основании анамнеза (случайное удушье кормом), рентгенологических данных, результатов лабораторных исследований и скорости разрешения легочного паренхиматозного заболевания был сделан вывод о том, что причиной дыхательной недостаточности являлся постобструктивный отек легких, а не аспирационная пневмония.
Видео 1.
Случайное удушье кормом при его поедании является одной из причин возникновения постобструктивного отека легких у собак. В рамках исследования, посвященного отеку легких с отрицательным давлением у собак10, были проанализированы 35 случаев, из которых 9 были связаны с удушьем кормом. Средний возраст собак составлял 4 месяца. Из 35 собак 80% выжили, однако из семи невыживших животных четверо были подвергнуты эвтаназии, а трое умерли естественной смертью. Точная причина эвтаназии не была установлена, но наиболее вероятными факторами могли быть финансовые обстоятельства или неблагоприятный прогноз. Таким образом, реальная выживаемость в данной группе пациентов, вероятно, превышает 80%. Средняя продолжительность госпитализации составляла 2 дня.
На вторые сутки после отлучения от ИВЛ у щенка были выявлены скованность походки и хромота, преимущественно на тазовые конечности (видео 1), а также болезненность при пальпации плечевых, локтевых и тазобедренных суставов. Были отобраны образцы крови для проведения общеклинического и биохимического анализов, результаты которых не показали специфических изменений.
Дополнительно были взяты образцы крови для определения уровня С-реактивного белка и выявления антител к возбудителям анаплазмоза собак (Anaplasma platys, Anaplasma phagocytophilum), лейшманиоза (Leishmania spp.), эрлихиоза (Ehrlichia canis), боррелиоза (Borrelia burgdorferi), антигенов возбудителей дирофиляриоза (Dirofilaria immitis) методом ИФА, а также для обнаружения микрофилярий методом Кнотта и антител к возбудителям бруцеллеза собак методом быстрой агглютинации на стекле. Кроме того, были отобраны образцы крови для выявления методом ПЦР антигенов возбудителей таких инфекционных заболеваний, как бартонеллез (Bartonella vinsonii) и гемоплазмоз (Candidatus Mycoplasma haematoparvum, Candidatus Mycoplasma haemocanis). Также была отобрана синовиальная жидкость для бактериологического посева, клинического анализа и определения антигенов возбудителей боррелиоза (Borrelia burgdorferi sensu lato) методом ПЦР.
Результаты анализов показали, что уровень С-реактивного белка составил 126,3 мг/л, что значительно превышает референсные значения (0,0–20,0 мг/л). Все отобранные инфекции ожидаемо дали отрицательный результат. В клиническом анализе клеточный состав синовиальной жидкости был представлен большим количеством крупных мононуклеарных клеток, значительная часть которых (более 40%) имела вакуолизированную цитоплазму. Также были обнаружены небольшие количества малых лимфоцитов и единичные недегенеративные нейтрофилы. Фон имел оксифильный зернистый окрас и содержал небольшое количество эритроцитов и разрушенных клеток. Инфекционные агенты и признаки злокачественности не были выявлены. Цитоз составил 1270,0 мкл, уровень белка – 27,8 г/л.
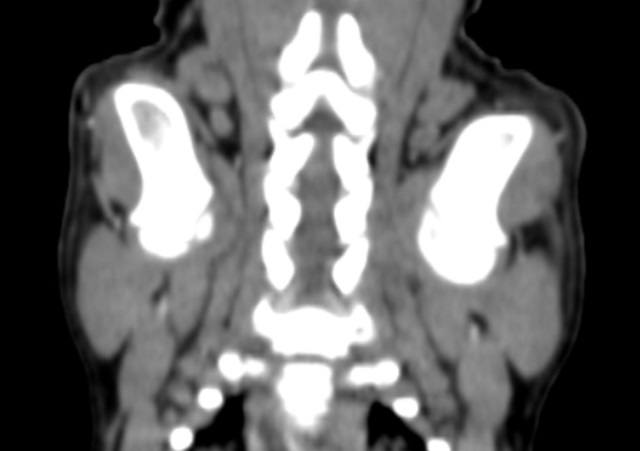
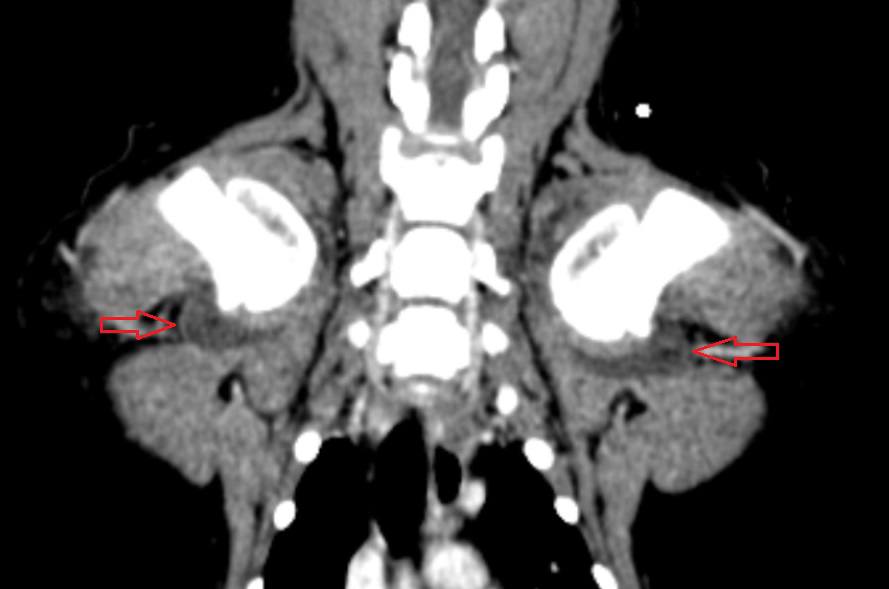
Была проведена повторная КТ с внутривенным контрастированием, по результатам которой было выявлено значительное увеличение размеров капсул в обоих плечевых (рис. 3, 4), локтевых и тазобедренных суставах, а также в левом коленном суставе по сравнению с данными первоначального КТ-исследования.
На основании клинических симптомов, анамнеза приема левофлоксацина, отсутствия ортопедических симптомов до поступления пациента в клинику, результатов анализов крови и синовиальной жидкости, а также проведенной КТ был поставлен диагноз «множественная артропатия, вызванная применением фторхинолонов».
Лечение. Терапия заключалась в отмене левофлоксацина, который щенок успел получить трехкратно в дозировке 20 мг/кг внутривенно. Ввиду выраженного болевого синдрома была назначена мультимодальная анальгезия: трамадол внутримышечно в дозе 3 мг/кг 2 раза в сутки, габапентин в дозе 15 мг/кг перорально 2 раза в сутки и мелоксикам в дозе 0,05 мг/кг перорально 1 раз в сутки. Также 3 раза в день проводились занятия с реабилитологом (видео 2).
Амоксиклав был отменен после получения результатов бактериологического посева. Спустя три дня с момента начала курса были прекращены введение трамадола и габапентина, а мелоксикам был отменен через пять дней. Спустя семь дней после отмены левофлоксацина симптомы полиартропатии исчезли (видео 3). К этому моменту уровень С-реактивного белка снизился до 4,21 мг/л (референтные значения: 0,0–10,0 мг/л).
Видео 2.
Видео 3.
Выводы
Качественные литературные данные, описывающие распространенность, патогенез, диагностику, лечение и прогноз артропатии у собак, вызванной применением фторхинолонов, очень ограничены. В одном исследовании (антигуманном, по мнению авторов этой статьи) с участием трех здоровых щенков породы бигль7 изучалась патофизиология развития артропатии после перорального применения офлоксацина (левофлоксацин – оптический S-изомер офлоксацина). Целью исследования было выявление макроскопических и гистологических изменений в пораженных суставах. Изменения в суставах были зафиксированы уже через 24 часа после первого введения препарата в терапевтической дозе, что указывает на возможность их развития после однократного применения препарата.В представленном клиническом случае объем проведенной диагностики, вероятно, был избыточным, однако это позволило подтвердить установленный диагноз, исключив все остальные причины полиартрита. С учетом отсутствия ортопедических симптомов до начала приема фторхинолонов и их появления после начала терапии можно сделать вывод о развитии артропатии вследствие применения данных фторхинолонов.
Терапия включает отмену фторхинолонов и назначение симптоматического лечения, включающего применение анальгетиков и реабилитацию. Краткосрочный прогноз (на примере нашего клинического случая) хороший. Однако неизвестно, как перенесенное в щенячьем возрасте структурное заболевание хрящевой ткани суставов повлияет на их развитие в будущем.
В заключение необходимо подчеркнуть, что многие случаи, которые клинически воспринимаются как аспирационная пневмония, на самом деле таковыми не являются. Применение фторхинолонов для лечения даже подтвержденной аспирационной пневмонии не всегда оправдано.
Левофлоксацин запрещен или ограничен к использованию у ветеринарных пациентов во многих странах мира за исключением некоторых государств, включая Россию. Это связано с серьезными опасениями относительно устойчивости микроорганизмов к антибиотикам. Важно осознавать, что проблема резистентности микроорганизмов не ограничивается локальными границами. Она может распространяться через продукты питания, полученные от сельскохозяйственных животных, миграцию населения, туризм и трудовую деятельность, включая перемещение людей и их домашних животных. Ненадлежащее использование левофлоксацина и других антибиотиков может привести к значительным негативным последствиям для эффективности антимикробной терапии и глобального здравоохранения.
Список литературы:
- North D. S., Fish D. N., Redington J. J. Levofloxacin, a second-generation fluoroquinolone. Pharmacotherapy, 18(5): 915–935, 1998.
- The Selection and Use of Essential Medicines: Report of the WHO Expert Committee on Selection and Use of Essential Medicines, 2019 (Including the 21st WHO Model List of Essential Medicines and the 7th WHO Model List of Essential Medicines for Children). World Health Organization, Geneva.
- European Medicines Agency, 2020. EMA/CVMP/CHMP/682198/2017 Categorisation of Antibiotics in the European Union.
- Animal Medicinal Drug Use Clarification Act of 1994. Extralabel Use of FDA Approved Drugs in Animals, Limitations to Extralabel Use Provisions of AMDUCA, Extralabel Use in Food-producing Animals, pp. 5–9.
- Andrejs Sitovs, Irene Sartini, Mario Giorgi. Levofloxacin in veterinary medicine: a literature review, Research. Veterinary Science, 137: 111–126, 2021.
- Mark G. Papich. Handbook of Veterinary Drugs, 5th Edition, 2020.
- Yabe K., Satoh H., Ishii Y., Jindo T., Sugawara T., Furuhama K., Goryo M., Okada K. Early pathophysiologic feature of arthropathy in juvenile dogs induced by ofloxacin, a quinolone antimicrobial agent. Vet Pathol, 41(6): 673–81, Nov 2004.
- Takizawa T., Hashimoto K., Minami T., Yamashita S., Owen K. The comparative arthropathy of fluoroquinolones in dogs. Exp Toxicol, 18(6): 392–9, Jun 1999.
- Yabe K., Yoshida K., Yamamoto N., Nishida S., Ohshima C., Sekiguchi M., Yamada K., Furuhama K. Diagnosis of quinolone-induced arthropathy in juvenile dogs by use of magnetic resonance (MR) imaging. Vet Med Sci, 59(7): 597–9, Jul 1997. doi: 10.1292/jvms.59.597.
- Vicente J. Herrería-Bustillo at al. Retrospective evaluation of negative-pressure pulmonary edema in dogs (2006-2018): 35 cases, J Vet Emerg Crit Care, 32: 397–404, 2022.
- Туницкая В. Л., Хомутов А. Р., Кочетков С. Н. и др. Ингибирование ДНК-гиразы левофлоксацином и другими производными фторгетероциклов. Acta Naturae, 2011.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург