Отлучение или вининг (weaning) – это процесс отмены аппаратной респираторной поддержки и перевода пациента на полноценное спонтанное дыхание.
При непродолжительной искусственной вентиляции легких (до 24 часов) пациента можно отлучить в короткие сроки.
Цель данной статьи: проанализировать подходы к винингу после продолжительной вентиляции на основании сведений, представленных в ветеринарной литературе, в совокупности с данными, заимствованными из медицины человека, а также практическим опытом специалистов нашего отделения.
Когда начинать процесс отлучения от аппарата ИВЛ
Критерии, по которым можно оценить готовность пациента к винингу с минимальными рисками осложнений: удовлетворительные показатели кислотно-основного состояния и электролитов, уровень FiO2 – 21–35%, стабильная гемодинамика, умеренное количество отделяемого из дыхательных путей при санации; основное заболевание излечено или есть выраженная положительная динамика1.Несвоевременное отлучение несет за собой риски в виде вентилятор-ассоциированной пневмонии (ВАП), вентилятор-индуцированного повреждения легких, а также избыточного применения седативных препаратов. Однако слишком ранняя экстубация чревата аспирацией, гипоксемией и последующей реинтубацией3.
Чем больше продолжительность искусственной вентиляции легких, тем сложнее период отлучения, который предполагает сокращение аппаратной поддержки и восстановление самостоятельного дыхания. То есть по мере возрастания дыхательной активности животного и его способности эффективно спонтанно дышать уменьшается степень респираторной поддержки.
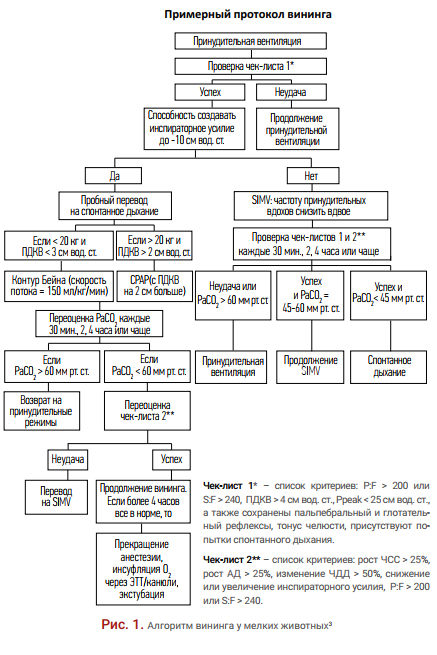
Протокол вининга, описанный в ветеринарной литературе (рис. 1)3
Вентиляция на принудительных режимах, в которых оценивается соотношение P:F (более 200) или отношение сатурации к фракции кислорода во вдохе (более 240). При этом ПДКВ (положительное давление конца выдоха) устанавливается на уровне, не превышающем 4 см вод. ст., а пиковое давление (Ppeak) – менее 25 см вод. ст. Если при низком уровне седации у животного есть попытки сопротивления аппарату, сохранены рефлексы черепно-мозговых нервов, хороший тонус челюсти, то возможен перевод на спонтанное дыхание. Однако при этом инспираторное усилие пациента должно составлять не менее –10 см вод. ст. При меньшем значении стоит рассмотреть перевод на режим SIMV (синхронизированная перемежающаяся принудительная вентиляция; англ. synchronized intermittent mandatory ventilation) со снижением принудительных вдохов на 30–50%.При PaCO2 > 60 мм рт. ст. рекомендован возврат на принудительную вентиляцию, если < 60, то при росте ЧСС, АД и ЧДД, а также при нормальном соотношении P:F можно продолжить вининг с постепенным полным отключением седативных препаратов и подачей кислорода с последующей экстубацией.
Есть моменты, которые требуют уточнения, например, 25 см вод. ст. – довольно высокий уровень пикового давления. Оно также может быть неинформативным, поскольку складывается из суммы показателей ПДКВ и величины инспираторного давления (Pinsp). Уровень Pinsp у животных со здоровыми легкими составляет 5–8 см вод. ст. (литературных данных о животных нет, значения основаны на практическом опыте ОРИТ Клиники доктора Сотникова). В своей практике мы обычно проводим отлучение от аппарата ИВЛ при уровне Ppeak не более 14–16 см вод. ст.
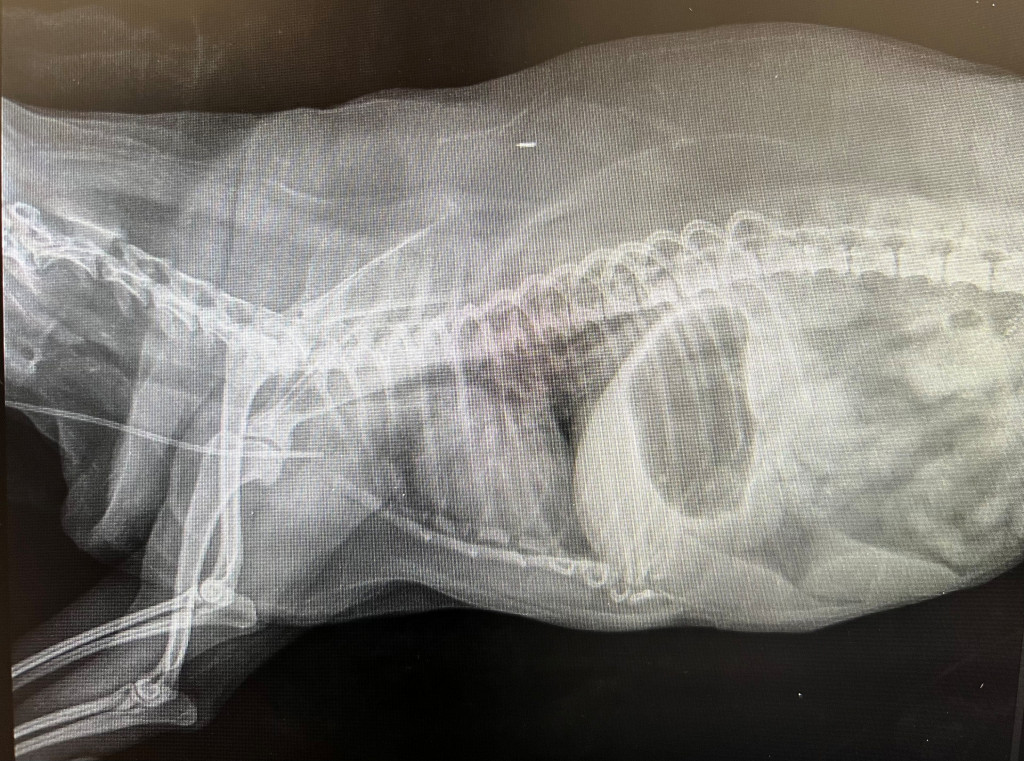
Инспираторное усилие –10 см вод. ст. – это очень высокий уровень даже для животного со здоровой паренхимой легких. Учитывается и конституция пациента: животным с избыточной массой тела требуется большее давление для достижения дыхательного объема из-за сниженной податливости. В связи с этим при принятии решения о вининге мы ориентируемся на совокупность результатов диагностических исследований и клиническое состояние пациента (рис. 2).
Чек-лист 1* – список критериев: P:F > 200 или S:F > 240, ПДКВ > 4 см вод. ст., Ppeak < 25 см вод. ст., а также сохранены пальпебральный и глотательный рефлексы, тонус челюсти, присутствуют попытки спонтанного дыхания.
Чек-лист 2** – список критериев: рост ЧСС > 25%, рост АД > 25%, изменение ЧДД > 50%, снижение или увеличение инспираторного усилия, P:F > 200 или S:F > 240.
Режим SIMV дает возможность постепенного уменьшения аппаратной поддержки. При данном режиме принудительные вдохи синхронизируются с попытками вдоха пациента, а между ними животное может делать вдохи самостоятельно, дыхательный объем спонтанного дыхания поддерживается настройкой Psupport (давление поддержки). Когда количество аппаратных вдохов минимальное, можно перевести пациента на PSV (вентиляция с поддержкой спонтанных вдохов давлением; англ. pressure support ventilation), снижая поддержку. Достижение ПДКВ до 5 см вод. ст. и Psupport – до 5 см вод. ст. является предиктором к успешному переводу на режим CPAP (спонтанная вентиляция с поддержанием постоянного положительного давления; англ. continuous positive airway pressure)1.
Существуют также интеллектуальные режимы респираторной поддержки. Данные режимы позволяют сохранить активность дыхательной мускулатуры, предотвратить асинхронию, а также упростить и ускорить отмену искусственной вентиляции легких.
Режим управления объемом с помощью давления (англ. pressure-regulated volume control; PRVC). Первый вдох происходит по принципу Volume Control с заданным целевым объемом, измеряются комплайнс пациента и давление plato, второй вдох – Pressure Control. Аппаратом определяется минимальная величина Pinsp, позволяющая за установленное врачом время вдохнуть объем, измеренный во вдохе по объему. В течение нескольких циклов подбирается уровень Pinsp, дальнейшая вентиляция производится по давлению. Колебания Pinsp составляют до 3 см вод. ст. между соседними вдохами и ограничены уровнем, который на 5 см вод. ст. ниже, чем граница тревоги.
Режим с чередованием двух уровней давления (BiLevel). Задаются постоянные PEEP high (верхний уровень) и PEEP low (нижний уровень) и две временные фазы для переключения. Режим похож на режим PCV (англ. pressure control ventilation), но в течение всего дыхательного цикла пациент может дышать спонтанно, и с ростом дыхательной активности может увеличиваться частота переключений. Со временем можно приводить верхний и нижний уровни к одному значению, тогда BiLevel будет схож с режимом PSV (англ. pressure support ventilation).
Режим пропорциональной поддержки давлением (англ. proportional assist ventilation; PAV), как и PSV, регулируется по давлению: вдох начинает пациент, а переключение на выдох выполняется по потоку. Отличие от PSV заключается в том, что аппарат устанавливает Psupport на каждый вдох, основываясь на измерении потока в начале вдоха, поддерживая дыхательный объем. В итоге пациент получает ровно ту поддержку, которая требуется ему в данный момент5.
Для определения готовности пациента к винингу также проводится проба спонтанного дыхания (SBT), которая представляет собой минимизацию поддержки аппаратом и оценку спонтанного дыхания пациента (рис. 3). Есть два основных способа проведения SBT:
- Отключение животного от ИВЛ, при этом остается только подача увлажненной газовой смеси с требуемой фракцией кислорода. Однако в таком случае затруднен респираторный мониторинг дыхательного объема (ДО).
- Кратковременное переключение на режим СPAP (постоянное положительное давление в дыхательных путях пациента) c минимальным сохранением поддержки по давлению. Плюсом такого более предпочтительного способа также является возможность быстрого возврата на принудительную вентиляцию в случае неудачи. Во время теста проводится мониторинг следующих показателей: артериальное давление, капнография, пульсоксиметрия, ЧСС, ЧДД, цвет слизистых оболочек, а также неврологический статус (наличие ажитации или, наоборот, ступора)4.
Критерии неэффективности спонтанного дыхания и необходимости вернуться на прежний режим1:
- тахипноэ;
- десатурация ниже 90%;
- гиперкапния (PaCO2 > 50 мм рт. ст.);
- дыхательный объем < 7 мл/кг;
- тахикардия;
- гипертензия;
- гипертермия или повышение температуры более чем на 1 градус.
Проблемой при проведении SBT у ветеринарных пациентов также является применение анестетиков и седативных препаратов в процессе вентиляции. При подозрении на неэффективное спонтанное дыхание из-за препаратов нужно дать животному проснуться и повторить тест.
Помимо f/Vt, есть другие респираторные маневры, также являющиеся предикторами готовности пациента к отлучению.
Показатель Р0.1 используется для количественной оценки респираторного драйва и отображает отрицательное давление в дыхательных путях пациента в первые 100 мсек спонтанного вдоха. Если пациенту тяжело дышать спонтанно или недостаточен уровень давления поддержки (на вспомогательных режимах), то активность респираторного драйва растет и Р0.1 снижается. Повышение показателя можно наблюдать при снижении комплайнса, ацидозе или низкой чувствительности триггера7.
Маневр отрицательной силы вдоха (NIF) или оценка максимального инспираторного давления. Производится задержка на вдохе, т. е. пациент пытается вдохнуть, аппарат не позволяет этого сделать, и каждая следующая попытка становится сильнее предыдущей, как следствие, нарастает давление в дыхательных путях. Значение при достижении плато на кривой «давление – время» – сила дыхательной мускулатуры5.
Р0.1 и NIF активно применяются в медицине человека, однако пока не имеют референтных значений у ветеринарных пациентов. Данные изучаются и интерпретируются самостоятельно.
Трахеостомия (ТСТ) в первые дни ИВЛ – опциональное решение. Поскольку животным не нужна настолько глубокая седация, как при наличии эндотрахеальной трубки, многие неврологические пациенты, которым необходима респираторная поддержка, вовсе не требуют седации при наличии трахеостомы.
После отлучения от инвазивной вентиляции в Клинике доктора Сотникова мы чаще всего переводим пациента на неинвазивную высокопоточную оксигенацию (ВПО) через назальные канюли (рис. 4). Плюсом является подача увлажненной и теплой газовой смеси, увеличенных фракций кислорода в первое время, что упрощает животному процесс дыхания. ВПО можно осуществлять и через трахеостомическую трубку, которая не удаляется до момента уверенности в отсутствии рисков аспирации, нормального глотания и газообмена. При сохранении стомы у пациента ВПО необходима, поскольку использование холодной и сухой газовой смеси в процессе дыхания приведет к обструкции трубки2.
Осложнения при вининге
Первостепенный ряд осложнений при вининге связан с непродуктивным спонтанным дыханием и необходимостью реинтубации и возврата на аппарат.Кроме того, при удалении эндотрахеальной трубки (ЭТТ) может произойти аспирация содержимого надманжеточного пространства, поэтому рекомендуется провести санацию незадолго до экстубации, пока позволяет уровень сознания пациента.
Можно выделить три основных осложнения, развивающихся на фоне самой длительной вентиляции:
- Прогрессирование основного заболевания. Например, при пневмонии поражен большой процент паренхимы легких и полностью вернуть функцию газообмена невозможно2.
- Приобретенная слабость дыхательных мышц, снижение эластичности грудной клетки, которые развились из-за вентиляции (начинаются уже спустя 20 часов ИВЛ).
Атрофия дыхательной мускулатуры развивается не только из-за принудительных режимов вентиляции, но и от применения миорелаксантов, из-за электролитных нарушений, развивающегося или перенесенного сепсиса. Работа дыхательных мышц оценивается при акте дыхания – исследовании на С-дуге, где видно, какие мышцы участвуют во вдохе и выдохе, как сокращается диафрагма.
- Вентилятор-ассоциированная пневмония (ВАП). Причинами являются как эндогенная флора пациента (содержимое ротоглотки, носовых пазух), так и экзогенные факторы в клинике (руки персонала, контаминированное оборудование и внутрибольничная микрофлора)6.
Заключение
Отлучение от инвазивной респираторной поддержки – многоэтапный и нужный процесс в лечении. Некоторые пациенты погибают непосредственно в момент отлучения от ИВЛ или спустя некоторое время после этого из-за несвоевременного или быстрого проведения. Комплексный подход к лечению и респираторной поддержке помогает увеличить шансы пациентов на выздоровление.Успешный вининг – предиктор выписки, за которым следует не менее сложный процесс восстановления.
Список литературы:
- Deborah C. Silverstein, Kate Hopper, BVSc, PhD, DACVECC: Critical Care Medicine, Discontinuing Mechanical Ventilation, 9780-323-76469-8, 2023.
- Neil MacIntyre: Discontinuing Mechanical Ventilatory Support; Chest 2007; 132;10491056.
- Mellema M. S., Haskins S. C. Weaning from mechanical ventilation. Clin Tech Small Anim Pract, PMID: 11109717, 2000.
- Jens Geiseler, Michael Westhoff: Weaning from invasive mechanical ventilation, PMID: 34586430, 2021.
- Горячев А. С., Савин И. А. Основы ИВЛ. М.: Медиздат, 2019.
- Светлицкая О. И., Канус И. И. Пути решения проблемы отлучения от искусственной вентиляции легких, 2020.
- Сатишур О. Е. Механическая вентиляция легких, 5-89677-034-0, 2006, с. 288–295.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург