Сокращения:
ИЛ – индолентная лимфома;
АЛ – алиментарная лимфома;
LGAL – алиментарная лимфома низкой степени злокачественности;
DLBCL – диффузная В-клеточная крупноклеточная лимфома;
TZL – лимфома Т-зоны;
MZL – лимфома маргинальной зоны;
FeLV – вирус лейкоза кошек;
ДИ – доверительный интервал;
ВЗК – воспалительные заболевания кишечника;
ИПК – инфекционный перитонит кошек;
СLL – хронический лимфолейкоз;
SLL – мелкоклеточная лимфоцитарная лимфома.
Ключевые слова: лимфома, индолентная лимфома, алиментарная лимфома.
Лимфомы – это большая группа неоплазий, значительная часть которых состоит из моноклональной популяции крупных лимфоцитов, имеет высокую степень злокачественности, агрессивное биологическое поведение и достаточно быстрое время прогрессирования от начала появления первых клинических признаков. Наиболее часто описываемый тип крупноклеточных лимфом – диффузная В-клеточная крупноклеточная лимфома (DLBCL). Общая классификация лимфоидных опухолей животных включает около 35 подтипов. Меньшая группа лимфом представляет собой опухоли, которые состоят преимущественно из мелких и средних лимфоцитов и отличаются от крупноклеточных лимфом медленным прогрессированием симптомов, смазанной клинической картиной и определенными трудностями в постановке диагноза.
На долю мелкоклеточных лимфом из всех лимфопролиферативных заболеваний у собак приходится около 29%1, у кошек – 11%. При этом самой распространенной формой индолентной лимфомы у кошек является алиментарная мелкоклеточная Т-клеточная лимфома (50–80% случаев от общего количества алиментарных лимфом), а у собак – лимфома Т-зоны (около 60% от общего количества индолентных лимфом).
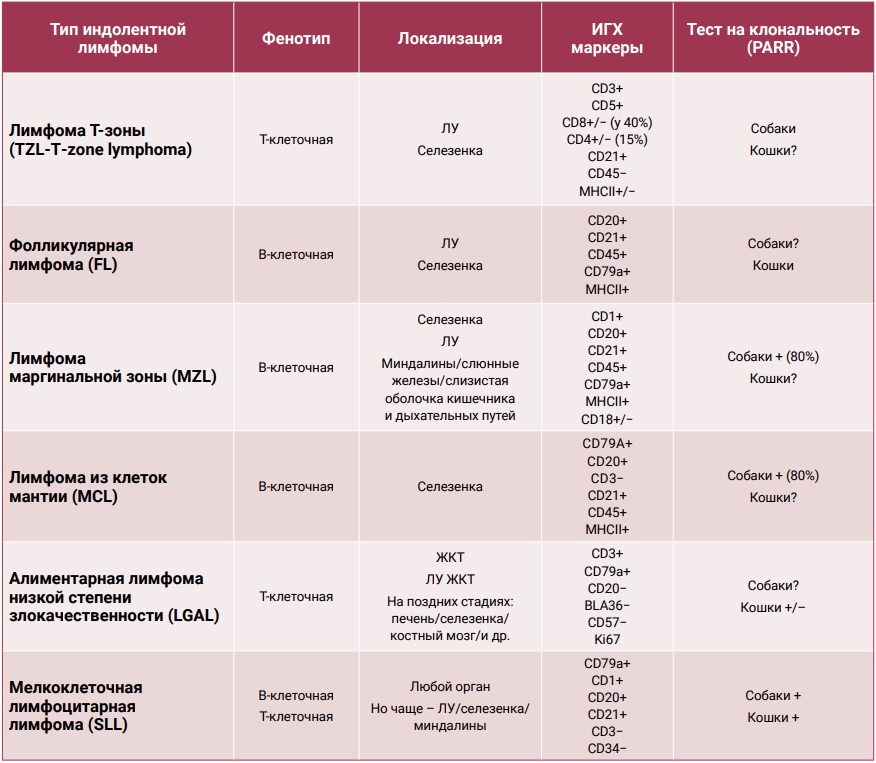
К индолентным лимфомам относят следующие подтипы:
- фолликулярная лимфома (ФЛ);
- лимфома маргинальной зоны (MZL);
- лимфома из клеток мантии (MCL);
- лимфома Т-зоны (TZL);
- алиментарная лимфома низкой степени злокачественности (LGAL);
- мелкоклеточная лимфоцитарная лимфома (SLL).
Этиология и клинические признаки (табл. 2)
Длительное время ИЛ могут оставаться бессимптомными (подстадия а) и проявляться увеличением одного/группы лимфатических узлов (ЛУ) или мультицентрическим вовлечением всех лимфатических узлов. Также возможно первичное поражение только селезенки (как единственного органа) либо характерное для развития IV стадии заболевания прогрессирование болезни из ЛУ. При этом поражения селезенки могут быть как в виде нодулярных образований, так и в виде диффузных поражений.Симптомы подстадии b чаще всего смазанные, неспецифические, включают постепенно прогрессирующую апатию, хроническую потерю веса, периодическую лихорадку, снижение аппетита и наличие сопутствующих заболеваний, например демодекоза (выявляется в 50% случаев у собак с индолентной лимфомой)10 или других неоплазий. При этом считается, что развитие вторичной неоплазии и демодекоза будет связано с длительной иммуносупрессией в связи с возникновением дефектов в противоопухолевом иммунитете на фоне лимфопролиферативного заболевания.
Поражение лимфомой селезенки (например, лимфома Т-зоны или маргинальной зоны) часто приводит к разрыву капсулы органа и гемоабдомену12,13,14.
Гематологические изменения возникают как вследствие поражения костного мозга (миелофтиз), так и без его поражения, и могут включать анемию (регенераторную/нерегенераторную), тромбоцитопению, лейкопению, лейкоцитоз и лимфоцитоз.
Методы и особенности диагностики
Диагностика ИЛ может представлять собой определенную трудность, и связано это с несколькими факторами. Данные опухоли состоят из мелких и средних лимфоцитов, которые часто сложно отличить от реактивной инфильтрации, и, что важно понимать, в зависимости от типа ИЛ инфильтрация опухолевыми клетками происходит не диффузно, поражая весь ЛУ, а локально, затрагивая определенные зоны органа. В результате тонкоигольная и толстоигольная биопсии часто дают ложноотрицательные результаты из-за того, что в биоптаты не попадает пораженный участок ткани. Именно по этой причине для биопсии рекомендуется полное удаление ЛУ либо проведение клиновидной биопсии с захватом всех слоев органа. Для биопсии селезенки могут быть актуальными отбор материала из нодулы (при нодулярном поражении) и интерпретация результата в зависимости от процентного содержания клеточного состава и структуры органа11.Цитология как метод диагностики ИЛ в большинстве случаев не даст клиницисту однозначной информации по причинам, описанным выше. При диффузной инфильтрации органа опухолевыми лимфоцитами цитологическая картина образцов ткани может характеризоваться наличием большого количества мелких и средних лимфоцитов, которые сложно отличить от реактивных. В таком случае возможно применение теста на подтверждение клональности лимфоцитов (PARR)18, например в лимфомах из клеток мантии у собак клональность обнаруживается в 80% случаев. Однако (согласно данным нескольких современных исследований) следует помнить, что для диагностики алиментарных мелкоклеточных лимфом специфичность и чувствительность этого теста достаточно низкая и имеет высокий риск получения как ложноположительных, так и ложноотрицательных результатов15,16. Также по результатам исследования, проведенного в 2019 году, было установлено отсутствие клональности фолликулярных лимфом у кошек5.
Из-за большого количества противоречивых исследований мы не можем использовать PARR как единственный источник подтверждения заболевания. И наконец, считается, что при гистологически очевидном диагнозе тест на клональность делать излишне.
Для диагностики ИЛ существует несколько новых систем, которые находятся на стадии разработки и доклинических исследований.
Лечение
Многие ИЛ являются бессимптомными, поэтому таким пациентам длительное время не назначают лечение, за ними рекомендовано активное наблюдение, которое представляет собой регулярный мониторинг: физикальный осмотр, общеклинический анализ крови с исследованием мазка крови, а также ультразвуковое исследование селезенки и печени на неспецифические мегалии. Первоначально такие животные осматриваются ежемесячно, а далее (при стабильном состоянии) – не реже одного раза в 2–3 месяца.Утверждается, что терапию необходимо начинать только тогда, когда появляются общие симптомы заболевания, прогрессирующий лимфоцитоз в крови становится выше 9 тыс. кл/мкл, возникают клинически значимые цитопения, массивная или прогрессирующая лимфаденопатия, гепатоспленомегалия.
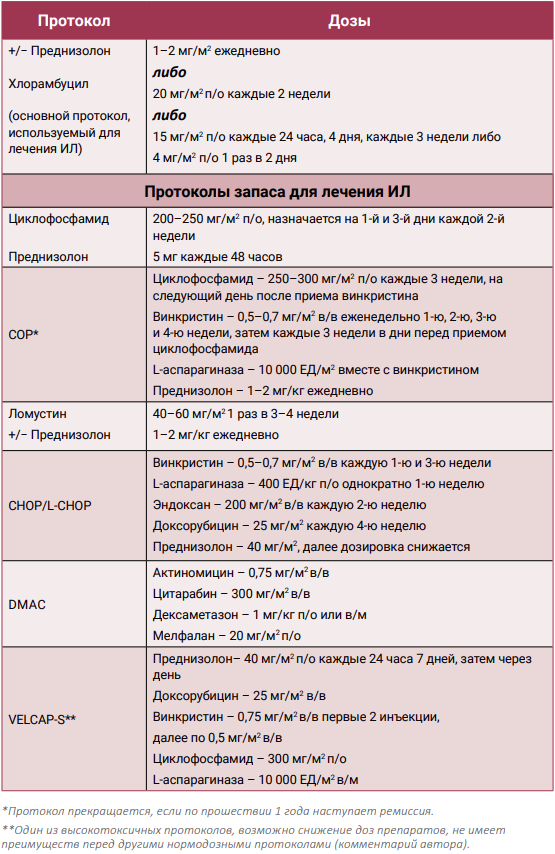
Препаратами выбора для лечения ИЛ являются хлорамбуцил и преднизолон. Кроме этого, существуют протоколы запаса (препараты второго, третьего выбора), которые включают циклофосфамид, ломустин и другие цитостатики (табл. 3). Также опубликованы данные нескольких исследований, где описывается терапия ИЛ с использованием протоколов, применяющихся в лечении крупноклеточных лимфом. Данные протоколы не показали преимуществ перед низкодозной химиотерапией (ХТ). Известно, что некоторые ИЛ могут прогрессировать до диффузной В-клеточной крупноклеточной лимфомы (DLBCL), в этом случае применение стандартных протоколов лечения агрессивных лимфом будет оправданным.
Для лечения первичных ИЛ селезенки с наличием или отсутствием прогресса в регионарные лимфатические узлы и без признаков поражения других органов методом выбора является спленэктомия без проведения дальнейшей ХТ. По данным нескольких исследований, химиотерапия не увеличивает продолжительность жизни пациентов с первичными селезеночными лимфомами12,13,14.
Продолжительность лечения не установлена, однако возможна его отмена после одного года терапии при условии достижения полной клинической ремиссии и своевременного обследования пациентов на момент возникновения рецидива. При повторном появлении заболевания необходимо возобновить прием преднизолона и хлорамбуцила. При устойчивых формах или прогрессировании заболевания на фоне применяемого лечения необходимо перейти на протокол запаса (табл. 3). Прогноз для пациентов с большинством ИЛ, как правило, хороший. Большая часть больных животных погибает от развития сопутствующих заболеваний (вследствие развития ИЛ) или по другим причинам.
Далее мы рассмотрим отдельные, наиболее часто встречающиеся типы индолентных лимфом.
Фолликулярная лимфома (ФЛ) – это мелкоклеточная В-клеточная индолентная лимфома, которая происходит из В-клеток фолликулярного центра. У людей данный тип ИЛ занимает второе место по встречаемости, у собак же составляет всего 1%3,4 от неходжкинских лимфом, а у кошек – 18 случаев на 602 животных5. Также зарегистрированы случаи развития ФЛ у лошадей и крупного рогатого скота. ФЛ относится к узловым формам лимфом, обычно поражаются лимфатические узлы и/или селезенка. Первичное поражение селезенки встречается реже, чем ЛУ, при этом селезенка не будет вовлечена диффузно, а будут наблюдаться нодулярные поражения.
Основной дифференциальный диагноз – это доброкачественная фолликулярная гиперплазия (BFH) или доброкачественная атипичная фолликулярная гиперплазия (BAFH). Однако, по данным нескольких исследований, среднее время выживаемости у собак с обеими формами заболевания было равнозначное (около 350 дней). По мнению авторов, это может быть связано с ошибкой интерпретации результатов и с недостаточной диагностикой6.
Средний возраст для кошек – 7 лет, также зарегистрированы случаи обнаружения ФЛ у животных в возрасте от 7 месяцев до 15 лет5. Для собак средний возраст не установлен в связи с тем, что зарегистрированная встречаемость ФЛ у них крайне низкая.
Большинство животных с ФЛ имеют подстадию а, единственный симптом которой – увеличение лимфатических узлов. Чаще всего поражаются ЛУ головы и шеи, но могут быть вовлечены и любые другие лимфатические узлы, возможно также мультицентрическое поражение.
На поздних этапах заболевания будут вовлекаться печень и костный мозг, неопластические клетки при поражении печени будут расположены периваскулярно в триадах и вокруг центральных вен. При поражении костного мозга опухолевые клетки в крови обычно не обнаруживаются (в отличие от людей с ФЛ), однако могут наблюдаться цитопении из-за миелофтиза.
Среднее время выживаемости у кошек и собак значительно варьируется. У собак медиана выживаемости составляет около одного года, независимо от лечения, а у кошек – 5,8 лет в случае проведения лечения и около 1,5 лет без лечения5. При этом подстадия b и мультицентрическое поражение ЛУ будут считаться отрицательным прогностическим фактором.
Лимфома Т-зоны (TZL) – это наиболее распространенная форма индолентной лимфомы у собак, которая составляет примерно 5–15% от всех лимфом и примерно 60% от ИЛ. Крайне редко встречается у кошек. Породная предрасположенность есть у золотистых ретриверов (40–50%), ши-тцу, боксеров и терьеров7. Средний возраст пациентов – 8–10 лет.
Лимфома Т-зоны возникает из малых и средних лимфоцитов в периартериальной Т-зоне ЛУ и, реже, селезенки. Считается, что данная разновидность лимфом имеет крайне низкий митотический индекс, с этим связывают медленное развитие (в течение 1–2 лет до появления клинических признаков) и прогрессирование заболевания.
Основные симптомы – увеличение одного или нескольких нижнечелюстных ЛУ в области головы и шеи, реже наблюдаются другие поверхностные лимфаденопатии. Все ЛУ подвижные и безболезненные, у 25–80% пациентов зарегистрирован умеренный лимфоцитоз 6–15 тыс. кл/мкл, однако диапазон может варьироваться от 1 до 82 тыс. кл/мкл, также наблюдаются панцитопении (менее 10%), чаще всего умеренные. Большая часть животных имеет подстадию a, то есть бессимптомное течение. Чаще всего на момент обращения к врачу у собак уже диагностируется IV или V стадия заболевания из-за поражения периферической крови или костного мозга. Интересно то, что наличие лимфоцитов чаще связано с выбросом опухолевых клеток из первичного образования, а не с поражением костного мозга. Кроме того, наличие лимфоцитоза ниже 9 тыс. кл/мкл не будет являться негативным прогностическим фактором.
Медиана выживаемости может достигать 4,4 лет1. Нет в достаточной мере подтвержденной информации о влиянии ХТ на продолжительность жизни животных. Основная тактика лечения при данном типе лимфом заключается в активном наблюдении пациентов, назначении противоопухолевой терапии с момента появления клинических признаков и при условии снижения качества жизни животных из-за заболевания (см. выше раздел «Лечение ИЛ»). Среднее время выживаемости может достигать 44 месяцев в случаях применения сочетанного лечения хлорамбуцилом и преднизолоном и 22 месяца при использовании протокола CНОР. Однако большинство животных может погибнуть в результате развития сопутствующих патологий, а не от основного заболевания1.
Основной дифференциальный диагноз – гиперплазия Т-зоны, но при этом известно, что развитие лимфомы Т-зоны сопровождается утратой антигена CD45, который сохранен в нормальных или реактивных лимфоцитах, что может быть полезным маркером для дифференциации лимфоидной гиперплазии и TZL1.
Продолжение Часть 2
Список литературы:
- Flood-Knapik K. E., Durham A. C., Gregor T. P., Sánchez M. D., et al. Clinical, histopathological and immunohistochemical characterization of canine indolent lymphoma. Veterinary and Comparative Oncology, 11(4), 272–286, 2012.
- Vezzali E., Parodi A. L., Marcato P. S. Histopathologic classification of 171 cases of canine and feline non-Hodgkin lymphoma according to the WHO. Veterinary and Comparative Oncology, 8(1), 38–49, 2010.
- Ponce F., Marchal T., Magnol J. P., Turinelli V., Ledieu D., Bonnefont C., et al. A morphological study of 608 cases of canine malignant lymphoma in France with a focus on comparative similarities between canine and human lymphoma morphology. Veterinary Pathology, 47: 414–433, 2010.
- Valli V. E., San Myint M., Barthel A., Bienzle D., Caswell J., Colbatzky F., et al. Classification of canine malignant lymphomas according to the World Health Organization criteria. Veterinary Pathology, 48: 198–211, 2011.
- Henrich M., Bauknecht A., Hecht W., & Reinacher M. Lack of Bcl-2 expression in feline follicular lymphomas. Journal of Veterinary Diagnostic Investigation, 2019.
- Tumors in domestic animals, edited by Donald J. Meuten, 2017.
- Seelig D. M., Avery P., Webb T., Yoshimoto J., Bromberek J., et al. Canine T-zone lymphoma: unique immunophenotypic features, outcome, and population characteristics. Journal of Veterinary Internal Medicine, 28: 878–886, 2014.
- Flood-Knapik K. E., Durham A. C., Gregor T. P., Sanchez M. D., et al. Clinical, histopathological and immunohistochemical characterization of canine indolent lymphoma. Veterinary and Comparative Oncology, 11: 272–286, 2013.
- Seelig D. M., et al. Canine T-zone lymphoma: unique immunophenotypic features, outcome, and population characteristics. Journal of veterinary internal medicine, 28.3: 878–886, 2014.
- De Lorimier L-P., Campbell O. Canine T-zone lymphoma: an apparent risk factor for adult‐onset demodicosis. Journal of Small Animal Practice, 61.5: 323–324, 2020.
- Moore A. S., et al. Histologic and immunohistochemical review of splenic fibrohistiocytic nodules in dogs. Journal of veterinary internal medicine, 26.5: 1164–1168, 2012.
- Lucinda van Stee, 12. Sarah E12. .12. Boston, et al. Outcome and prognostic factors for canine splenic lymphoma treated by splenectomy (1995–2011). Veterinary Surgery, 44.8: 976–982, 2015.
- O'Brien D., 13. Moore P. F., et al. Clinical characteristics and outcome in dogs with splenic marginal zone lymphoma. Journal of veterinary internal medicine, 27.4: 949–954, 2013.
- Stefanello D., Valenti P., et al. Splenic marginal zone lymphoma in 5 dogs (2001–2008). Journal of veterinary internal medicine, 25.1: 90–93, 2011.
- Marsilio S., Ackermann M. R., Lidbury J. A., Suchodolski J. S., Steiner J. M. Results of histopathology, immunohistochemistry, and molecular clonality testing of small intestinal biopsy specimens from clinically healthy client-owned cats. J Vet Intern Med, 33: 551-558, 2019.
- Marsilio S., Newman S. J., Estep J. S., et al. Differentiation of lymphocytic-plasmacytic enteropathy and small cell lymphoma in cats using histology-guided mass spectrometry. J Vet Intern Med, 34: 669-677, 2020.
- Manfred Henrich, et al. Lack of Bcl-2 expression in feline follicular lymphomas. Journal of Veterinary Diagnostic Investigation, 31.6: 809–817, 2019.
- Ehrhart E. J., et al. Polymerase chain reaction for antigen receptor rearrangement: Benchmarking performance of a lymphoid clonality assay in diverse canine sample types. Journal of veterinary internal medicine, 33.3: 1392–1402, 2019.
- Franz, A.M., Sarver, A.L., Ito, D., et al. (2013) Molecular profiling reveals prognos tically significant subtypes of canine lymphoma. Vet Pathol. 50:693–703.
- Richards, K.L., Motsinger‐Reif, A.A., Chen, H.W., et al. Gene profiling of canine B‐cell lymphoma reveals germinal center and post germinal center subtypes with different survival times, modeling human DLBCL. Cancer Res. 73:5029–5039, 2013.
- Barrs, Vanessa, and Julia Beatty. Feline alimentary lymphoma: 1. Classification, risk factors, clinical signs and non-invasive diagnostics. Journal of Feline Medicine and Surgery .14.3: 182-190, 2012.
- Vanessa R Barrs, Julia Beatty. Feline alimentary lymphoma: 2. Further diagnostics, therapy and prognosis. Journal of feline medicine and surgery. 14.3: 191-201, 2012.
- Mathieu V Paulin, et al. Feline low-grade alimentary lymphoma: an emerging entity and a potential animal model for human disease." BMC veterinary research. 14.1: 1-19, 2018.
- Rissetto K, Villamil JA, Selting KA, Tyler J, Henry CJ. Recent trends in feline intestinal neoplasia: an epidemio- logic study of 1129 cases in the Veterinary Medical Database from 1964 to 2004. J Am Anim Hosp Assoc. 47: 28–36, 2011.
- Mardell Ellie. Is there a link between tobacco smoke exposure and the development of alimentary lymphoma in cats? Veterinary Record. 186.13: 411-413, 2020.
- Moore PF, Woo JC, Vernau W, Kosten S, Graham PS. Characterization of feline T cell receptor gamma (TCRG) variable region genes for the molecular diagnosis of feline intestinal T cell lymphoma. Vet Immunol Immunopathol; 106: 167–178, 2005.
- Briscoe KA, Krockenberger M, Beatty JA, Crowley A, et al. Histopathological and immunohisto- chemical evaluation of 53 cases of feline lymphoplasma- cytic enteritis and low-grade alimentary lymphoma. J Comp Pathol; 145: 187–198, 2011.
- Lingard AE, Briscoe K, Beatty JA, Moore AS, Crowley AM, et al. Low-grade alimentary lymphoma: clinicopathological findings and response to treatment in 17 cases. J Feline Med Surg; 11: 692–700,2009.
- Carreras JK, Goldschmidt M, Lamb M, McLear RC, Drobatz KJ, Sorenmo KU. Feline epitheliotropic intestinal malig- nant lymphoma: 10 cases (1997–2000). J Vet Intern Med; 17: 326–331, 2003.
- Hart JR, Shaker E, Patnaik E and Garvey MS. Lymphocytic- plasmacytic enterocolitis in cats: 60 cases (1988–1990). J Am Anim Hosp Assoc; 30: 505–514, 1994.
- Davenport DJ, Leib NS, Roth L. Progression of lymphocytic-plasmacytic enteritis to gastrointestinal lymphosarcoma in three cats. Proceedings of the Veterinary Cancer Society, 1987.
- Kiupel M, Smedley RC, Pfent C, Xie Y, et al. Diagnostic algorithm to differentiate lymphoma from inflammation in feline intestinal biopsy specimens. Vet Pathol; 48: 212–222, 2011.
- Cesari A, Bettini G, Vezzall E. Feline intestinal T-cell lymphoma: assessment of morphologic and kinetic features in 30 cases. J Vet Diagn Invest; 21: 277–279, 2009.
- Moore, Peter F., A. Rodriguez-Bertos, Philip H. Kass. Feline gastrointestinal lymphoma: mucosal architecture, immunophenotype, and molecular clonality. Veterinary pathology; 49.4: 658-668, 2012.
- Beatty JA, Lawrence CE, Callanan JJ, Grant CK, et al. Feline immunodeficiency virus (FIV)-associated lymphoma: a potential role for immune dysfunction in tumourigenesis. Vet Immunol Immunopathol. 1998; 65: 09–22.
- Lutz H, Pedersen NC, Theilen GH. Course of feline leukemia virus infection and its detection by enzymelinked immunosorbent assay and monoclonal antibodies. Am J Vet Res. 44: 2054–9, 1983.
- Bridgeford EC, Marini RP, Feng Y, Parry NMA, Rickman B, et al. Gastric helicobacter species as a cause of feline gastric lymphoma: a viable hypothesis. Vet Immunol Immunopathol; 123:106–13, 2008.
- Hoehne SN, McDonough SP, Rishniw M, Simpson KW. Identification of mucosa-invading and intravascular Bacteria in feline small intestinal lymphoma. Vet Pathol. 54:234–41, 2017.
- Gianella P, Pietra M, Crisi PE, Famigli Bergamini P, et al. Evaluation of clinicopathological features in cats with chronic gastrointestinal signs. Pol J Vet Sci. 20:403–10, 2017.
- Stein TJ, Pellin M, Steinberg H, Chun R. Treatment of feline gastrointestinal small-cell lymphoma with chlorambucil and glucocorticoids. J Am Anim Hosp Assoc. 46:413–7, 2010.
- Kiselow MA, Rassnick KM, McDonough SP, Goldstein RE, et al. Outcome of cats with low-grade lymphocytic lymphoma: 41 cases (1995-2005). J Am Vet Med Assoc. 232:405–10, 2008.
- Fondacaro JV, Richter KP, Carpenter JL, Hart JR, Hill SL, Fettman MJ. Feline gastrointestinal lymphoma: 67 cases (1988–1996).
- Eur J Comp Gastroenterol. 1999;4:5–11. Pope KV, Tun AE, McNeill CJ, Brown DC, Krick EL. Outcome and toxicity assessment of feline small cell lymphoma: 56 cases (2000–2010). Vet Med Sci.1:51–62, 2015.
- Vail DM, Moore AS, Ogilvie GK, Volk LM. Feline lymphoma (145 cases): proliferation indices, cluster of differentiation 3 immunoreactivity, and their association with prognosis in 90 cats. J Vet Intern Med. 12:349–54, 1998.
- Zwahlen CH, Lucroy MD, Kraegel SA, Madewell BR. Results of chemotherapy for cats with alimentary malignant lymphoma: 21 cases (1993-1997). J Am Vet Med Assoc. 213:1144–9,1998.
- Campbell M. W., Hess P. R., Williams L. E. Chronic lymphocytic leukaemia in the cat: 18 cases (2000–2010). Veterinary and comparative oncology. Т. 11. – №. 4. – С. 256-264, 2013.
- Weiss D. J., Wardrop K. J. (ed.). Schalm's veterinary hematology. John Wiley & Sons, 2011.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург