г. Санкт-Петербург.
Введение
Лимфома (злокачественная лимфома или лимфосаркома) представляет собой группу новообразований, происходящих из опухолевых лимфоцитов. Эти новообразования локализуются преимущественно в лимфоидных тканях, таких как лимфатические узлы (ЛУ), селезенка и костный мозг. Однако лимфомы могут развиваться практически в любой ткани организма, что определяет клиническую форму заболевания и степень его злокачественности. Ежегодная заболеваемость лимфомой у собак и кошек трудно поддается точной оценке из-за отсутствия национального регистра опухолей у этих видов животных. Тем не менее данное злокачественное новообразование является одним из наиболее распространенных у собак и кошек. По различным оценкам, ежегодная заболеваемость лимфомой среди собак колеблется от 13 до 114 случаев на 100 000 животных в группе риска. Показатели варьируются в зависимости от возраста: у собак младше 1 года заболеваемость составляет около 1,5 случаев на 100 000, а у собак в возрасте от 10 до 11 лет – 84 случая на 100 0001.Лимфомы кошек можно классифицировать по анатомическому расположению (медиастинальная, алиментарная, мультицентрическая и другие формы лимфомы, такие как ренальная, назальная и окулярная)1,2 и по размеру клеток (мелкие, средние или крупные)3. Наиболее часто заболевание диагностируется у пациентов среднего возраста (примерно 11 лет), однако возрастной диапазон может быть достаточно широким3,4.
Лечение
Основным вариантом лечения лимфомы до сих пор остается многокомпонентная цитотоксическая противоопухолевая терапия (химиотерапия)3-9. При комплексном лечении различных по месту локализации форм лимфом с использованием противоопухолевых препаратов показатели общего ответа (англ. overall response rate; ORR) варьируются в широком диапазоне – от 40 до 95% в зависимости от применяемого протокола, а общее медианное время выживания (англ. overall survival time; OST) может составить от 50 до 388 дней7-15. К сожалению, существует ограниченное количество публикаций, посвященных общему времени выживания кошек с лимфомой, получавших в качестве единственного метода лечения только глюкокортикоиды.Применение гормональных препаратов в качестве единственного метода лечения обычно приводит к увеличению продолжительности жизни не более чем на 3 месяца. В то же время в сочетании с применением химиотерапии этот показатель может увеличиться до 6–9 месяцев, что существенно отличается от показателей у собак13,14. При отсутствии лечения среднее время выживания пациентов составляет 6–8 недель6. Несмотря на разнообразие протоколов лечения лимфомы у кошек, около
65 –75% пациентов демонстрируют положительный ответ на начальную противоопухолевую терапию, независимо от выбранного метода лечения.
Применение противоопухолевой терапии с использованием пегаспаргазы (ONCASPAR®)
(обзор на основе опубликованных данных)
Противоопухолевая терапия остается основным методом лечения лимфомы у кошек и собак.
Традиционное лечение включает основной многокомпонентный протокол противоопухолевой терапии, состоящий из циклофосфамида, винкристина и преднизолона (COP) или циклофосфамида, доксорубицина, винкристина и преднизолона (CHOP). Данные по эффективности обоих протоколов лечения, по-видимому, в значительной степени сопоставимы, и поэтому добавление доксорубицина не оказывает статистически значимого влияния на выживаемость кошек. Общие показатели ответа для протокола на основе COP варьируются от 39 до 96% при медианном общем времени выживания (OST) 45–388 дней, тогда как для протоколов на основе CHOP показатели ответа – от 38 до 95% при OST 97–657 дней4,14,15.
Также в литературе описаны протоколы противоопухолевой терапии с применением аспарагиназы, L-аспарагиназы и пегаспаргазы как в составе мототерапии, так и в комплексе с другими мультимодальными противоопухолевыми протоколами.
Аспарагиназа (АСП) – это бактериальный фермент, получаемый из Escherichia coli или Erwinia chrysanthemi. Под действием аспарагиназы истощаются запасы аспарагина в сыворотке крови. Клетки острого лимфобластного лейкоза (ОЛЛ) и лимфобластной лимфомы (ЛЛБ), в отличие от большинства здоровых клеток, характеризуются низким уровнем или полным отсутствием фермента аспарагинсинтетазы и поэтому в значительной степени зависят от экзогенного аспарагина, циркулирующего в крови14-17. При достаточном уровне активности аспарагиназы истощается сывороточный аспарагин, что в конечном итоге приводит к апоптозу опухолевых клеток, характеризующихся дефицитом аспарагинсинтетазы20-21.
За последние десятилетия схемы на основе аспарагиназы (АСП) стали ключевым элементом успешной терапии ОЛЛ и неходжкинских лимфом/ЛЛБ у людей8, 9. Однако из-за определенных терапевтических ограничений и спектра токсичности нативная форма аспарагиназы недоступна в продаже (в отличие от ряда стран, в том числе Российской Федерации). В связи с этим во многих странах ее применение было заменено на пегилированную версию – пегилированную аспарагиназу (пегаспаргазу)21.
Пегаспаргаза обладает рядом преимуществ, включая сниженную иммуногенность, что приводит к уменьшению частоты реакций гиперчувствительности и снижению выработки антител к аспарагиназе. Кроме того, пегаспаргаза характеризуется значительно более длительным периодом полураспада, что позволяет уменьшить частоту введений препарата по сравнению с нативным ферментом. В медицине человека включение пегаспаргазы в состав интенсивного многокомпонентного протокола химиотерапии показало высокую эффективность, несмотря на развитие терапевтически контролируемой токсичности преимущественно у взрослых пациентов и значительно реже – у детей20-22.
В контексте лечения лимфомы у собак было показано, что пегаспаргаза демонстрирует сопоставимую эффективность с L-аспарагиназой23,24. Недавнее исследование подтвердило эффективность применения пегаспаргазы в качестве дополнения к стандартным и модифицированным режимам химиотерапии, включающим циклофосфамид, винкристин и преднизолон (COP), у кошек25.
С учетом данных научных публикаций и возможностей владельцев в применении пегаспаргазы целью этого исследования было изучение эффективности пегаспаргазы (Oncaspar®) в комбинации с ломустином (CCNU) при лечении кошки с крупноклеточной лимфомой (мультицентрическими поражениями) в качестве потенциальной альтернативы паллиативному лечению кортикостероидами животных, владельцы которых отказываются от цитотоксической противоопухолевой терапии.
Клинический случай
Пациент:кошка породы русская голубая в возрасте 17 лет и 1 месяц (на момент первичного обращения). Не вакцинирована, дегельминтизация проводится с периодичностью 1 разв 3–4 месяца с использованием препарата, содержащего в качестве действующих веществ мильбемицина оксим и празиквантел.
Владельцы обратились с жалобами на изменение в поведении питомца, несвоевременное отправление естественных нужд в непривычных местах, появление рвоты, а при попытках принудительного кормления – отсутствие интереса к пище.
Анамнез жизни животного отягощен наличием хронической болезни почек, холангиогепатита, хронического панкреатита и бронхиальной астмы, находящихся в состоянии ремиссии. На момент обращения вес пациента составлял 3370 граммов.
При осмотре и пальпации периферических лимфатических узлов не было выявлено никаких изменений. При пальпации брюшной полости обнаружено объемное безболезненное и высокоподвижное новообразование. Внешняя оценка состояния животного показала наличие дегидратации в пределах 4%.
Диагностика
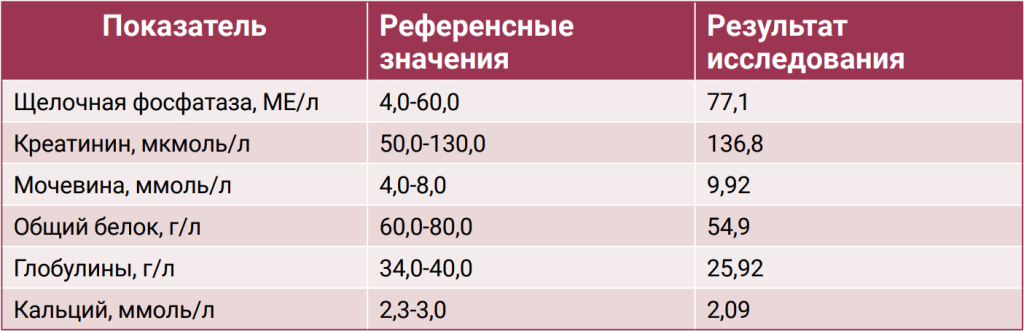
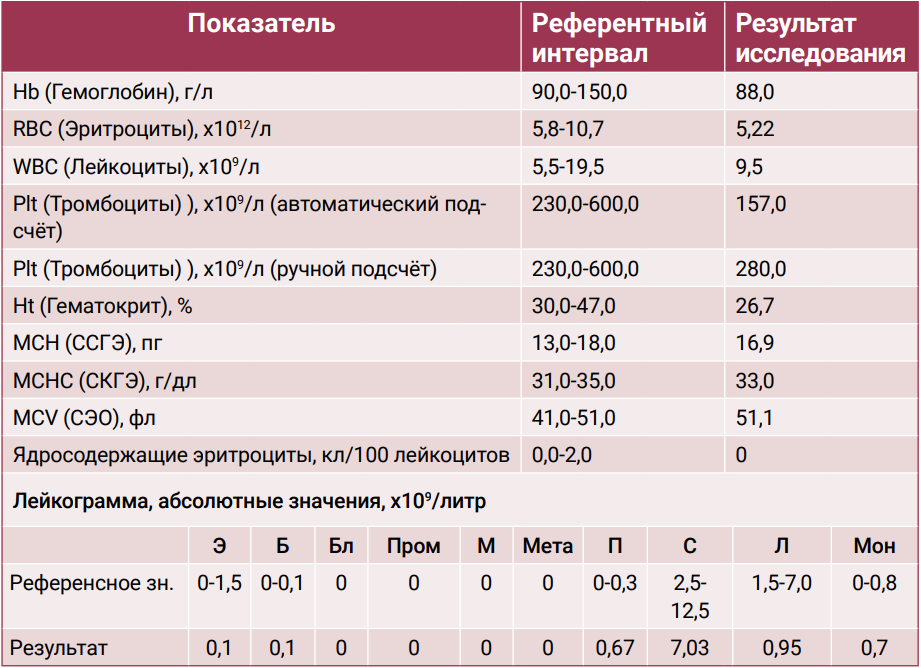
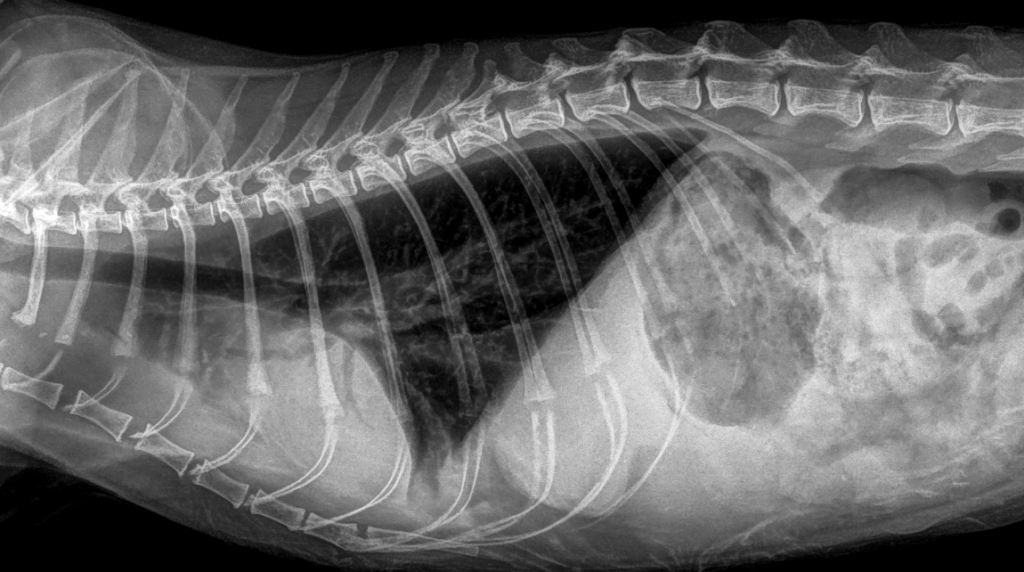
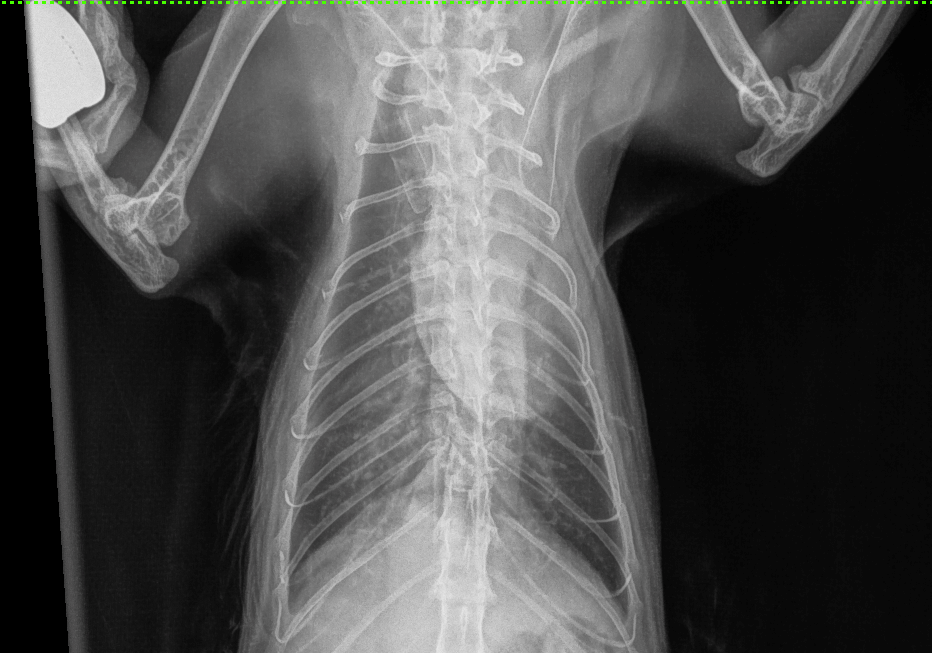
При биохимическом анализе сыворотки крови выявлено незначительное повышение уровней креатинина и мочевины, что согласуется с наличием в анамнезе хронической болезни почек у данного пациента (табл. 1). Клинический анализ крови демонстрирует выраженные изменения в составе эритроцитов (красных кровяных телец), что может свидетельствовать о развитии у пациента регенераторной анемии (табл.2), поскольку количество ретикулоцитов у него находится в пределах нормы (табл. 3). В свою очередь анемия как паранеопластический синдром отмечается у 43–58% кошек с лимфомой и у 30–43% собак. Она является неблагоприятным прогностическим фактором для обоих видов животных32-34.Рентгенография. После проведения рентгенографии грудной клетки в вентродорсальной и латеролатеральной проекциях выявлены следующие изменения: затемнение в области краниальных долей легких, сглаженность тени сердца. На рентгенограммах также обнаружены затемнения в каудальных долях легких, соответствующие ателектазу и смещению вентральной границы между вентральной стенкой грудной клетки, что может указывать на развитие гидроторакса в умеренном количестве (рис. 1, 2)
В качестве дополнительного метода диагностики было выполнено УЗИ, которое позволило выявить значимые изменения в органах брюшной и грудной полостей. В брюшной полости обнаружены небольшое количество свободной жидкости (до 6 мм локально) и новообразование стенки кишечника с локальным утолщением до 17,8 мм и максимальным диаметром 48 мм, содержащее гиперэхогенные включения. Просвет кишки при этом не был нарушен, но наблюдалась сниженная перистальтическая активность. Слоистость стенки ободочной и прямой кишки сохранена, перистальтика снижена, но не нарушена. При исследовании мезентериальных лимфатических узлов выявлена выраженная гиперплазия основных и добавочных узлов, включая каудальные мезентериальные лимфатические узлы, увеличенные до 25 мм, с признаками сниженной эхогенности. Также обнаружены ультразвуковые признаки диффузного оментита по всей брюшной полости.
В грудной полости при УЗИ выявлены признаки наличия свободной жидкости до 3 мм в области диафрагмы и объемного новообразования в краниальном средостении.
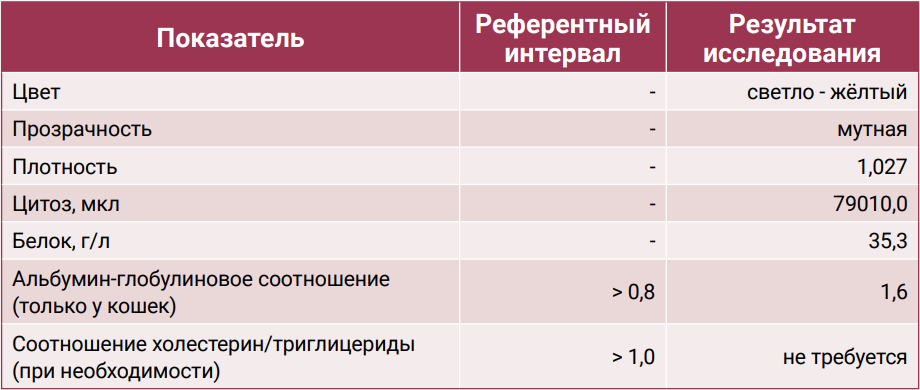
На основании полученных данных было принято решение о проведении аспирации свободной жидкости (табл. 4), тонкоигольной биопсии новообразования кишечника и новообразования краниального средостения с последующим направлением пациента на неселективную КТ-ангиографию.
Цитология выпотной жидкости: клеточный состав представлен большим количеством округлых мононуклеарных клеток, расположенных дискретно. Наблюдается выраженный анизоцитоз и анизокардиоз. Ядра клеток имеют округлую форму с неровным ядерным контуром, у части клеток ядра имеют причудливую форму. Хроматин варьируется от зернистого до грубозернистого; в некоторых клетках визуализируются 1-3 округлые нуклеолы разного размера, включая макронуклеолы. Цитоплазма варьируется от скудной до умеренной, от светло-базофильной до темно-базофильной.
У части клеток обнаруживаются множественные мелкие вакуоли и цитоплазматические выросты, а также мелкие оксифильные гранулы. Присутствуют двухъядерные клетки и атипичные митозы. Встречаются небольшое количество активированных макрофагов, часть из которых находятся в состоянии лейкофагоцитоза, а также небольшое количество малых лимфоцитов и недегенеративных нейтрофилов.
Фон представлен единичными эритроцитами и разрушенными клетками.
Инфекционные агенты не обнаружены.
Заключение: неопластический выпот
Дифференциальный диагноз « крупноклеточная анапластическая лимфома».
Результат цитологического исследования новообразования тощей кишки
При проведении цитологического исследования новообразования тощей кишки (5 стекол) обнаружены большое количество средних и больших мононуклеарных клеток, расположенных дискретно. Ядра крупные, округлой формы, с хроматином от нежного сетчатого до зернистого, в некоторых клетках визуализируются 1-2 средние нуклеолы. Цитоплазма скудная, базофильная, в единичных клетках визуализируются пылевидные оксифильные гранулы. Встречается небольшое/умеренное количество малых лимфоцитов и единичные недегенеративные нейтрофилы.
Фон представлен умеренным количеством эритроцитов, лимфогландулярными тельцами, разрушенными клетками.
Инфекционные агенты в данном материале не обнаружены.
Заключение: крупноклеточная лимфома.
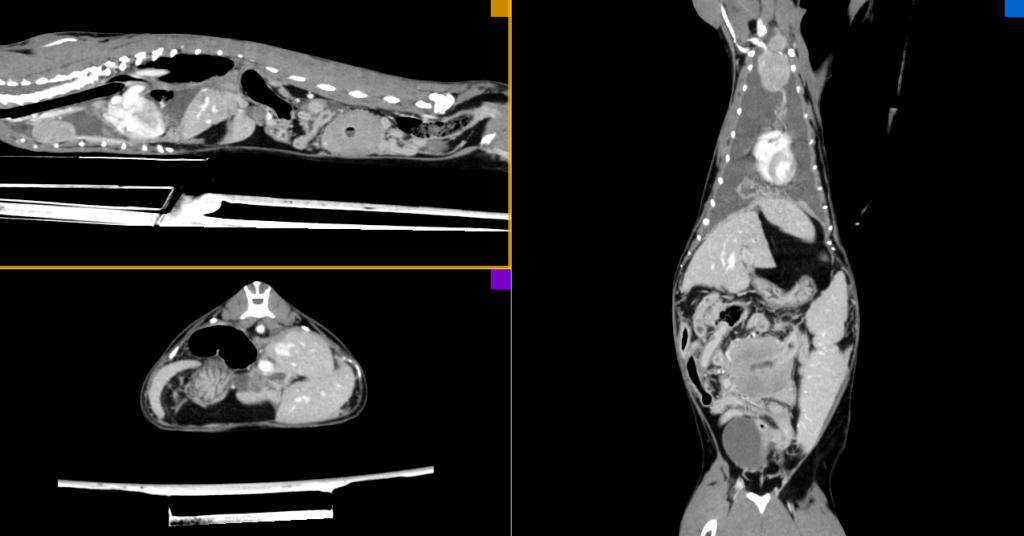
Неселективная КТ-ангиография (рис. 3) является одним из наиболее информативных методов диагностики опухолевых заболеваний у мелких домашних животных, она позволяет с высокой точностью определить зоны поражения, их анатомическое расположение, объем и связь с другими структурами организма пациента.
Описание результатов КТ. При проведении КТ у пациента было выявлено новообразование в краниальном средостении с иррегулярной формой и гетерогенной структурой, вовлекающее группу лимфатических узлов. На нативной серии плотность новообразования преимущественно изоденсивная, а его границы нечеткие.
После введения контрастного препарата отмечается его равномерное накопление преимущественно с гиперденсивной плотностью на контрастных и постконтрастных сериях. Границы между структурами лимфатических узлов остаются нечеткими, новообразование формирует единый конгломерат с ровными и гладкими краями. Значительные размеры новообразования (44,1 × 24,4 × 20,9мм) данного пациента привели к интимному прилежанию новообразования к легочному стволу и аорте. По данным КТ, также была обнаружена свободная жидкость в плевральной полости высотой до 25,2 мм с рентгенологической плотностью 13,9 HU.
Воздушность легких снижена, выявлены ателектазы краниальной доли левого легкого, вентральной части краниальной доли и средней доли правого легкого. Убедительных данных о наличии очагов патологической плотности, характерных для неопластического/метастатического поражения, не получено.
При исследовании брюшной полости методом неселективной ангиографии также была выявлена свободная жидкость высотой до 10 мм. Ткани сальника имеют признаки выраженного отека, печень выступает за край реберной дуги, сосудистый рисунок не обеднен, паренхима гомогенная. Отмечается выраженная гиперплазия мезентериальных лимфатических узлов, которая имеет схожие характеристики с лимфатическими узлами грудной полости.
Портальные лимфоузлы увеличены, имеют гетерогенную структуру и размеры 19,6 × 16,5 мм. Стенка кишечника утолщена до 3,9 мм, преимущественно в тонком отделе, активно накапливает контрастный препарат. Мезентериальные лимфоузлы увеличены, неоднородные по структуре, длина до 21,3 мм. В анатомическом расположении тощей кишки выявлено объемное новообразование (44,8 × 49,6 × 36,1 мм) с признаками сохранения просвета и толщиной стенки до 20 мм. Неопластический очаг имеет иррегулярную форму и гетерогенную массу, демонстрируя изоденсивную плотность на нативной серии и преимущественно гиперденсивную на постконтрастных сериях. Граница неопластического поражения на нативной серии нечеткая.
Заключение по результатам неселективной КТ-ангиографии:
- В проекции тощей кишки выявлены объемное образование (характерно для неопластического поражения, возможно, лимфомы), лимфаденопатия мезентериальных и портальных лимфоузлов (вероятнее всего, характерная для диффузного поражения), сопутствующие оментит и асцит.
- В краниальном средостении обнаружено объемное образование, что также характерно для неопластического поражения, наблюдаются гидроторакс и ателектаз долей легких.
- В краниальном полюсе левой доли щитовидной железы выявлено объемное образование, что может соответствовать неопластическому процессу.
Протокол лечения
В связи с наличием у пациента хронической болезни почек (IRIS II), высоким риском развития диспептического синдрома на фоне хронического панкреатита, холангиогепатита, а также возможным усугублением почечной недостаточности при использовании протокола COP в качестве альтернативы был предложен протокол с применением пегаспаргазы в дополнение к терапии кортикостероидами и ломустин, поскольку владельцы пациента отказались от противоопухолевой терапии по протоколу COP.Протокол лечения включал:
- перорально – ломустин (CCNU) – 70 мг/м2, преднизолон (начальная доза 2 мг/кг, с последующим снижением до 1 мг/кг в сутки);
- внутримышечно инъекции пегаспаргазы (Oncaspar®; Les Laboratoires Servier) – 500 МЕ/м2 (30–40 МЕ/кг). Препарат применялся в соответствии с рекомендациями производителя: порошок для инъекций разводился до концентрации 750 МЕ/мл и хранился при температуре 4 °C не более 14 дней для каждой последующей инъекции. Курс лечения состоял из 12 инъекций, вводимых на 0, 2, 4, 6, 8, 12, 15, 18, 22-й неделях.
В первый месяц терапии наблюдались признаки частичного ответа (PR), а на всех последующих циклах – признаки полного ответа (CR). Это сопровождалось хорошим качеством жизни питомца, и владельцы отказались от перехода на химиотерапию по протоколу COP, поэтому им было предложено продолжить терапию без ограничения по времени после 12-й инъекции пегаспаргазы (Oncaspar®; Les Laboratoires Servier).
В протокол лечения была включена пегаспаргаза спустя 10 дней после первого сеанса терапии ломустином.
Благоприятный ответ пациент получил после первого сеанса терапии ломустином в дозировке
70 мг/м2, которая проводилась на 1, 4, 7, 10, 13, 16-й неделях, и преднизолона в формате ежедневного применения.
Перед каждой процедурой дачи ломустина проводился общий клинический анализ крови, а также осуществлялся постоянный ультразвуковой контроль брюшной полости для мониторинга рецидива и при необходимости – в случае ухудшения аппетита или других нарушений общего состояния пациента. При появлении негативных реакций со стороны организма, связанных с противоопухолевой терапией, также осуществлялся ультразвуковой мониторинг и дополнительно проводился ОАК. Контрольное рентгенологическое исследование не проводилось. Спустя 6 месяцев после начала терапии (в состоянии клинической ремиссии и полного клинического ответа) было выполнено контрольное КТ-исследование.
Ответ на проведение противоопухолевого протокола:
- Использование преднизолона в дозе 1 мг/кг. Общее клиническое улучшение на протяжении 4 суток (с 20.01 по 24.01), последующая стабилизация. Статус: частичный ответ (PR).
- Использование ломустина (24.01) в дозе 70 мг/м2. Зафиксирована стабилизация состояния, а также положительная динамика по данным УЗИ. Статус: частичный ответ (PR).
- Использование пегаспаргазы (07.02) в дозе 40 мг/кг. Статус: стабилизация состояния и полная ремиссия (CR).
Осложнения. На фоне применения комбинированной терапии ломустином и пегаспаргазой у пациента с мультицентрической крупноклеточной лимфомой в начале лечения развились желудочно-кишечные расстройства, проявляющиеся кашицеобразным стулом, а также наблюдался единичный случай внепеченочного холестаза. Токсического воздействия на костный мозг не зарегистрировано.
УЗИ подтвердило наличие хронического панкреатита на фоне применения противоопухолевой терапии, но без ярко выраженной отрицательной динамики на всем протяжении лечения.
Дозировки применяемых препаратов не снижались, кратность применения не нарушалась.
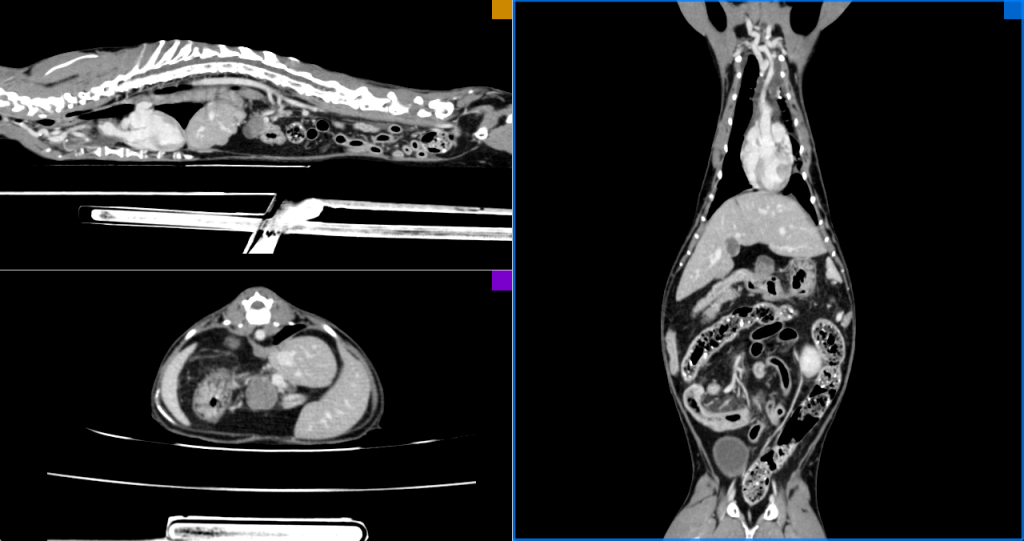
Спустя 6 месяцев с момента проведения компьютерной томографии в момент обращения была проведена контрольная неселективная КТ-ангиография (рис. 4).
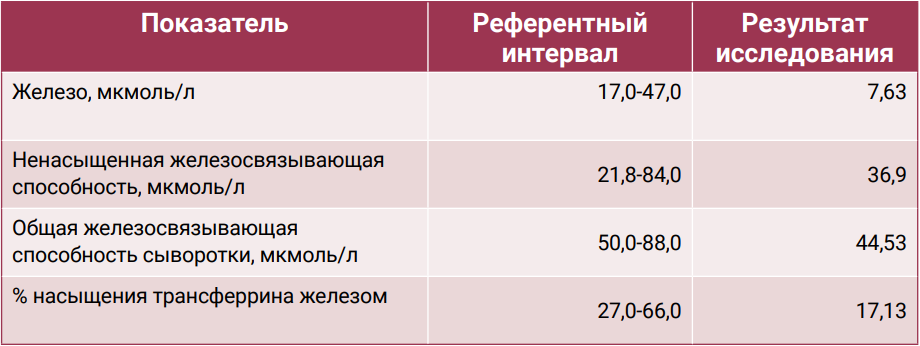
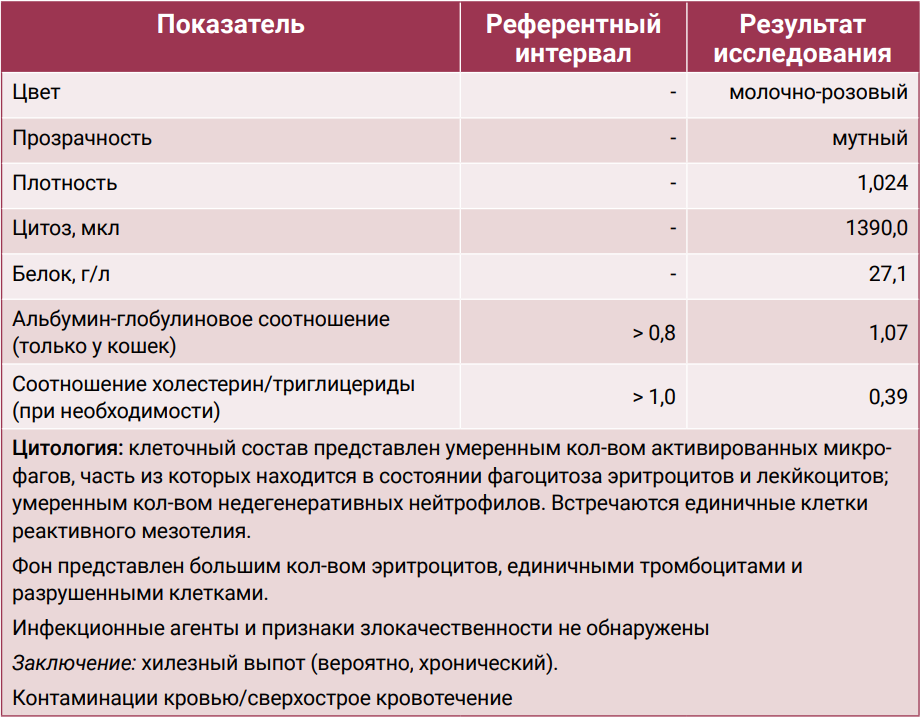
Исход. Смерть наступила на фоне обострения хронического панкреатита (табл. 5), прогрессирующей хронической болезни почек, железодефицитной анемии (табл. 6) и хилезного выпота в грудной (преимущественно; табл. 7) и брюшной полостях. Общее время выживания с момента постановки диагноза составило 180 дней.
Выводы
Пегилированная аспарагиназа остается редко применяемым препаратом в ветеринарной медицине, несмотря на ее эффективность в лечении лимфом и лейкозов у людей. Это обусловлено необходимостью частого введения (каждые 14 дней), высокой стоимостью и сложностями с приобретением препарата.На протяжении многих лет пегилированная аспарагиназа была ключевым компонентом успешной терапии пациентов с острым лимфобластным лейкозом (ОЛЛ) и некоторыми неходжкинскими лимфомами20,21,26-30. Многочисленные исследования демонстрируют, что значительная часть кошек с лимфомой высокой степени злокачественности могут достичь объективного ответа после однократной инъекции пегаспаргазы. В одном из таких исследований в популяции из 56 кошек с лимфомой у 82% пациентов был достигнут объективный ответ: 38% кошек получили полную клиническую ремиссию и 44% – частичную25. Эти результаты согласуются с данными Van Vliet M. и соавторов, где 12 кошек с лимфомой носовой полости получали лечение пегаспаргазой31. С клинической точки зрения все кошки в этом исследовании достигли полной ремиссии со средним временем 25 дней.
В некоторых исследованиях отмечено, что однократное применение пегилированной аспарагиназы может приводить к формированию положительного ответа 25. Однако важно иметь в виду, что у кошек полная ремиссия зачастую достигается только после многократного применения препарата в отличие от однократной инъекции31.
Для оценки ответа на схему применения пегилированной аспарагиназы, ломустина и преднизолона данному пациенту ежемесячно проводили УЗИ брюшной полости с целью мониторинга состояния опухолевых поражений, по результатам которого не определялось выраженной отрицательной динамики. Поскольку визуализация и эндоскопические методы не всегда применялись для повторной оценки, ремиссии были квалифицированы как клинические.
Выражаем благодарность владельцам данного пациента за предоставление пегаспаргазы на безвозмездной основе для 8 пациентов, нуждающихся в данном препарате.
Список использованной литературы:
- Dorn C. R., Taylor D. O., Frye F. L., et al. Survey of animal neoplasms in Alameda and Contra Costa Counties, California. I. Methodology and description of cases, J Natl Cancer Inst, 40: 295–305.
- Valli V. E., Jacobs R. M., Norris A., Couto C. G., Morrison W. B., et al. The histologic classification of 602 cases of feline lymphoproliferative disease using the National Cancer Institute working formulation. J Vet Diagn Invest, 12: 295–306, 2000.
- Louwerens M., London C. A., Pedersen N. C., et al. Feline lymphoma in the post-feline leukemia virus era. J Vet Intern Med, 19: 329–335, 2005.
- Collette S. A., Allstadt S. D., Chon E. M., et al. Treatment of feline intermediate-to high-grade lymphoma with a modified university of Wisconsin–Madison protocol: 119 cases (2004–2012). Vet Comp Oncol, 14 Suppl 1: 136–146, 2016.
- Simon D., Eberle N., Laacke-Singer L., et al. Combination chemotherapy in feline lymphoma: treatment outcome, tolerability, and duration in 23 cats. J Vet Intern Med, 22: 394–400, 2008.
- Mooney S. C., Hayes A. A., MacEwen E. G., et al. Treatment and prognostic factors in lymphoma in cats: 103 cases (1977–1981). J Am Vet Med Assoc, 194: 696–702, 1989.
- Zwahlen C. H, Lucroy M. D., Kraegel S. A., et al. Results of chemotherapy for cats with alimentary malignant lymphoma: 21 cases (1993–1997). J Am Vet Med Assoc, 213: 1144–1149, 1998.
- Vail D. M., Moore A. S., Ogilvie G. K., et al. Feline lymphoma (145 cases): proliferation indices, cluster of differentiation 3 immunoreactivity, and their association with prognosis in 90 cats. J Vet Intern Med, 12: 349–354, 1998.
- Waite A. H., Jackson K., Gregor T. P., et al. Lymphoma in cats treated with a weekly cyclophosphamide, vincristine and prednisone-based protocol: 114 cases (1998–2008). J Am Vet Med Assoc, 242: 1104–1109, 2013.
- Teske E., Van Lankveld A. J. and Rutteman G. R. Intraperitoneal antineoplastic drug delivery: experience with a cyclophosphamide, vincristine and prednisolone protocol in cats with malignant lymphoma. Vet Comp Oncol, 12: 37–46, 2014.
- Mahony O. M., Moore A. S., Cotter S. M., et al. Alimentary lymphoma in cats: 28 cases (1988–1993). J Am Vet Med Assoc, 207: 1593–1598, 1995.
- Jeglum K. A., Whereat A. and Young K. Chemotherapy of lymphoma in 75 cats. J Am Vet Med Assoc, 190: 174–178, 1987.
- Fabrizio F., Calam A. E., Dobson J. M., et al. Feline mediastinal lymphoma: a retrospective study of signalment, retroviral status, response to chemotherapy and prognostic indica-tors. J Feline Med Surg, 16: 637–644, 2014.
- Mortier F., Daminet S., Vandenabeele S., et al. Canine lymphoma: a retrospective study (2009–2010). Vlaams Diergeneeskd Tijdschr, 81: 341–351, 2012.
- Limmer S., Eberle N., Nerschbach V., et al. Treatment of feline lymphoma using a 12-week, maintenance free combination chemotherapy protocol in 26 cats. Vet Comp Oncol, 14 Suppl 1: 21–31, 2016.
- Meijster T., Fransman W., Veldhof R., et al. Exposure to antineoplastic drugs outside the hospital environment. Ann Occup Hyg, 50: 657–664, 2006.
- Smith A. N., Klahn S., Phillips B., et al. ACVIM small animal consensus statement on safe use of cytotoxic chemotherapeutics in veterinary practice. J Vet Intern Med, 32: 904–913, 2018.
- Chun R., Garrett L. and MacEwen E. G. Cancer chemotherapy. In: Withrow SJ and MacEwen EG (eds) Small animal clinical oncology. Philadelphia, PA: WB Saunders, pp 92–119, 2001.
- Connor T. H., MacKenzie B. A., De Bord D. G., et al. NIOSH list of antineoplastic and other hazardous drugs in healthcare settings. DHHS publication; no. (NIOSH) 2016–161, 2016. ссылка (2016, accessed 10 July 2022)
- Bade N. A., Lu C., Patzke C. L., et al. Optimizing pegylated asparaginase use: an institutional guideline for dosing, monitoring and management. J Oncol Pract, 26: 74–92, 2020.
- Geyer M. B., Ritchie E. K., Rao A. V., et al. Pediatric-inspired chemotherapy incorporating pegaspargase is safe and results in high rates of minimal residual disease negativity in adults up to age 60 with Philadelphia chromosome negative acute lymphoblastic leukemia. Haematologica, 106: 2086–2094, 2021.
- Graham M. L. Pegaspargase: a review of clinical studies. Adv Drug Deliv Rev, 26: 1293–1302, 2003.
- Teske E., Rutteman G. R., van Heerde P., et al. Polyethyleneglycol L-asparaginase versus native L-asparaginase in canine non-Hodgkin’s lymphoma. Eur J Cancer, 26: 891–895, 1990.
- Feenstra L. R., Gehring R., van Geijswijk I. M., et al. Evaluation of PEG-L-asparaginase in asparagine suppression and anti-drug antibody development in healthy Beagle dogs: a multiphase preclinical study. Vet J, 286, 2022. DOI: 10. 1016/j.tvjl.2022.105854.
- Krupa A., de Vos J., Van Eetvelde L., et al. Pegylated asparaginase in feline high-grade lymphoma: clinical results of single injection and continued incorporation into a modified COP regimen. J Feline Med Surg, 24: e203–e213, 2022.
- Keating M. J., Holmes R., Lerner S., et al. L-asparaginase and PEG asparaginase past, present, and future. Leuk Lymphoma, 10 Suppl: 153–157, 1993.
- Asselin B. L. The three asparaginases. Comparative pharmacology and optimal use in childhood leukemia. Adv Exp Med Biol, 457: 621–629, 1999.
- Tong W. H., Pieters R., Kaspers G. J., et al. A prospective study on drug monitoring of PEGasparaginase and Erwinia asparaginase and asparaginase antibodies in pediatric acute lymphoblastic leukemia. Blood, 123: 2026–2033, 2014.
- Asselin B. and Rizzari C. Asparaginase pharmacokinetics and implications of therapeutic drug monitoring. Leuk Lymphoma, 56: 2273–2280, 2015.
- Bender C., Maese L., Carter-Febres M., et al. Clinical utility of pegaspargase in children, adolescents and young adult patients with acute lymphoblastic leukemia: a review. Blood Lymphat Cancer, 11: 25–40, 2021.
- Van Vliet M. J., Roos A. and Tan J. Single-agent Peg-asparaginase as an alternative therapy for feline nasal lymphoma: twelve cases. Proceedings of the European Society of Veterinary Oncology Congress, May 28–30, p. 59, 2015; Krakow, Poland. Newark, NJ: Nightingale Press.
- Abbo A. H., Lucroy M. D. Assessment of anemia as an independent predictor of response to chemotherapy and survival in dogs with lymphoma, J Am Vet Med Assoc, 231: 1836–1842, 2007.
- Miller A. G., Morley P. S., Rao S., et al.: Anemia is associated with decreased survival time in dogs with lymphoma, J Vet Intern Med, 23:116–122, 2009.
- Haney S. M., Beaver L., Turrel J., et al. Survival analysis of 97 cats with nasal lymphoma: a multi-institutional retrospective study (1986–2006), J Vet Intern Med, 23:287–294, 2009.



 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург