г. Санкт-Петербург.
Серомашенко А. А., ветеринарный врач-онколог, хирург, ветеринарная клиника «ТрастВет»,
г. Санкт-Петербург.
Этиология
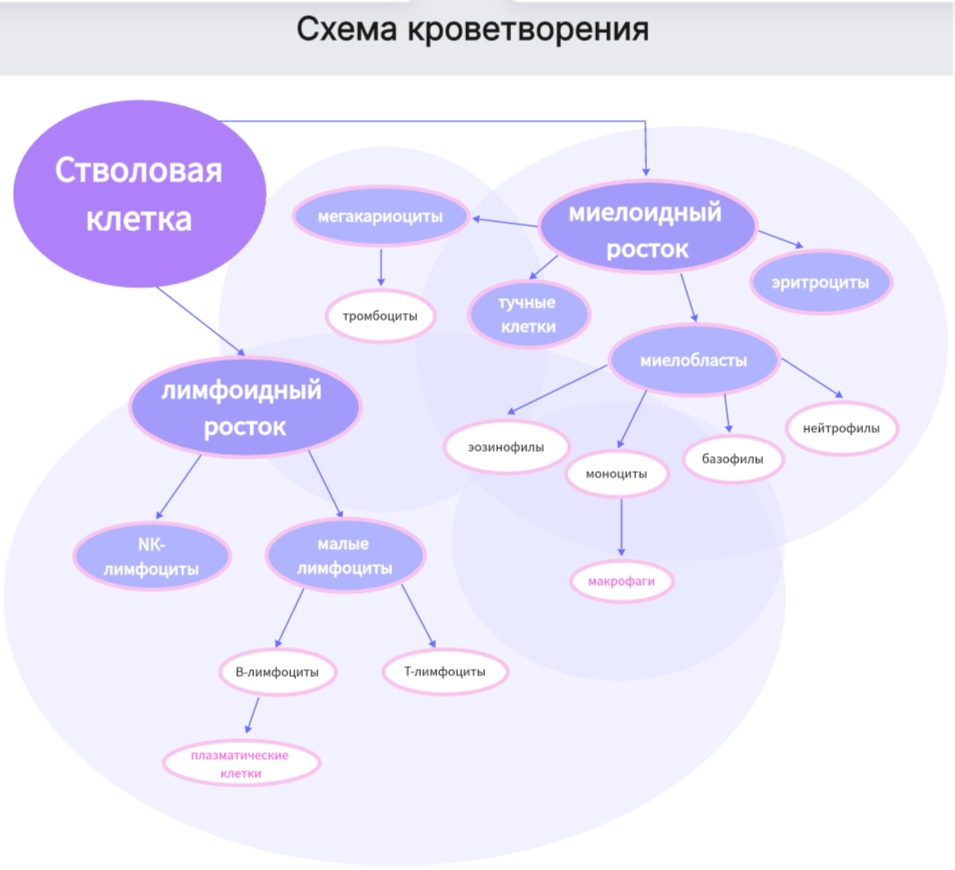
Миелопролиферативные заболевания (МПЗ) – группа неоплазий костного мозга, вызванных клональной трансформацией гемопоэтических стволовых клеток, которая приводит к избыточной пролиферации одной или нескольких клеточных линий крови и нарушению их созревания19,43,46.Кроветворение – это процесс пролиферации, дифференцировки и созревания стволовых клеток в терминально дифференцированные клетки крови6. Плюрипотентные стволовые клетки дифференцируются в общую лимфоидную или общую миелоидную прогениторные линии. Эти линии, в свою очередь, формируют различные типы клеток крови, включая эритроциты, гранулоциты, моноциты и тромбоциты, под воздействием факторов роста, таких как эритропоэтин и колониестимулирующие факторы52.
При эритропоэзе первой клеткой является проэритробласт, образующийся из эритроцитарной колониеобразующей клетки (КОК-Э), затем последовательно образуются эритробласт, ретикулоцит и зрелый эритроцит, жизненный цикл которого составляет около 120 дней43. Гранулоцитопоэз проходит через стадии промиелоцита, содержащего азурофильные гранулы, затем миелоцита, метамиелоцита, палочкоядерного и зрелого гранулоцита. Тромбоциты образуются в результате процесса частичной фрагментации цитоплазмы гигантских клеток костного мозга – мегакариоцитов. В результате созревания образуются окончательно дифференцированные клетки крови, поступающие в кровоток: эритроциты, гранулоциты, моноциты и тромбоциты13,27. Упрощенная схема кроветворения представлена на рис. 1.
МПЗ у собак встречаются значительно реже, чем у кошек, и у обоих видов животных они возникают реже, чем лимфопролиферативные злокачественные новообразования. Большинство животных с МПЗ – собаки крупных пород и кошки в возрасте от 7 до 8 лет, хотя острый миелоидный лейкоз может развиваться у собак и кошек в раннем возрасте19.
Классификация и патогенез
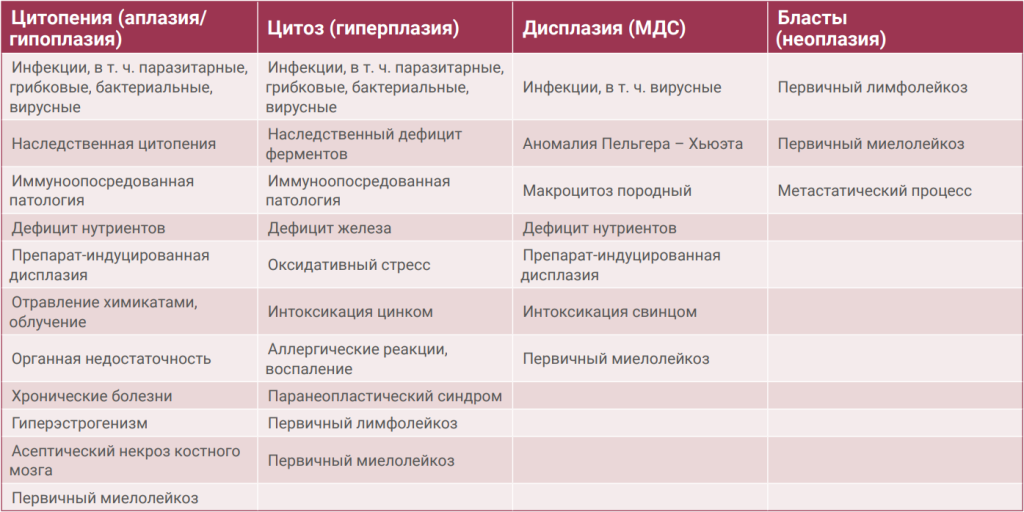
Регуляция процесса кроветворения – сложнейшая, генетически обусловленная система. Любые нарушения этого процесса быстро приводят к отклонениям от нормального состава крови и развитию заболеваний37.Клональные нарушения в костном мозге включают 29,46,61:
- миелоаплазию (низкое количество всех линий клеток крови, таких как эритроциты, лейкоциты и тромбоциты);
- миелодисплазию (миелодиспластический синдром [МДС] – группа заболеваний, при которых костный мозг не функционирует должным образом и производит недостаточное количество кровяных телец);
- МДС с рефрактерной цитопенией (менее 6% миелобластов);
- МДС с сидеробластной дифференцировкой;
- МДС с избытком миелобластов (6–200% миелобластов);
- миелопролиферацию (заболевание системы крови, при котором в костном мозге вырабатывается слишком много клеток крови определенного типа).
В основе патогенеза болезней системы крови лежат внешние (физические, химические, инфекционные и др.) и внутренние (гормональные, метаболические, врожденные, наследственные и др.) факторы. В целом ряде заболеваний системы крови причины этих нарушений пока не установлены52.
Апластическая панцитопения (апластическая анемия) – это заболевание, при котором нарушаются пролиферация и дифференцировка стволовых клеток крови вследствие их апоптоза под действием повреждающих факторов55. Разрушение стволовых клеток/клеток-предшественников, вызванное инфекционными агентами (например, Ehrlichia sp., парвовирус, FeLV), лекарственными средствами (сульфадиазин, НПВС, цефалоспорин, альбендазол, транквилизаторы, гризеофульвин и др.; у кошек основную опасность представляют сульфадиазин, альбендазол и гризеофульвин), токсинами, эстрогеном. Ионизирующая радиация является еще одной причиной разрушения гемопоэтических клеток13. Из-за сравнительно короткого периода полураспада нейтрофилов (4–8 часов) и тромбоцитов (5–7 дней) в крови по сравнению с эритроцитами (120 дней у собак и 55 дней у кошек) первоначально это приводит к нейтропении и тромбоцитопении52. Неэффективный эритропоэз, гранулоцитопоэз и мегакариоцитопоэз – термины, применяемые к ситуации, когда имеется гиперплазия клеточной линии в костном мозге, но сохраняется соответствующая цитопения в крови без признаков причины периферических потерь. На основе этих данных можно сделать вывод о том, что интрамедуллярная гибель клеток-предшественников, как правило, обусловлена апоптозом. Наиболее распространенной причиной является иммуноопосредованное разрушение этих клеток. Такая анемия часто носит обратимый характер13,44. В результате костный мозг становится гипоклеточным и замещается жировой тканью. Это отличает апластическую анемию от миелодиспластического синдрома, при котором, несмотря на уменьшение числа клеток в периферической крови, костный мозг демонстрирует гиперклеточность2.
Более чем у половины пациентов не удается выявить конкретные причинные факторы – это так называемая идиопатическая апластическая анемия. Диагноз «идиопатическая апластическая панцитопения» может быть поставлен только в том случае, если процесс соответствует следующим критериям8,13:
- сохраняется не менее 2 недель;
- сохраняется после лечения сепсиса или эндотоксемии;
- отсутствие контакта с лекарственными средствами в течение 4 недель до постановки диагноза;
- исключена ХБП;
- исключены состояния, ассоциированные с гиперэстрогенизмом;
- отрицательные результаты серологических тестов на эрлихии, бабезии, риккетсии и лейшмании;
- выявление при биопсии красного костного мозга замещения жировой тканью.
МДС может быть первичным или вторичным49,51. Первичный МДС представляет собой необратимые нарушения развития стволовых клеток костного мозга, не связанные с сопутствующим заболеванием, недостаточностью питания или лекарственным токсикозом, и, вероятно, является результатом генетических изменений в гемопоэтических стволовых клетках, которые обеспечивают преимущество роста и приводят к клональному кроветворению. Возникает в результате клональной экспансии дефектных плюрипотентных стволовых клеток. Сопутствующий неэффективный гемопоэз является результатом сложного взаимодействия дефектных клеток-предшественников и гемопоэтического микроокружения49. Это приводит к увеличению скорости апоптоза.
Вторичный МДС классифицируется по сопутствующим заболеваниям, воздействию лекарств или токсинов, а также по диспластическим признакам49. Диспластические проявления у собак с вторичным МДС характеризовались значительным разнообразием и включали нарушения гранулопоэза, эритропоэза или тромбопоэза, а также их комбинации. Во всех зарегистрированных случаях вторичного МДС у собак уровень миелобластов в костном мозге не превышал 5%49.
Поскольку первичный и вторичный МДС невозможно четко дифференцировать цитологически, рекомендуется искать вторичные причины МДС, а диагноз «первичный МДС» следует ставить только после исключения иммуноопосредованных, неопластических и лекарственно/токсин-ассоциированных причин МДС49. Вторичный МДС у собак может быть вызван злокачественной лимфомой, миелофиброзом, иммуноопосредованной тромбоцитопенией, иммуноопосредованной гемолитической анемией, множественной миеломой, ионизирующей радиацией и приемом лекарств. У кошек МДС может быть связан с вирусом лейкоза кошек (FeLV)49.
Минимальные диагностические критерии МДС 52:
- персистирующая цитопения без другой очевидной причины (лекарства, питание, кровопотеря);
- увеличенное количество миелобластов (5–19%);
- выраженная дисплазия (> 10% клеток в одном ростке костного мозга: эритроидном, гранулоцитарном, мегакариоцитарном).
Миелопролиферативные заболевания
Миелофиброз – это хроническое миелопролиферативное заболевание, при котором происходит активация мегакариоцитов, выделяющих фиброгенные цитокины. Это приводит к фиброзу костного мозга и развитию экстрамедуллярного гемопоэза в печени и селезенке.Миелофиброз может быть первичным (идиопатическим) или вторичным по отношению к МПЗ (например, полицитемия вера и эссенциальная тромбоцитемия)33, а также возникающим вследствие лучевого, токсического воздействия (например, при приеме эстрогенов, цефалоспоринов) или врожденной гемолитической анемии40. В ряде случаев заболевание развивается на фоне инфекционных процессов, таких как эрлихиоз и сепсис. Существует предположение, что фибробласты пролиферируют в ответ на высвобождение медиаторов воспаления, связанных с некротическими процессами. В некоторых случаях этиология заболевания остается неизвестной (идиопатический миелофиброз)40,50.
Эссенциальная тромбоцитемия характеризуется мутациями в генах JAK2, CALR и MPL, которые активируют сигнальные пути, способствующие пролиферации мегакариоцитов и избыточному образованию тромбоцитов2,26. Несмотря на значительное увеличение количества тромбоцитов, они могут быть функционально неполноценными, что повышает риск развития как тромбозов, так и кровотечений42.
У людей эссенциальная тромбоцитемия, или первичный тромбоцитоз, характеризуется постоянным превышением тромбоцитов до уровня не менее 600 000/мкл. При этом в крови отсутствуют бластные клетки, а мегакариоциты имеют выраженные морфологические признаки28. В костном мозге наблюдается гиперплазия мегакариоцитарного ростка без признаков миелофиброза.
Для постановки диагноза необходимо исключить другие МПЗ, особенно полицитемию и состояния, сопровождающиеся реактивным тромбоцитозом, включая воспаление, гемолитическую анемию, железодефицитную анемию, злокачественные новообразования, восстановление после тяжелого кровотечения, последствия иммуноопосредованной тромбоцитопении и спленэктомии19,24. Кроме того, некоторые лекарственные препараты, например винкристин, могут индуцировать тромбоцитоз41. В литературе упомянуты случаи тромбоцитемии у собак, чаще всего сопровождавшиеся базофилией, кровотечением, отсутствием бластов в периферической крови. У одной из собак была зарегистрирована трансформация в хронический миелоидный лейкоз (ХМЛ)22.
Базофильный и эозинофильный лейкозы – редкие формы хронических миелоидных неоплазий, характеризующиеся массивной пролиферацией соответствующих лейкоцитарных линий.
При базофильном лейкозе избыток базофилов приводит к выбросу гистамина и цитокинов, вызывая зуд, гипотонию и инфильтрацию органов23. В ветеринарии было зарегистрировано восемь случаев базофильного лейкоза у собак, все они были хронического типа3. Кроме того, зарегистрировано по одному случаю базофильного лейкоза у кошек и лошадей, которые характеризовались острым течением1. Все случаи у животных рассматриваются как первичные, случаев вторичного заболевания не зарегистрировано.
Эозинофильный лейкоз сопровождается тканевым повреждением, что проявляется в таких заболеваниях, как миокардит и легочный фиброз16. Зарегистрированные случаи эозинофильного лейкоза были ассоциированы с высоким количеством эозинофилов в крови и инфильтрацией эозинофилами органов15. Явные различия между неопластической пролиферацией эозинофилов и идиопатическим гиперэозинофильным синдромом остаются неизвестными. Однако современные методы молекулярной диагностики (например, PARR и анализ мутаций) позволяют отличать реактивную (поликлональную) эозинофилию от неопластической (моноклональной)16.
Важно исключать заболевания, не относящиеся к МПЗ, но сопровождающиеся эозинофилией, такие как паразитарные инфекции, кожные заболевания, заболевания дыхательных путей и желудочно-кишечного тракта, лимфомы, эозинофильные гранулемы, тучноклеточные опухоли и другие новообразования. В частности, у кошек эозинофилия была зарегистрирована при переходноклеточной карциноме, а у собак – при фибросаркоме полости рта и лейомиосаркоме перикарда.
Хронический моноцитарный лейкоз – это заболевание из группы миеломоноцитарных неоплазий, характеризующееся стойким моноцитозом более 1 × 109/л и признаками клеточной дисплазии. Заболевание может сопровождаться спленомегалией, цитопенией и воспалительным синдромом.
В описанном случае моноцитарного лейкоза 2-летняя стерилизованная домашняя короткошерстная кошка поступила в ветеринарную клинику с жалобами владельцев на анорексию и апатию, наблюдаемые в течение одной недели. При физикальном осмотре животное проявляло признаки вялости и лихорадки. Также были выявлены спленомегалия, анизокория и язвенный стоматит. Результаты лабораторных исследований крови показали наличие лейкоцитоза, значительного количества бластных клеток в периферической крови, тромбоцитопении, гиперглобулинемии и положительного результата теста на антиген вируса лейкоза кошек (FeLV). На основании результатов цитологического анализа, гистопатологии и иммунохимических исследований костного мозга (с использованием маркеров CD3, CD79a, лизоцима и миелопероксидазы) был поставлен диагноз «острый миеломоноцитарный лейкоз». После неожиданного периода клинической и клинико-патологической ремиссии, продолжавшегося в течение месяца без проведения химиотерапии, у кошки произошел рецидив, и спустя неделю она умерла25.
Хронический миелолейкоз (ХМЛ) – заболевание, обусловленное транслокацией t (9; 22) (q34; q11), приводящей к образованию гена BCR-ABL1, кодирующего аномальную тирозинкиназу с конститутивной активностью. Это вызывает неконтролируемую пролиферацию гранулоцитарного ряда9,46. ХМЛ имеет фазное течение: хроническую фазу, фазу акселерации и бластный криз20.
В описанных случаях хронического миелогенного лейкоза наблюдались лейкоцитоз, зрелая нейтрофилия, эозинофилия и базофилия. При аспирации костного мозга выявлялись гиперклеточность с пролиферацией клеток миелоидного ряда. Другие причины, способные вызывать лейкоцитоз, отсутствовали34. Описан случай ХМЛ у семилетнего кота, который из-за отсутствия клинических признаков заболевания находился только под наблюдением (без лечения) в течение 7 месяцев после постановки диагноза. Впоследствии у животного появились зудящие поражения кожи, которые удавалось успешно контролировать с помощью перорального введения преднизолона. Через 42 месяца после постановки диагноза у животного развилась лимфома носа, которую успешно лечили с помощью лучевой терапии, что привело к полной ремиссии. Кот продолжал находиться в хорошем физическом состоянии спустя 63 месяца после первоначальной постановки диагноза, несмотря на сохранение выраженной нейтрофилии, эозинофилии и базофилии34.
Истинная полицитемия (polycythemia vera). Первичный эритроцитоз, или истинная полицитемия, представляет собой МПЗ, вызванное чрезмерным увеличением количества клеток-предшественников эритроидного ростка в костном мозге36.
Термин «полицитемия» подразумевает повышение всех показателей крови, возникновение лейкоцитоза и тромбоцитоза наряду с эритроцитозом, однако у животных-компаньонов это происходит исключительно редко. Следовательно, полицитемию правильнее было бы называть эритроцитозом, и клинически она означает увеличение количества эритроцитов в крови выше нормы11. У полицитемических животных клинические признаки не проявляются до тех пор, пока гематокрит не достигнет > 60%, причем некоторые из самых высоких зарегистрированных значений превышают 85%. Из-за недооценки нормального верхнего предела гематокрита у кошек (48%) по сравнению с собаками (56%) полицитемия у кошек обычно не диагностируется35,36. В зависимости от объема крови и массы эритроцитов полицитемию можно разделить на относительную и абсолютную, которые представляют собой совершенно разные состояния, требующие немедленных, но противоположных терапевтических вмешательств47. Относительная полицитемия характеризуется повышенным гематокритом при нормальной (или даже сниженной) общей массе эритроцитов. Обычно это происходит из-за уменьшения объема плазмы, связанного с тяжелым обезвоживанием или увеличением общего количества белков в сыворотке (например, сильная рвота и диарея или тяжелые ожоги)31,32. Гематокрит, как правило, повышен незначительно, поэтому относительная полицитемия редко сочетается с признаками гипервязкости. Из-за очевидных признаков обезвоживания относительная полицитемия обычно легко распознается и корректируется агрессивной инфузионной терапией. Абсолютная, или истинная, полицитемия характеризуется увеличением массы эритроцитов32. Дифференциация первичной и вторичной абсолютной полицитемии более сложная и зависит от того, является ли данное состояние эритропоэтин-независимым или зависимым47.
Клинические признаки
МПЗ характеризуется медленным прогрессирование, часто бессимптомным, постепенным миелофтизом и нередко заканчивается бластным кризом12.У собак и кошек с миелоидными неоплазиями развиваются схожие клинические признаки: снижение активности, непереносимость физических нагрузок, летаргия, анемичность слизистых оболочек, анорексия (полная или частичная), снижение массы тела, кахексия, персистирующая лихорадка, шумы в сердце, связанные с анемией, наличие петехий, гепатоспленомегалия и (реже) лимфаденопатия, цитопения/полицитемия, биохимические изменения при инфильтрации органов (могут возникать лишь при заметной инфильтрации внутренних органов, а в большинстве случаев показатели остаются в пределах референтных значений)12,39. Также могут отмечаться перемежающаяся хромота, поражение глаз и рецидивирующие инфекции. Рвота, диарея, одышка и неврологические расстройства встречаются относительно редко и более характерны для собак52.
Диагностика
Подход к диагностике МПЗ всегда комплексный и включает обзорную рентгенографию органов грудной полости, ультразвуковое исследование органов брюшной полости, биохимическое и клиническое исследования периферической крови с определением уровня бластных клеток (цитология), биопсию костного мозга14,52.Во всех случаях миелоидных новообразований диагноз ставится на основании результатов исследования периферической крови и костного мозга. У кошек также необходимо проводить диагностику хронических инфекционных заболеваний (FIP, FIV, FeLV) как в периферической крови, так и в костном мозге39.
Цитология костного мозга может обеспечить самую быструю оценку морфологии клеток, однако этот метод не позволяет поставить точный диагноз. Для его уточнения применяются гистологическое исследование и иммунофенотипирование. Биопсия костного мозга позволяет выявить воспалительные процессы, неоплазии, некроз, остеолизис, а также миелофиброз49,52.
Гистологическое исследование мазков, полученных из лимфатических узлов, селезенки или печени, позволяет выявить опухолевые клетки, однако данный метод обладает ограниченной диагностической чувствительностью. Для уточнения клеточного происхождения применяются методы окраски бластов стандартными красителями Романовского. При миеломоноцитарном лейкозе ядра бластов демонстрируют плеоморфность и имеют форму от округлой до дольчатой. Для мегакариоцитарного лейкоза характерно наличие вакуолей и цитоплазматических пузырьков в бластах. Также могут наблюдаться нетипичные макротромбоциты52.
Трепанобиопсию для гистологического исследования следует проводить из следующих костных структур: проксимальная плечевая кость (после закрытия эпифизарной пластинки роста), проксимальный отдел бедренной кости и гребень подвздошной кости. Для выполнения данной процедуры применяются иглы Klima или Jamshidi. Полученный материал для гистологического исследования помещают в 10%-ный забуференный раствор формалина. При необходимости проведения дополнительных ПЦР-исследований образец фиксируется в 70%-ном растворе спирта или 0,9%-ном растворе натрия хлорида52.
Для окончательного определения происхождения бластов обычно требуется проведение иммунофенотипирования, которое проводится методом проточной цитометрии, также этот метод может быть выполнен на цитологических или гистологических препаратах15. Интерпретация результатов иммунофенотипирования должна осуществляться в комплексе с данными гематологических исследований, анализа костного мозга и морфологических характеристик изучаемых клеток52.
К сожалению, в ветеринарной медицине нет генетических маркеров, которые характеризуют многие типы МПЗ у пациентов, поэтому мы используем морфологические признаки и иммунофенотипирование.
Дифференциальные диагнозы19: острый лимфобластный лейкоз (ОЛЛ), лимфомы, иммуноопосредованные анемии и тромбоцитопении, гемолиз, инфекционные заболевания (ВЛК, эрлихиоз, парвовирусные инфекции).
Лечение
Стандартного режима лечения МПЗ не существует.В медицине человека часто люди не получают лечения, если данные патологии не вызывают клинических признаков. Трансфузии крови и кровепродуктов проводятся по показаниям. Пациенты с лихорадкой подвергаются тщательной диагностике с целью исключения инфекций, аутоиммунных заболеваний и лейкемии43,60.
Гидроксимочевина является наиболее эффективным средством лечения ХМЛ, а также препаратом выбора для первоначального контроля тромбоцитоза14,38,54,59. Другие цитостатики используются как по отдельности, так и в комбинации, например, при эссенциальной тромбоцитемии одна собака была успешно вылечена по протоколу комбинированной химиотерапии, который включал винкристин, цитарабин, циклофосфамид и преднизолон25,57.
Ингибиторы ангиогенеза используются при лечении МПЗ, ХМЛ и ОМЛ. Применение основано на исследованиях, подтверждающих, что опухоли секретируют ангиогенные факторы, такие как фактор роста эндотелия сосудов (VEGF), тем самым увеличивая плотность микрососудов30. Незрелые миелоидные клетки при МДС продуцируют большое количество VEGF, а также имеют рецепторы VEGF. Следовательно, VEGF может вызывать не только неоваскуляризацию, но и аутокринную стимуляцию миелоидных клонов. Внутриклеточная передача сигнала после лигирования рецептора VEGF, а также множества других гемопоэтических факторов роста опосредуется активацией рецепторных тирозинкиназ. Введение низкомолекулярных ингибиторов рецепторов тирозинкиназ вызывало ремиссию у пациентов с ОМЛ17. Талидомид также является антиангиогенным средством10,38. В одном исследовании примерно у 30% пациентов улучшилось производство эритроцитов после 12 недель лечения талидомидом, однако улучшение количества гранулоцитов и тромбоцитов наблюдалось реже36. В настоящее время документально подтверждено, что часть ХМЛ у собак ассоциирована с определенной хромосомной аномалией BCR-ABL, которая аналогична транслокации «филадельфийской хромосомы», ответственной за подавляющее большинство ХМЛ у людей7. Известно, что иматиниб – ингибитор тирозинкиназы – эффективен для лечения ХМЛ у людей. Для животных с ХМЛ эти типы лекарств также могут обладать аналогичной активностью 14. Одна собака с хроническим моноцитарным лейкозом при лечении тоцеранибом и преднизолоном достигла клинической ремиссии (до развития прогрессирующего заболевания)38.
Основные препараты для лечения МПЗ 14,38,48,54:
- цитарабин 0,7–1,4 мг/кг/сут, п/к, 2–4 недели либо 100–200 мг/м2/сут, в/в или п/к, 4 дня, каждые 3 недели;
- преднизолон 2–4 мг/кг/сут, п/о, в/м или в/в, длительно;
- циклофосфамид 50 мг/м2, п/о, 4 дня в неделю, длительно;
- гидроксимочевина 30 мг/кг/сут, п/о;
- хлорамбуцил 2–8 мг/м2/сут, п/о, длительно;
- ингибиторы ангиогенеза.
Варианты в гуманной медицине 4,36,38,48:
- ингибиторы ангиогенеза (ранибизумаб, леналидомид);
- ингибиторы топоизомеразы (иринотекан, доксорубицин, этопозид);
- ингибиторы гистондеацетилазы (азацитидин, децитабин);
- ингибиторы ДНК-метилтрансферазы (5-азацитидин, децитабин);
- талидомид;
- триоксид мышьяка;
- гематологические факторы роста;
- трансплантация костного мозга.
Вспомогательное лечение 14,25,48,60:
- гемотрансфузия;
- флеботомия;
- антибиотики широкого спектра действия;
- дарбэпоэтин альфа, начальная доза 1 мкг/кг, п/к, 1 раз в 7 дней;
- филграстим 100–500 тыс. ед/кг 1 раз в сутки;
- ромиплостим 3–5 мкг/кг пк 1 раз в 7 дней, дозы описаны только для собак;
- циклоспорин А 2,5–5 мг/кг;
- интерферон-α (в качестве модификатора биологического ответа для кошек, инфицированных FeLV).
Прогнозы
Прогноз при МПЗ всегда осторожный и зависит в основном от патогенетического варианта течения данной патологии, а также от наличия или отсутствия тяжелых симптомов и сопутствующих заболеваний52. Главными параметрами в оценке прогноза являются уровень бластных клеток в костном мозге и выраженность цитопении45. Также прогнозы зависят от характера заболевания, степени тяжести клинических проявлений, ответа на терапию, скорости трансформации в лейкоз и сопутствующих заболеваний. Большинство пациентов живут от нескольких месяцев до нескольких лет54.Список литературы:
- Alroy J. Basophilic leukemia in a dog // Vet Pathol. 1972;9(2):90-5. doi: 10.1177/030098587200900201. PMID: 4526497.
- Arber D. A., Orazi A., Hasserjian R. et al. The 2016 revision to the WHO classification of myeloid neoplasms and acute leukemia // Blood. — 2016. — Vol. 127, № 20. — Pp. 2391–2405.
- Azakami D. et al. Chronic basophilic leukaemia in a dog // Journal of Comparative Pathology. — 2019. — Vol. 166. — P. 5–8. DOI: 10.1016/j.jcpa.2018.10.170
- Barbui T., et al. Philadelphianegative classical myeloproliferative neoplasms: critical concepts and management recommendations from European LeukemiaNet // J Clin Oncol. 2011 Feb 20; 29(6):761-70.
- Bejar R. Prognostic models in myelodysplastic syndromes. Hematology Am Soc Hematol Educ Program. 2013; 2013:504-10. doi: 10.1182/asheducation-2013.1.504. PMID: 24319225.
- Birbrair A, Frenette PS. Niche heterogeneity in the bone marrow. Ann N Y Acad Sci. 2016 Apr;1370(1):82-96. doi: 10.1111/nyas.13016. Epub 2016 Mar 25. PMID: 27015419; PMCID: PMC4938003.
- Bonkobara M. Dysregulation of tyrosine kinases and use of imatinib in small animal practice // Veterinary Journal. — 2015. — Vol. 205, № 2. — Pp. 180–188. DOI: 10.1016/j.tvjl.2014.12.015
- Camitta B. M., et al. Severe aplastic anemia: a prospective study of the effect of early marrow transplantation on acute mortality // Blood. — 1976. — Vol. 48, № 1. — Pp. 63–70.
- Deininger M. W., Goldman J. M., Melo J. V. The molecular biology of chronic myeloid leukemia // Blood. — 2000. — Vol. 96, № 10. — Pp. 3343–3356.
- Dredge K. et al. Novel thalidomide analogues display anti-angiogenic activity independently of immunomodulatory effects. Br J Cancer. 2002 Nov 4;87(10):1166-72. doi: 10.1038/sj.bjc.6600607. PMID: 12402158; PMCID: PMC2376196.
- eClinPath. Erythrocytosis (Cornell University laboratory resource). — 2022.
- Evans R. J, Gorman N. T. Myeloproliferative disease in the dog and cat: definition, aetiology and classification // Veterinary Record. — 1987. — Vol. 121, № 19. — Pp. 437–443. — DOI: 10.1136/vr.121.19.437.
- Feldman B. F., Zinkl J. G., Jain N. C. Schalm’s Veterinary Hematology. 5th ed. — Lippincott Williams & Wilkins; 2000.
- Gardner H. L., Fenger J. M., London C. A. Dogs as a model for cancer // Annual Review of Animal Biosciences. — 2016. — Vol. 4. — Pp. 199–222. DOI:10.1146/annurev-animal-022114-110911
- Gelain M. E. et al. Chronic eosinophilic leukemia in a cat: cytochemical and immunophenotypical features // Veterinary Clinical Pathology. — 2006. — Vol. 35. — Pp. 454–459.
- Gotlib J., Shomali W. World Health Organization-defined eosinophilic disorders: 2022 update on diagnosis, risk stratification, and management. Am J Hematol. 2022 Jan 1;97(1):129-148. doi: 10.1002/ajh.26352. Epub 2021 Oct 8. PMID: 34533850.
- Gupta P. et al. A phase II study of the oral VEGF receptor tyrosine kinase inhibitor vatalanib in myelodysplastic syndrome: Cancer and Leukemia Group B Study 10105 // Investigational New Drugs. — 2013. — Vol. 31, № 6. — Pp. 1311–1320. DOI:10.1007/s10637-013-9978-z
- Haferlach T., et al. Genetic classification of acute myeloid leukemia (AML). Ann Hematol. 2004;83 Suppl 1:S97-100. doi: 10.1007/s00277-004-0850-2. PMID: 15124693.
- Harvey J. W. Myeloproliferative disorders in dogs and cats // Veterinary Clinics of North America: Small Animal Practice. — 1981. — Vol. 11, № 2. — Pp. 349–381. — DOI: 10.1016/S0195-5616(81)50034-9.
- Hehlmann R., Hochhaus A., Baccarani M. Chronic myeloid leukemia // Lancet. — 2007. — Vol. 370, № 9584. — Pp. 342–350.
- Hoffman R., et al. Hematology: Basic Principles and Practice. 7th ed. — Elsevier; 2017. http://doi.org/10.1016/C2013-0-23355-9.
- Hopper P. E., et al. Probable essential thrombocythemia in a dog // Journal of Veterinary Internal Medicine. — 1989. — Vol. 3, № 2. — Pp. 79–85.
- Horny HP, Sotlar K, Valent P, Hartmann K. Mastocytosis: a disease of the hematopoietic stem cell. Dtsch Arztebl Int. 2008 Oct;105(40):686-92. doi: 10.3238/arztebl.2008.0686. Epub 2008 Oct 3. PMID: 19623287; PMCID: PMC2696962.
- Hoskins J. D. Increased number of platelets call for review of thrombocytosis // Compendium on Continuing Education for the Practicing Veterinarian. — 2002. — May; № 5.
- Shimoda T., Tanabe M., Shoji Y., Kanda T., et al. Monoblastic leukemia (M5a) with chronic basophilic leukemia in a cat // J. Vet. Med. Sci. – Vol. 84. – 2022. – 251–256 pp.
- Klampfl T., Gisslinger H., Harutyunyan A. S. et al. Somatic mutations of calreticulin in myeloproliferative neoplasms // New England Journal of Medicine. — 2013. — Vol. 369, № 25. — Pp. 2379–2390.
- Kuter DJ. The biology of thrombopoietin and thrombopoietin receptor agonists. Int J Hematol. 2013 Jul;98(1):10-23. doi: 10.1007/s12185-013-1382-0. Epub 2013 Jul 3. PMID: 23821332.
- Leukemia & Lymphoma Society. Essential thrombocythemia facts // Mortality & morbidity data. — 2022.
- McManus P. M. Classification of myeloid neoplasms: a comparative review // Veterinary Clinical Pathology. — 2005. — Vol. 34, № 3. — Pp. 189–212.
- Medinger M., Mross K. Clinical trials with antiangiogenic agents in hematological malignancies // Vascular Cell. — 2010. — Vol. 2. — Article 10. DOI: 10.1186/2040-2384-2-10.
- Elizabeth Flaherty, Lisa M. Pohlman. Top 5 Causes of Erythrocytosis in Dogs & Cats. 2022
- S.N. Yadav, N. Ahmed, A.J. Nath, P.K. Boro. Erythrocyte Parameters as a Diagnostic Tool in Canine Medicine: A Review.2021.
- Mesa R. A., Verstovsek S., Cervantes F. et al. Primary myelofibrosis (PMF), post-polycythemia vera MF, and post-essential thrombocythemia MF: points to consider // Leukemia research, Vol.31(6), pp.737-740 2007.
- Mochizuki H., et al., Chronic myelogenous leukaemia with persistent neutrophilia, eosinophilia and basophilia in a cat. J Feline Med Surg. 2014 Jun;16(6):517-21. doi: 10.1177/1098612X13505576. Epub 2013 Oct 9. PMID: 24108200; PMCID: PMC11112184.
- Julie Webb, Chery Auch.Erythrocytosis (Polycythemia) in Animals, 2024/
- Musto P. et al. Combination of erythropoietin and thalidomide for the treatment of anemia in patients with myelodysplastic syndromes // Leukemia Research. — 2006. — Vol. 30, № 4. — Pp. 385–388. DOI: 10.1016/j.leukres.2005.08.020/
- Orkin S. H., Zon L. I. Hematopoiesis: an evolving paradigm for stem cell biology // Cell. — 2008 Feb 22;132(4):631-44. doi: 10.1016/j.cell.2008.01.025. PMID: 18295580; PMCID: PMC2628169.
- Pérez M. L., et al. Partial cytogenetic response with toceranib and prednisone treatment in a young dog with chronic monocytic leukemia // Anticancer Drugs. — 2013. — Vol. 24, № 10. — Pp. 1098–1103. DOI:10.1097/CAD.0000000000000018/
- PetMD Editorial. Myeloproliferative disorders in cats: symptoms and clinical approach // PetMD. — 2010.
- Reagan W. J. A review of myelofibrosis in dogs // Toxicologic Pathology. — 1993;21(2):164-9. doi: 10.1177/019262339302100208. PMID: 8210938.
- Rocha M. N. A. et al. Thrombocytosis: a retrospective study of 573 dogs (2016–2017) // Veterinary Medicine – Ciência Animal Brasileira. — 2019. — Vol. 20. DOI:10.1590/1089-6891v20e-51837
- Tefferi A., Barbui T. Polycythemia vera and essential thrombocythemia: 2021 update on diagnosis, riskstratification and management // American Journal of Hematology. — 2020. — Vol. 95, № 12. — Pp. 1599–1613.
- Thapa B., et al., Myeloproliferative Neoplasms // StatPearls [Internet]. — Treasure Island (FL): StatPearls Publishing; 2025 Jan.
- Thrall M. A., et al., Veterinary Hematology and Clinical Chemistry. 2nd ed. — Wiley-Blackwell; 2012.
- Valli V. E., Kiupel M., Bienzle D. et al. Classification of canine malignant lymphomas according to the World Health Organization criteria // Veterinary Pathology. — 2015. — Vol. 52, № 1. — Pp. 91–103.
- Vardiman J. W., Harris N. L., Brunning R. D. The World Health Organization classification of the myeloid neoplasms // Blood. 2002 Oct 1;100(7):2292-302. doi: 10.1182/blood-2002-04-1199. PMID: 12239137.
- E. Kelly Nitsche. Erythrocytosis in Dogs and Cats: Diagnosis and Management, 2004.
- Weiss D. J. New insights into the physiology and treatment of acquired myelodysplastic syndromes and aplastic pancytopenia // Veterinary Clinics of North America: Small Animal Practice. — 2003. — Vol. 33, № 6. — Pp. 1317–1334. PMID:14664201.
- Weiss D. J., Aird B. Cytologic evaluation of primary and secondary myelodysplastic syndromes in the dog // Veterinary Clinical Pathology. — 2001. — Vol. 30, № 2. — Pp. 67–75. DOI:10.1111/j.1939-165X.2001.tb00261.x.
- Weiss D. J., Smith S. A. A retrospective study of 19 cases of canine myelofibrosis // Journal of Veterinary Internal Medicine. — 2002. — Vol. 16, № 2. — Pp. 174–178.
- Weiss D. J., Smith S. A. Primary myelodysplastic syndromes of dogs: a report of 12 cases // Journal of Veterinary Internal Medicine. — 2000. — Vol. 14, № 5. — Pp. 491–494.
- Weiss D. J., Wardrop K. J. Schalm’s Veterinary Hematology. 6th ed. — Wiley-Blackwell; 2010.
- WHO Classification of Tumours Editorial Board. WHO Classification of Tumours: Haematolymphoid Tumours. 5th ed. — IARC; 2022.
- Withrow & MacEwen’s Small Animal Clinical Oncology. 5th ed. — Elsevier Saunders; 2014.
- Young N. S., Calado R. T. Aplastic anemia // New England Journal of Medicine. — 2015. — Vol. 373, № 17. — Pp. 1641–1652.
- Hisasue M., Tanaka M., Neo S. A cat with myelodysplastic syndrome by administration of the methylation inhibitor Azacytidine. // Vet Med Sci – 2022. – Vol. 24. – 142-148 pp.
- Takeshi M., Yasuhito F., Kuniyoshi Y., Hidefumi M., et al. Thrombocythemia in a Dog // Journal of Veterinary Medical Science. – 2006. – Vol. 68. – 1203-1206 pp.
- Ide K., Momoi Y., Minegishi M., et al. A severe hepatic disorder with myelodysplastic syndrome, treated with cytarabine ocfosfate, in a dog // Aust Vet J. – 2003. – Vol. 81. – 47-49 pp.
- Diogo C.C., Fabretti A.K., Camassa J.A., Bonelli Mde A., et al. Diagnosis and Treatment of Primary Erythrocytosis in a Dog: A Case Report // Top Companion Anim Med. – 2015. – Vol. 30. – 65-67 pp.
- Кузнецова А.Л. Миелодиспластический синдром // Тезисы XVIII Всероссийской конференции по онкологии мелких домашних животных. – Москва. – 2023.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург