1. Ветеринарная клиника неврологии, травматологии и интенсивной терапии, г. Санкт-Петербург, anna491994@gmail.com
2. ГВОЦ «Прайд», wolfberg.guard@gmail.com
Распространенность и разнообразие опухолей сердца не очень высоки, однако в литературных источниках можно встретить описание некоторых из них: гемангиосаркомы39,40, хемодектомы (параганглиомы)36,39, мезотелиомы4,8 17,43, злокачественной опухоли оболочек периферических нервов (шванномы)42, смешанной мезенхимальной опухоли16, миксомы2,9,12,23, 30, миксосаркомы1,7, хондросаркомы11,28, остеосаркомы29,32,33, липомы6 19 34, опухоли гранулярных клеток31, бластомы39, меланомы39, мастоцитомы39, фибромы21, фибросаркомы26,35,38, рабдомиомы27, рабдомиосаркомы20, лейомиомы15, лейомиосаркомы13, первичной кардиальной липомы39, лимфомы22, эктопической карциномы щитовидной железы3,5 18,39,40, гамартромы24.
В этой статье мы остановимся на наиболее распространенных новообразованиях.
Гемангиосаркома – это злокачественная опухоль, возникающая либо из сосудистого эндотелия, либо из эндотелиальных клеток-предшественников. Первичная гемангиосаркома может развиваться в любом хорошо васкуляризованном органе, но наиболее часто локализуется в селезенке, правом предсердии и ушке предсердия, почках и печени. Опухоль метастазирует на ранних стадиях по гематогенным путям, поскольку имеет свободный доступ к системному кровообращению. Подверженные породы – золотистый ретривер, немецкая овчарка, такса. Суки болеют чаще. Средний возраст заболевших – около 9 лет (3–13 лет).
Хемодектомы встречаются практически в 10 раз реже, чем гемангиосаркомы. Данные опухоли чаще всего локализуются у основания сердца вблизи синуса коронарных артерий, между аортой и легочной артерией, а также рядом с основанием правой подключичной артерии. У кошек опухоль чаще локализуется у основания левой подключичной артерии и с правой стороны от аорты. Каротидные тельца расположены на бифуркации общей сонной артерии. Данная опухоль доброкачественная, но она может вызывать значительные нарушения гемодинамики за счет сдавливания анатомических структур. Для этого типа опухолей характерна породная предрасположенность. В частности, у собак брахицефальных пород (боксеры, бостон-терьеры, французские бульдоги, грифоны, мопсы) чаще отмечают подобные опухоли. Предполагают, что виной этому является хроническая гипоксия, которая индуцирует гиперплазию хеморецепторных органов как у собак, так и у людей. Возрастная категория – 9 лет (диапазон от 7 до 12 лет).
Мезотелиомы – редкие опухоли, которые возникают из мезотелиальной оболочки серозных полостей и чаще всего поражают плевральный, перитонеальный и перикардиальные участки. Микроскопически выделяют три вида мезотелиом: эпителиоидные, саркоматоидные и смешанные (двухфазные). Мезотелиомы также способны включать другие мезенхимальные элементы, соответственно, мезотелиальные клетки обладают потенциалом опухолей с различными микроскопическими особенностями: хрящевыми, костными, мышечными и иногда жировыми. Этот неопластический процесс не имеет породной предрасположенности, однако в одном из исследований представлены данные о повышенной частоте встречаемости у золотистых ретриверов. Средний возраст – 8,6 лет (от 4 до 14 лет).
Миксома – это новообразование, состоящее из звездчатых мезенхимальных клеток, располагающихся в миксоидной строме.
Миксосаркома – злокачественная опухоль из клеток мезенхимального или фибробластного происхождения. В отличие от фибросаркомы имеет обилие муцина в межклеточной матрице. Опухоль часто демонстрирует локально инвазивное, агрессивное поведение. Наиболее часто встречаются миксосаркомы кожи, реже опухоли могут возникать в других участках, таких как сердце, глаза, мозг. Миксосаркомы чаще локализуются в левом желудочке, в правом предсердии, в области ушка правого предсердия и на трехстворчатом клапане.
Реже остальных встречается интракардиальная опухоль периферических нервных оболочек. Нейрогенные сердечные опухоли почти всегда являются первичными и доброкачественными, хотя были зарегистрированы злокачественные и метастатические новообразования. Предпочтительной локализацией является правая сторона сердца. Причина, обусловливающая данное местоположение, заключается в том, что происхождение сердечной шванномы берет начало от сердечной ветви блуждающего нерва и сердечного сплетения. В редких случаях шванному можно обнаружить в левом предсердии или вблизи левого желудочка. Наличие множественных внутрисердечных образований в этом случае необычно, это больше характерно для метастатических поражений.
Клинические признаки
Опухоли, в зависимости от типа и анатомического расположения, вызывают разнообразные клинические признаки. Неоплазии сердца могут вызывать разную степень тяжести манифестации клинических симптомов или быть случайной находкой. Чаще всего клинические симптомы не имеют прямой связи с характером опухоли, но больше зависят от локализации и вероятности образования выпота или обструкции магистральных сосудов.В большинстве случаев животные поступают в клинику с признаками перикардиального выпота, который может вызвать тампонаду с нарушением функции как правого предсердия, так и правого желудочка. Проявления идиопатического перикардиального выпота неотличимы от проявлений выпота, обусловленного неопластическим процессом. Более того, согласно статистике, на долю вызванных опухолью выпотов приходится до 60 % всех патологий перикарда.
Тампонада приводит к уменьшению преднагрузки, снижению сердечного выброса и/или правосторонней сердечной недостаточности.
Владельцы животных с неоплазией сердца нередко отмечают у своих питомцев приступы потери сознания, быструю утомляемость, пассивность, одышку, неожиданную слабость. При осмотре можно отметить приглушенные сердечные тоны, тахикардию, дефицит пульса, бледность слизистых, медленную скорость наполнения капилляров (СНК), диспноэ, положительный венный пульс, асцит, гидроторакс, признаки кахексии. Возможны также развитие синдрома краниальной полой вены при обширном росте опухоли и внезапная гибель животного при обструкции магистрального сосуда разросшейся неопластической массой. Признаки левосторонней недостаточности встречаются реже ввиду нечастой локализации опухолей в левой половине сердца. Нельзя исключить воздействие новообразований и на проводящую систему сердца: наджелудочковые и желудочковые тахикардии, атриовентрикулярные блокады также могут быть причиной внезапной смерти животного.
Диагностика
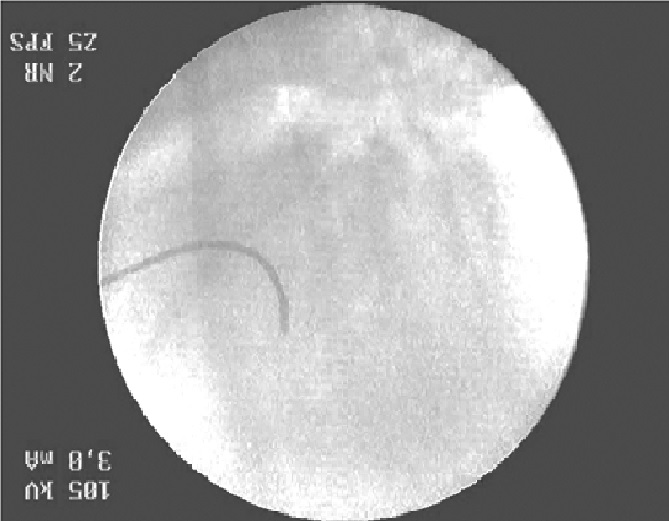
Для диагностирования сердечной опухоли необходимо использовать комплексный подход, который включает анамнестические данные, клинический осмотр, исследования крови (ОАК, биохимический анализ, исключение инфекционных процессов) и инструментальную диагностику. Задача врача-диагноста – охарактеризовать локализацию образования, определить первичное или вторичное поражение сердца, воздействие неопластических масс на функцию сердца и альтерацию внутренних регулирующих механизмов миокарда, выявить взаимоотношения образования с внутренними структурами грудной полости. Перечисленные параметры можно визуализировать с помощью ультразвуковой диагностики, ЭКГ, рентгенографии, томографии.Для определения типа неоплазии необходима оценка клеточной составляющей опухоли. Спектр средств диагностики достаточно широк: цитологическое исследование перикардиальной жидкости, тонкоигольная биопсия опухоли, отбор материала (полученного либо эндоваскулярным путем, либо при открытом доступе к неопластической массе) для гистологического исследования. Предпочтение отдается малоинвазивным методам ввиду нестабильности состояния животного на момент обращения к доктору. В нашей практике мы отдаем предпочтение эндоваскулярному методу с использованием рентгеноскопии (фото 1).
Лечение обычно предполагает хирургическое удаление новообразований и перикардиотомию, симптоматическую терапию, перикардиоцентез, радиотерапию и в случаях наличия чувствительных к цитостатикам новообразований – химиотерапию.
Прогноз вариативен. Среднее время выживания с гемангиосаркомой без лечения составляет 15–16 дней, при симптоматической терапии – 42 дня, среднее время жизни после операции и химиотерапии составляет 160–180 дней. У собак с лимфосаркомой, согласно литературным источникам, продолжительность жизни составляет 41–328 дней. Продолжительность жизни при мезотелиоме без лечения – 42 дня, а при перикардиотомии – 730 дней.
При доброкачественных опухолях существенную роль играют анатомическое расположение и биологическое поведение опухоли.
При выборе диагностического подхода необходимо руководствоваться такими основными моментами, как возможность взятия материала на гистологическое исследование, поскольку цитологическое исследование не всегда информативно и чаще всего основывается на отборе патологической жидкости из перикардиальной или грудной полости, и учитывать возможность полного или паллиативного удаления опухоли, в случае, когда она нарушает гемодинамический процесс. При этом необходимо оценить возможные риски, ассоциированные с манипуляцией, и ценность полученных результатов. Несмотря на неглубокую седацию и слабое влияние гипнотиков на функции сердечно-сосудистой системы, пациент перед манипуляцией должен быть стабилизирован гемодинамически, и анестезиологу следует быть готовым к нарушениям сердечного ритма и снижению давления в ходе процедуры. В случае, когда новообразование инфильтрирует стенку сердца и, соответственно, не подлежит хирургическому иссечению с последующим гистологическим исследованием материала для выбора тактики консервативного лечения, применяется методика эндоваскулярной диагностики. Также во всех случаях нарушения сердечной деятельности, связанной с патологическими изменениями тканей сердца, обосновано проведение данной диагностической методики с целью уточнения этиологической природы заболевания.
Трансваскулярная биопсия, помимо диагностики опухолевых процессов, может быть использована для выявления последовательных изменений биохимических, структурных и ультраструктурных сердечных показателей, что ранее также было доступно исключительно при инвазивном оперативном вмешательстве. Одним из наиболее значимых плюсов эндоваскулярной диагностики является возможность выявить локализованный инфекционный процесс посредством взятия образца из определенной ткани.
Техника трансваскулярной биопсии
Манипуляция проводится с использованием модифицированных биоптомов (Стэнфорда), одноразовых биопсийных щипцов под флюороскопическим контролем. Одноразовые щипцы обладают преимуществом перед многоразовыми, т.к. защитная оплетка первых не позволяет элементам рабочего механизма повреждать внутренние структуры органа. Для проведения манипуляции необходима седация животного. При положении пациента на боку доступ осуществляется через правую яремную вену, поскольку у некоторых животных предполагается наличие анатомической особенности, представляющей собой дополнительный сосуд, – левую полую вену, что может значительно затруднить проведение манипуляции. Также возможны доступы через артерии и вены бедра. Выбор сосуда зависит от поставленной задачи исследования и локализации патологических очагов.
Далее осуществляется сосудистый доступ с помощью постановки интродьюсера или секции. Интродьюсеры значительно облегчают задачу и позволяют без повторной перфорации сосуда отобрать необходимое количество образцов. Все манипуляции проводятся с соблюдением правил асептики и антисептики.
После обеспечения сосудистого доступа вводится биотом. С помощью флюороскопической визуализации, ориентируясь на анатомические маркеры, локализуют щипцы в области необходимого для взятия материала очага. Биотом вводится до упора, щипцы раскрываются, и производится захват материала из патологического очага. Отбор образцов ткани повторяется необходимое количество раз.
После окончательного извлечения инструмента удаляют интродьюсер и накладывают тугую повязку. При проведении секции ушивают сосуд и накладывают швы на кожу по правилам оперативной хирургии. Целостность сосудов необходимо сохранять для возможных последующих манипуляций.
Во время процедуры проводится мониторирование состояния животных по жизненно важным показателям с помощью ЭКГ-монитора, пульсоксиметра, капнографа и устройства для измерения давления. Контроль состояния проводится до полного реверса.
Возможными осложнениями при проведении данной процедуры могут быть отрыв хорды, травматизация клапанов, перфорация стенки камер ввиду неаккуратного отбора материала и погрешности в выборе локализации. Кровотечение при отсутствии перфорации стенок невозможно по объективным причинам. При адекватном анестезиологическом сопровождении риски осложнений невелики.
Гистопатологическое исследование ткани обычно является окончательным методом постановки диагноза. Данное исследование позволяет понять патогенез заболевания, что, в свою очередь, приводит к рациональному подходу в терапии.
За последние 25 лет техника субэндомиокардиальной биопсии была усовершенствована в той мере, в которой она проводится во всем мире и помогает в установлении этиологического фактора и выборе тактики лечения определенных сердечных заболеваний, в том числе онкологических. Биопсия стала ценным инструментом для диагностики кардиомиопатий, неоплазий, токсического воздействия на сердце некоторых противоопухолевых средств, а также системных болезней, которые влияют на сердечную деятельность.
Клинические случаи
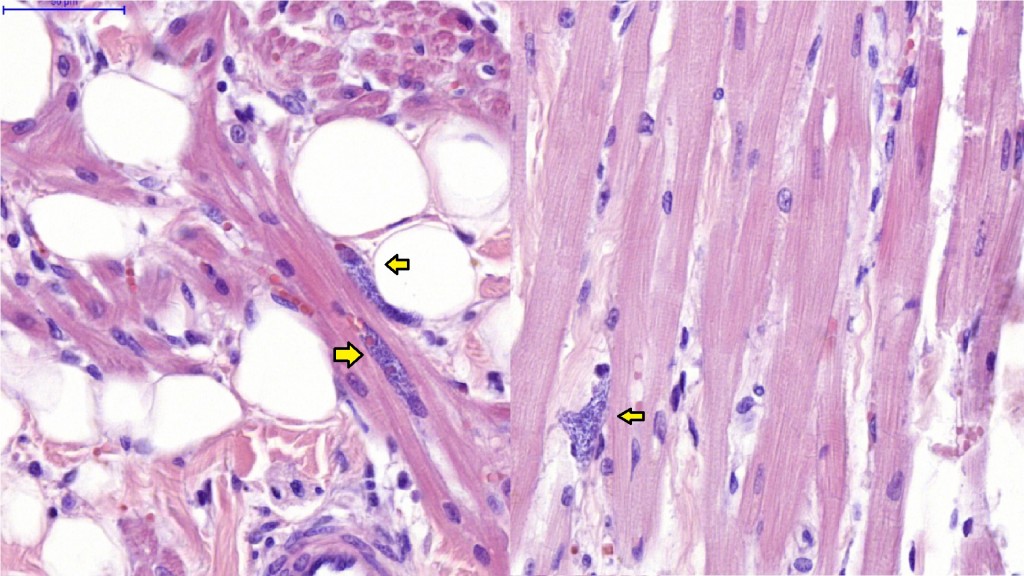
В нашей практике процедура биопсии проводится регулярно ввиду высокой частоты встречаемости соответствующих заболеваний. Наиболее показательными являются описанные ниже клинические случаи: пациенты с фенотипической картиной дилатационной кардиомиопатии, с подозрением на миокардит, приобретенными поражениями проводящей системы, быстро развивающейся сердечной недостаточностью, инфильтративными поражениями миокарда, внутриполостными опухолевыми образованиями.1. Миокардит у кошки, вызванный Toxoplasma gondii (фото 2).
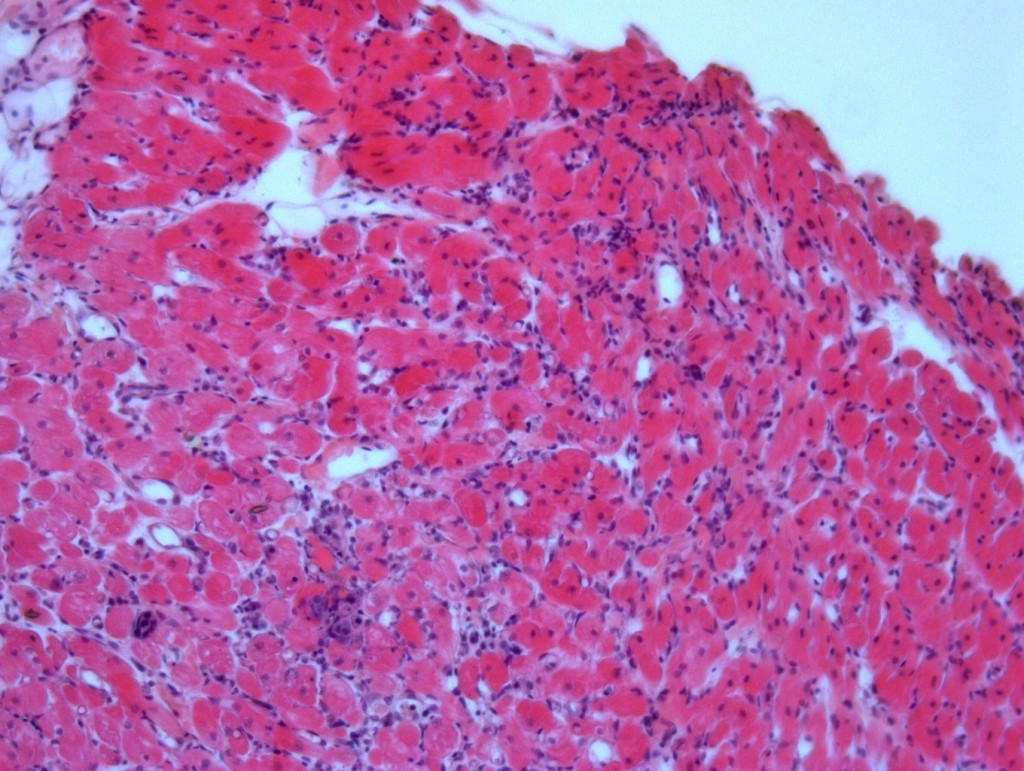
2. Пограничный миокардит у годовалой собаки, не имеющий выраженной клинической картины, но с транзиторной атриовентрикулярной блокадой 2-й степени и дилатацией полости левого предсердия и желудочка, сниженной систолической функцией (фото 3).
3. Стойкая атриовентрикулярная блокада 2-й степени и фиброз участка базального сегмента межжелудочковой перегородки в месте прохождения ножек пучка Гиса у полуторагодовалого спаниеля.
4. Инфильтрирующая миокард гемангиосаркома у кота 3,5 лет;
5. Метастатическое поражение тканей миокарда аденокарциномой легкого у кошки 8 лет (фото 4).
6. Лимфоцитарный миокардит у трех собак при боррелиозе (фото 5).
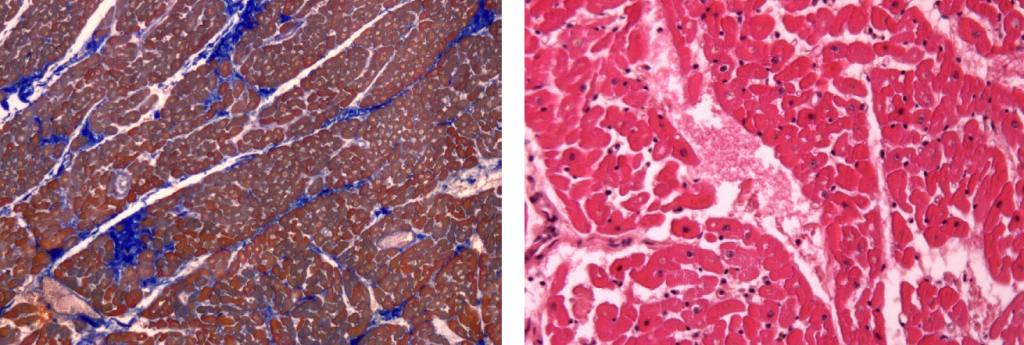
Фото 5. Выраженная пролиферация соединительнотканных элементов (слева). Окраска по Маллори, 200х. Обширные геморрагии в интерстициальном пространстве, единичные иммунокомпетентные клетки, отек кардиомиоцитов (справа). Окраска гематоксилин-эозином, 200х.
7. Опухоль у 4-летней собаки, растущая в межпредсердной перегородке и затрагивающая тракт от синоатриального узла к атриовентрикулярному соединению, вызывающая значительную атриовентрикулярную блокаду 1-й степени, которая при тахикардии способствует развитию синдрома Фредерика.
При проведении данной манипуляции летальные исходы отсутствовали. В момент взятия биопсии отмечались единичные желудочковые экстрасистолы. Других осложнений не наблюдалось, однако к рисковым факторам необходимо отнести предшествующее состояние. Например, атриовентрикулярная блокада 2-й или 3-й степени с низкой частотой сердечных сокращений будет способствовать снижению давления и повышать вероятность гибели животного. В то же время у пациента со сниженной систолической функцией левого желудочка риск получить негативный исход значительно меньше, чем при вышеописанных случаях, ввиду пластичности сердечного ритма по отношению к потребностям организма.
- Adissu H. A., Hayes G., Wood G. A. and Caswell J. L. Cardiac myxosarcoma with adrenal adenomaand pituitary hyperplasia resembling Carneycomplex in a dog. Veterinary Pathology,2010; 47:354–357.
- Akkoc A., Ozyigit M. O. and Cangul I. T. Valvularcardiac myxoma in a dog. Journal of VeterinaryMedicine. A, Physiology, Pathology, ClinicalMedicine,2007; 54: 356–358.
- Aupperle H., Marz I., Ellenberger C., Buschatz S.,Reischauer A. and Schoon H. A. Primary andsecondary heart tumours in dogs and cats. Journalof Comparative Pathology,2007;136: 18–26.
- Balli A., Lachat M., Gerber B., Baumgartner C. and Glaus T. Cardiac tamponade due to pericardial mesothelioma in an 11-year-old dog: diagnosis,medical and interventional treatments. Schweizer Archiv für Tierheilkunde, 2003; 145: 82–87.
- Bracha S., Caron I., Holmberg D. L., O’Grady M. R.,O’Sullivan L. M., Brisson B. A., et al. Ectopic thyroid carcinoma causing right ventricular outflow tract obstruction in a dog. Journalof the AmericanAnimal Hospital Association,2009; 45: 138–141.
- Brambilla P. G., Roccabianca P., Locatelli C., DiGiancamillo M., Di Marcello M. and Pittorru M.Primary cardiac lipoma in a dog. Journal ofVeterinary Internal Medicine,2006; 20: 691–693.
- Briggs O. M., Kirberger R. M. and Goldberg N. B. Rightatrial myxosarcoma in a dog. Journal of the SouthAfrican Veterinary Association,1997; 68: 144–146.
- Brower A., Herold L. V. and Kirby B. M. Caninecardiac mesothelioma with granular cellmorphology. Veterinary Pathology,2006; 43:384–387.
- Darke P. G. and Gordon L. R. Cardiac myxoma in adog. Veterinary Record,1974; 95: 565–567.
- Di Palma S., Lombard C., Kappeler A., Posthaus H.and Miclard J. Intracardiac ectopic thyroidadenoma in a dog. Veterinary Record,2010; 167:709–710.
- Dupuy-Mateos A., Wotton P. R., Blunden A. S. andWhite R. N. Primary cardiac chondrosarcoma in a paced dog. Veterinary Record,2008; 163: 272–273.
- Fernandez-del Palacio M. J., Sanchez J., Talavera J.and Martinez C. Left ventricular inflow tract© 2015 John Wiley & Sons Ltd, Veterinary and Comparative Oncology, 15, 2, 273–288.Cardiac tumours in dogs and cats 285 obstruction secondary to a myxoma in a dog. Journal of the American Animal Hospital Association,2011; 47: 217-223.
- Fews D., Scase T. J. and Battersby I. A.Leiomyosarcoma of the pericardium, with epicardial metastases and peripheral eosinophilia in a dog. Journal of Comparative Pathology, 2008;138: 224–228.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург