Ветеринарная клиника доктора Сотникова, г. Санкт-Петербург.
Целью данной статьи является детальное описание клинических проявлений лептоспироза у собак, течения этого заболевания, терапевтических подходов к его лечению и прогнозов, а также анализ ассоциированного с этим заболеванием вторичного гиперальдостеронизма на примере конкретного клинического случая.
Продолжение. Начало в №2.2025
Забегая вперед, приведем результаты проведенных анализов. Результат ПЦР на определение антигенов возбудителя лептоспироза в моче оказался положительным. С помощью реакции микроагглютинации (РМА) были обнаружены специфические антитела к лептоспирам Pomona в титре 1:3200, Icterohaemorrhagiae, Autumnalis и Cynopteri в титре 1:1600, а также к лептоспире Grippotyphosa в титре 1:50, что в совокупности свидетельствовало о положительном результате. РМА для обнаружения сывороточных антител против лептоспир и ПЦР для обнаружения ДНК лептоспир в настоящее время являются наиболее полезными диагностическими инструментами, доступными для практикующих врачей. Каждый из этих тестов имеет свои преимущества и ограничения, и их эффективность зависит от ряда факторов, включая стадию развития инфекции, а также предшествующее лечение антибиотиками.
Более подробно с преимуществами и недостатками этих исследований можно ознакомиться в обновленном консенсусном заявлении ACVIM по лептоспирозу у собак27.
Рениновая активность (PRA) составила 22,50 нг/мл/час (реф. зн. 0,30–2,60 нг/мл/час), результат измерения уровня альдостерона составил 387,8 пг/мл (реф. зн. 2–96 пг/мл), что в совокупности давало основание для постановки диагноза гиперренинемического гиперальдостеронизма, также известного как вторичный гиперальдостеронизм. Вторичный гиперальдостеронизм (ВГА) является редким состоянием в человеческой и (тем более) в ветеринарной медицине, в частности данные о ВГА у собак ограничены экспериментальными исследованиями. Альдостерон – это минералокортикоидный гормон, который способствует задержке натрия и воды почками, в конечном итоге повышая артериальное давление. Однако известно, что для собак артериальная гипертензия – это не обязательная находка даже при первичном гиперальдостеронизме. Альдостерон также увеличивает выделение калия с мочой, что приводит к гипокалиемии. Секреция альдостерона происходит в клубочковой зоне коры надпочечников. Вторичный гиперальдостеронизм обусловлен чрезмерной активацией ренин-ангиотензин-альдостероновой системы (РААС). У людей он может быть результатом физиологического состояния транзиторной активации РААС (например, гиповолемии), он также наблюдается при патологических состояниях устойчивой активации системы.
В данном клиническом случае у пациента отсутствовали признаки гиповолемии, анализ крови на альдостерон был взят после регидратации. Стеноз почечной артерии, например атеросклеротического или фибромышечного генеза, снижает почечный кровоток, что приводит к ложной стимуляции гиповолемии и увеличению секреции альдостерона. Застойная сердечная недостаточность левого желудочка и легочное сердце вызывают снижение сердечного выброса, что приводит к стимуляции выработки альдостерона. У пациентов с циррозом печени, нефротическим синдромом и асцитом снижение объема циркулирующей жидкости ухудшает перфузию почек и способствует увеличению секреции альдостерона. Активация РААС может быть вызвана опухолью, продуцирующей ренин в юкстагломерулярных клетках, хотя такие случаи редки. В нашем случае неадекватная секреция ренина и альдостерона у собаки, вероятно, была связана с почечной гипоперфузией на фоне лептоспирозного повреждения. При ВГА как концентрация ренина, так и активность ренина в плазме возрастают, поскольку ренин является основным стимулятором избыточной продукции альдостерона. В результате соотношение альдостерона и ренина в сыворотке оказывается значительно ниже, чем при первичном гиперальдостеронизме. Лечение вторичного гиперальдостеронизма наиболее эффективно при устранении основного заболевания, что обычно приводит к исчезновению симптомов. Для контроля гипокалиемии могут применяться добавки калия и калийсберегающие диуретики30.
Результаты бакпосева желчи, печени, а также анализ биоптатов методом ПЦР для выявления антигенов возбудителей кампилобактериоза и бартонеллеза оказались отрицательными. Цитологическое исследование желчи не предоставило значимой информации, выявив лишь нейтрофильное воспаление, которое могло быть связано с примесью периферической крови.
По результатам гистологического исследования печени был поставлен морфологический диагноз «хронический холангиогепатит умеренной степени выраженности, преимущественно лимфоплазмоцитарный».
На конец третьих суток пребывания пациента в ОРИТ (после хирургического вмешательства) терапия включала доксициклин, спиронолактон, смекту, поддерживающую инфузионную терапию с использованием раствора стерофундин и мультимодальную анальгезию с применением фентанила (3 мкг/кг/ч), кетамина (0,5 мг/кг/ч) и лидокаина (2 мг/кг/ч).
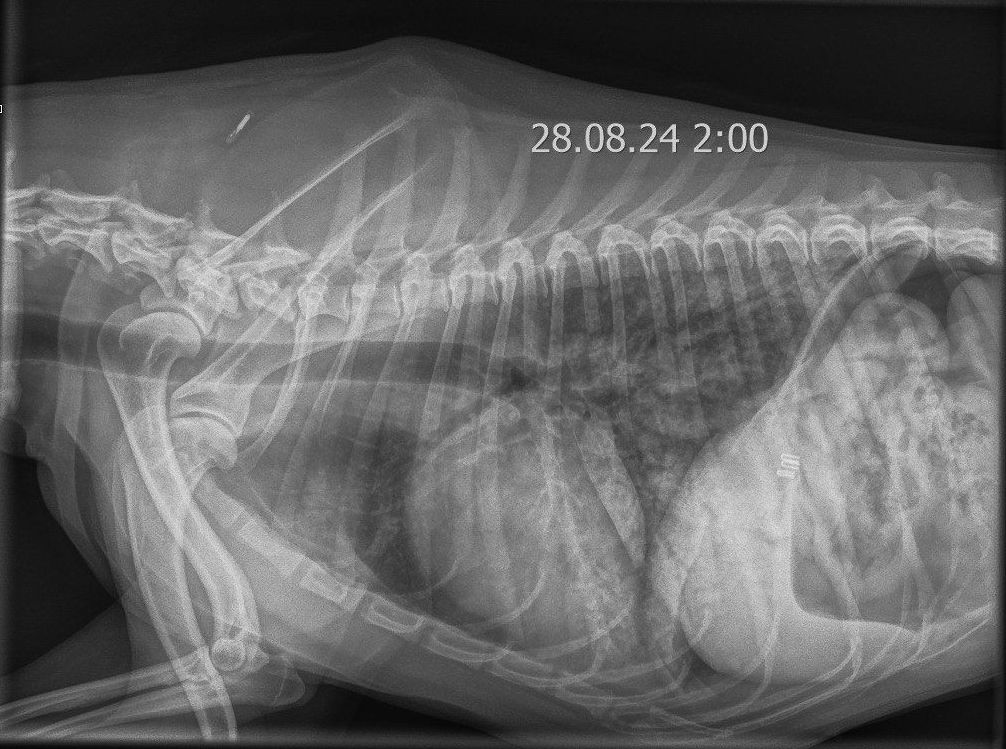
На пятые сутки, спустя двое суток после операции, общее состояние пациента и результаты анализов крови улучшились, активность увеличилась, собака стала более эмоциональной, но самостоятельный аппетит по-прежнему отсутствовал. Диарея не наблюдалась, жажда и мочеиспускание оставались без особенностей. Болезненность брюшной стенки оценивалась как легкая. Были отменены мультимодальная анальгезия, поддерживающая инфузионная терапия и смекта. Однако появились новые симптомы: кашель и увеличение частоты дыхательных движений во сне до 30 дых. дв./мин, без признаков диспноэ. Уровень насыщения крови кислородом (SpO2) без дополнительной оксигенотерапии составлял 93–95%. При рентгенологическом исследовании были выявлены преимущественно диффузные альвеолярные затемнения легочной ткани, охватывающие почти все поля легких. Наибольшая площадь поражения наблюдалась в каудальных долях обоих легких (рис. 9). Данные изменения в совокупности с установленным диагнозом указывали на высокую вероятность геморрагий в легочной паренхиме как одного из проявлений лептоспироза.
Бронхоальвеолярный лаваж не проводился по причине сохраняющегося стабильного состояния пациента, уже поставленного диагноза и назначенного специфического антибиотика. Значения коагулограммы, полученные в этот период, находились в пределах нормы.
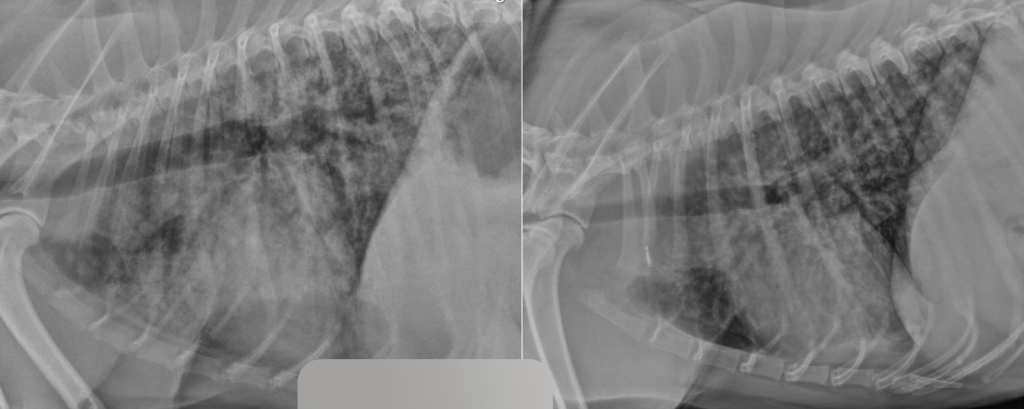
Синдром лептоспирозного легочного кровотечения (англ. leptospiral pulmonary haemorrhage syndrome; LPHS) является тяжелым проявлением острого лептоспироза и в последние годы все чаще диагностируется у собак и других видов животных14. Гистопатологические поражения легочной ткани при LPHS имеют схожие характеристики у разных видов и проявляются различной степенью внутриальвеолярного кровоизлияния при отсутствии выраженного воспалительного клеточного инфильтрата или васкулита. Внутриальвеолярный отек, фибрин и гиалиновые мембраны, характерные для патологий с диффузным альвеолярным повреждением (например, острый респираторный дистресс-синдром; ОРДС), также могут наблюдаться при LPHS, но не являются доминирующими признаками15. Патогенетические механизмы LPHS плохо изучены. В настоящее время исследуются несколько гипотез, включая системные воспалительные, иммуноопосредованные и прямые эффекты, вызываемые лептоспирами. Внутриальвеолярное кровоизлияние может быть обнаружено даже у собак без явных респираторных признаков17. Это указывает на то, что LPHS может быть более распространенным у собак с лептоспирозом, чем принято считать. Рентгенографические изменения, указывающие на LPHS, обычно первоначально проявляются в каудодорсальных отделах легочных полей и, как правило, носят двусторонний и недолевой характер. Поражения варьируются от легкого интерстициального рисунка до легкого или тяжелого ретикулонодулярного легочного рисунка с очаговыми альвеолярными инфильтратами. У некоторых собак наблюдается небольшое количество плеврального выпота (рис. 10). Рентгенографические изменения могут присутствовать даже при отсутствии клинических признаков респираторных нарушений26.
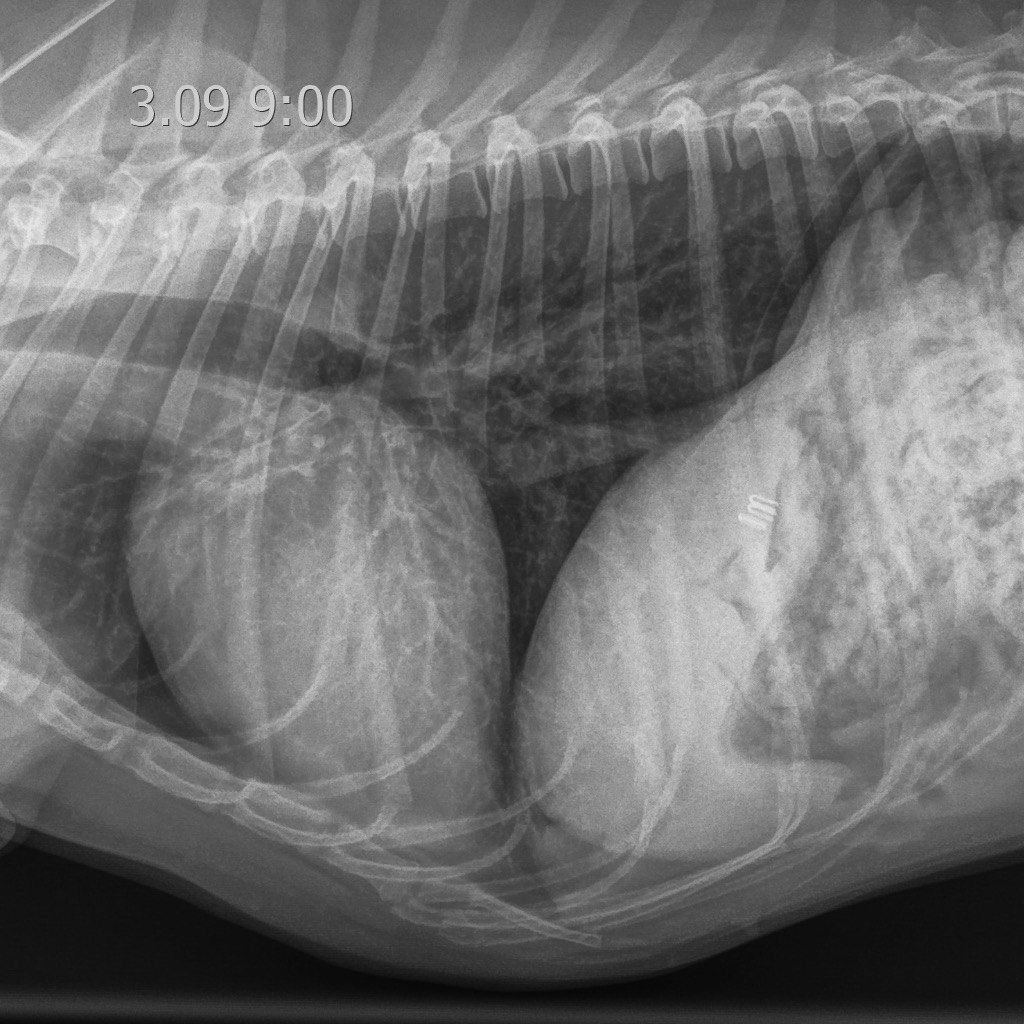
На восьмые сутки пребывания в ОРИТ у пациента наблюдались полное восстановление аппетита, нормализация общего состояния и активности. Респираторные симптомы были купированы, а рентгенологическая картина пришла в норму (рис. 11). Терапия включала использование доксициклина и спиронолактона в ранее установленных дозировках.
На 26-й день после начала применения доксициклина общее состояние пациента оставалось стабильным. Были взяты образцы крови для проведения общеклинического и биохимического анализов, а также моча для определения антигенов возбудителя лептоспироза методом ПЦР и сыворотка крови для выявления специфических антител к лептоспирам с использованием метода РМА.
Результаты ПЦР-исследования были отрицательными, что указывало на отсутствие ДНК лептоспир в образце. Реакция микроагглютинации (РМА) выявила присутствие антител к возбудителю лептоспироза только серогруппы Icterohaemorrhagiae в титре 1:800, что могло соответствовать поствакцинальному уровню. Антитела к другим серогруппам лептоспир не были обнаружены.
Результаты клинического анализа крови были без изменений. В биохимическом профиле наблюдались снижение уровня аланинаминотрансферазы с 2656,1 до 268,9 МЕ/л (реф. зн. 10,0–80,0 МЕ/л), нормализация уровня аспартатаминотрансферазы, снижение уровня щелочной фосфатазы с 5084,3 до 984,8 МЕ/л (реф. зн. 20,0–150,0 МЕ/л), а также рост уровня гамма-глутамилтрансферазы с 48,7 до 55,3 МЕ/л (реф. зн. 0,0–10,0 МЕ/л). Уровень глутаматдегидрогеназы снизился с 934,3 до 35,68 МЕ/л (реф. зн. 0,0–12,0 МЕ/л), уровень холестерина снизился с 7,29 до 7,08 ммоль/л (реф. зн. 3,5–7,0 ммоль/л), а концентрация общего билирубина нормализовалась.
В связи с отрицательными результатами ПЦР-исследования на лептоспироз, отсутствием или снижением антител к антигенам возбудителей лептоспироза, почти полной нормализацией биохимических показателей крови, а также полной нормализацией показателей клинического анализа крови и общего состояния пациента было принято решение отменить доксициклин. Пациент был выписан из стационара с назначением препарата «Спиронолактон» – 3 мг/кг 1 раз в день перорально. Спустя 14 дней после выписки по результатам мониторинга уровня электролитов препарат был отменен.
Выводы
Лептоспироз – высококонтагиозное заболевание, преимущественно поражающее собак, но также способное вызывать клинические проявления у людей. Болезнь может протекать как бессимптомно (при носительстве), так и в тяжелой форме с возможным летальным исходом, несмотря на своевременное лечение. Клиническая картина лептоспироза характеризуется вариабельностью симптомов, что затрудняет прогноз течения заболевания.В ходе недавнего исследования, направленного на оценку проявлений органной дисфункции у собак с острым лептоспирозом, были проанализированы данные 298 пациентов. Результаты показали высокую частоту поражения различных систем органов: 99,7% собак имели почечную дисфункцию, 35,4% – печеночную (подтвержденную наличием гипербилирубинемии), 68,8% – легочную и 18,4% – признаки диссеминированного внутрисосудистого свертывания (ДВС). У большинства собак (43,6%) наблюдалось поражение двух различных систем органов. В 24,5% случаев наблюдалось поражение только одного органа, в 23,2% – поражение трех систем органов, а у 8,7% животных были поражены все четыре системы органов14. Эти данные подчеркивают необходимость повышенного внимания ветеринарных врачей к лептоспирозу в своей повседневной практике.
Особое внимание хотелось бы обратить на то, что в данном исследовании впервые было описано развитие вторичного гиперальдостеронизма при лептоспирозе, что, вероятно, привело к стойкой гипокалиемии, несмотря на введение парентеральных препаратов калия.
- Faine S., Adler B., Bolin C., et al. Leptospira and Leptospirosis. 2nd ed. Melbourne: MediSci, 1999.
- Ganoza C. A., Matthias M. A., Saito M., et al. Asymptomatic renal colonization of humans in the peruvian Amazon by Leptospira. PLoS Negle Trop Dis, 2010.
- Arbour J., Blais M. C., Carioto L., et al. Clinical leptospirosis in three cats (2001-2009). J Am Anim Hosp Assoc, 2012.
- Klarenbeek A., Schuffner W. A. P. Appearance in Holland of Leptospira differing from Weil Strain. Nederlands Tijdschrift voor Geneeskunde, 1933.
- Ellis W. A. Control of canine leptospirosis in Europe: time for a change? Vet Rec, 2010.
- Ward M. P. Seasonality of canine leptospirosis in the United States and Canada and its association with rainfall. Prev Vet Med, 2002.
- Ghneim G. S., Viers J. H., Chomel B. B., et al. Use of a case-control study and geographic information systems to determine environmental and demographic risk factors for canine leptospirosis. Vet Res, 2007
- Werts C., Tapping R. I., Mathison J. C., et al. Leptospiral lipopolysaccha-ride activates cells through a TLR2-dependent mechanism. Nat Immunol, 2001.
- Meri T., Murgia R., Stefanel P., et al. Regulation of complement activation at the C3-level by serum resistant leptospires. Microb Pathog, 2005.
- Levett P. N. Leptospirosis. Clin Microb Rev, 2001.
- De Brito T., Menezes L. F., Lima D. M., et al. Immunohistochemical and in situ hybridization studies of the liver and kidney in human leptospirosis. Virchows Archiv, 2006.
- Mastrorilli C., Dondi F., Agnoli C., et al. Clinicopathologic features and outcome predictors of Leptospira interrogans Australis serogroup infection in dogs: a retrospective study of 20 cases (2001-2004). J Vet Intern Med, 2007.
- Yang H. L., Jiang X. C., Zhang X. Y., et al. Thrombocytopenia in the experimental leptospirosis of guinea pig is not related to disseminated intravascular coagulation. BMC Infect Dis, 2006.
- Major A., Schweighauser A. & Francey T. Increasing incidence of canine leptospirosis in Switzerland. Int J Environ Res Public Health, 2014.
- Nally J. E., Chantranuwat C., Wu X. Y., et al. Alveolar septal deposition of immunoglobulin and complement parallels pulmonary hemorrhage in a guinea pig model of severe pulmonary leptospirosis. Am J Pathol, 2004.
- Greenlee J. J., Alt D. P., Bolin C. A., et al. Experimental canine leptospirosis caused by Leptospira interrogans serovars pomona and bratislava. Am J Vet Res, 2005.
- Kohn B., Steinicke K., Arndt G., et al. Pulmonary abnormalities in dogs with leptospirosis. J Vet Intern Med, 2010.
- Greene E. C. Leptospirosis. In: Infectious Diseases of the Dog and Cat. 4th Ed. C. E. Greene. Elsevier, pp. 431-447, 2012.
- Schulz B. S., Seybold N., Adamik K. N., et al. Ileocolic intestinal intussus-ception in a dog with leptospirosis. Tierarztliche Praxis Ausgabe K: Kleintiere Heimtiere, pp. 403-405, 2010.
- Townsend W. M., Stiles J. & Krohne S. G. Leptospirosis and panuveitis in a dog. Vet Ophthalmol, 2006.
- Michel E., Kook P. H., Voss K., et al. [Generalized metastatic intestinal and cutaneous calcinosis in a Hovawart puppy with leptospirosis]. Schweiz Arch Tierheilkd, 2011.
- Kohn B., Engelbrecht R., Leibord W. Clinical findings, diagnostics and treatment results in primary and secondary immune-mediated thrombocytopenia in the dog. Kleintierpraxis, 2000.
- Geisen V., Stengel C., Brem S., et al. Canine leptospirosis infections – clinical signs and outcome with different suspected Leptospira serogroups (42 cases). J Small Anim Pract, 2007.
- Goldstein R. E., Lin R. C., Langston C. E., et al. Influence of infecting serogroup on clinical features of leptospirosis in dogs. J of Vet Intern Med, 2006.
- Mastrorilli C., Dondi F., Agnoli C., et al. Clinicopathologic features and outcome predictors of Leptospira interrogans Australis serogroup infection in dogs: a retrospective study of 20 cases (2001-2004). J Vet Intern Med, 2007.
- Baumann D. & Fluckiger M. Radiographic findings in the thorax of dogs with leptospiral infection. Vet Radiol Ultrasound, 2001.
- Jane E. Sykes et al. Updated ACVIM consensus statement on leptospirosis in dogs. J Vet Intern Med, 2023
- Vieira M. L., Nascimento A. Virulent Leptospira interrogans induce cytotoxic effects in human platelets in vitro through direct interactions. Front Microbiol, 2020.
- Juliette Sone et al. Prospective evaluation of abdominal ultrasonographic findings in 35 dogs with leptospirosis. Vet Radiol Ultrasound, 2018.
- Alejandro Dominguez, Vijayadershan Muppidi, Stephen W. Leslie, Sonu Gupta. Hyperaldosteronism, 2024.
- Birnbaum N. et al. Naturally acquired leptospirosis in 36 dogs: serological and clinicopathological features. J Small Anim Pract, 1998.
- Rentko V. T., et al. Canine leptospirosis. A retrospective study of 17 cases. J Vet Intern Med, 1992.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург