Ключевые слова: ДЗН – диск зрительного нерва; ВГД – внутриглазное давление; ОГ – офтальмогипертензия; ВГЖ – внутриглазная жидкость; ЦО – цилиарные отростки; ЦТ – цилиарное тело; ПК – передняя камера;
Глаукома – группа разнородных заболеваний (около 60), характеризующихся гибелью ганглиозных клеток сетчатки и увеличением экскавации диска зрительного нерва (ДЗН), что приводит к прогрессирующему снижению зрительных функций. Изменение внутриглазного давления (ВГД) при этом вариативно. На сегодняшний момент с точки зрения изменения ВГД разделяют гипер-, гипо- и нормотензивную глаукому. Например, при нормотензивной глаукоме выявляют нарушение перфузионного давления в сосудах сетчатки, а повышение ВГД при суточном мониторинге выше нормальных значений отсутствует.
В ветеринарной практике выявление глаукомы нормального и низкого давления является трудной задачей, поскольку не идентифицированы факторы риска (Oliver J., 2014), поэтому часто отождествляют офтальмогипертензию с глаукомой, что принципиально неверно. Однако следует отметить, что, по данным медицинских источников, повышение ВГД выше толерантного однозначно приводит к развитию глаукомы. Чем выше ВГД и чем дольше это состояние протекает, тем быстрее происходят необратимые изменения в сетчатке и ДЗН. Поэтому повышение ВГД является основным фактором риска развития глаукомы, при этом врачи его могут успешно контролировать.
Важным является своевременное обращение владельца животного к специалисту, а также регулярный профилактический осмотр у офтальмолога. Истинная глаукома пока не имеет надежных методов лечения. Современным и обоснованным подходом является контроль ВГД при повышении офтальмотонуса и нейропротекция. Здесь мы будем говорить о контроле ВГД.
Вот далеко не полный перечень патологических состояний, которые могут быть очевидной причиной повышения ВГД и развития глаукомы:
- Травма глазного яблока.
- Гониосинехии.
- Люксация хрусталика.
- Внутриглазное кровоизлияние.
- Неоплазия придаточного аппарата или интраокулярная.
- Набухающая катаракта.
- Гифема.
- Неоваскуляризация радужки.
- Задняя отслойка стекловидного тела.
- Грыжа стекловидного тела.
- Иридоцилиарная киста.
- Функциональный зрачковый блок.
- Породная предрасположенность.
- Гониодисгенез.
- Мезодермальный дисгенез.
- Возраст.
- Синдром пигментной дисперсии.
- Терапия стероидами, мидриатиками.
- Операции на глазном яблоке.
- Анатомические особенности угла передней камеры.
Используются препараты следующих групп (неполный список) и их комбинации:
• β-адреноблокаторы (тимолол, бетаксолол).Часто при лечении открытоугольной глаукомы наступает момент, когда гипотензивная терапия уже несостоятельна. В этой ситуации нужно прибегнуть к хирургическим методикам, принципиально разделяющимся на улучшающие отток и уменьшающие продукцию внутриглазной жидкости (ВГЖ). Если же глаукома закрытоугольная, то терапия препаратами может только снять острый приступ повышения ВГД и отсрочить необходимое в таком случае хирургическое вмешательство.
• α2-адреномиметики (клонидин, апраклонидин, бримонидин).
• М-холиномиметики (пилокарпин, ацеклидин).
• Аналоги простагландинов F2a (латанопрост, травопрост).
• Ингибиторы карбоангидразы (дорзоламид).
• Гиперосмотические средства (маннитол, глицерин).
Выбор методики хирургической коррекции глаукомы у животных остается за специалистом и зависит от сохранности зрения, состояния здоровья пациента, уровня подготовки хирурга и технических возможностей клиники.
На сегодняшний момент по частоте встречаемости в ветеринарной практике можно представить такой перечень процедур: абляция цилиарного тела гентамицином, энуклеация, интраокулярное протезирование, фистулизирующие (дренирующие) методики и лишь в конце – лазерная хирургия глаукомы. Заметим, что только последние два принципа могут применяться на зрячих глазах, тогда как применение других очевидно губительно для зрения.
Целью таких вмешательств при глаукоме различного генеза является:
1. Контроль ВГД для сохранения зрительных функций.Фистулизирующие операции (спонч-дренирование, клапан Ахмеда и др.) при относительной технической простоте выполнения имеют существенные недостатки. В первую очередь травматизм и непродолжительность хирургического эффекта. Последнее определяет необходимость дополнительного хирургического вмешательства. И если в гуманной медицине при хирургическом лечении глаукомы определяющим является принцип «сколько угодно операций для сохранения зрительной функции», то в ветеринарной практике такой подход наверняка встречал бы непонимание со стороны владельцев животных, так как это подразумевает дополнительный анестезиологический риск и серьезные финансовые затраты. Последнее к тому же является фактором, ограничивающим развитие антиглаукоматозных операций в ветеринарной офтальмологии. Поэтому при хирургии глаукомы часто руководствуются принципом «раз и навсегда». Но важно помнить о зрении: ставить его сохранность во главу угла в случае оказания первой помощи и выбора методики дальнейшего лечения.
2. Купирование боли для улучшения качества жизни.
3. Экономическая целесообразность (финансовые и временные затраты).
4. Косметический эффект.
Транссклеральная циклокриоабляция закисью азота или жидким азотом проводится с целью снизить ВГД или добиться субатрофии глазного яблока. Такая процедура может быть показана на невидящих глазах ввиду серьезных послеоперационных осложнений, которые были бы критичны для зрительной функции.
Лазерная хирургия глаукомы включает большое количество методик, но в ветеринарной практике они используются нечасто.
Транссклеральная циклофотоко-агуляция контактная (диодный лазер) и бесконтактная (YAG- лазер) предполагает проведение циклодеструкции с помощью лазерной энергии, распространяющейся через толщу конъюнктивы и склеры. При таком методе совершенно очевидны недостатки: нет визуализации анатомических особенностей расположения отростков цилиарного тела, невозможно точно дозировать лазерную энергию, что приводит к таким осложнениям, как выраженный увеит, отслойка цилиарного тела, гифема, стойкий мидриаз и др., почти не оставляя возможности для сохранения зрения.
Еще одним из лазерных методов коррекции высокого уровня ВГД является эндоскопическая циклофотоко-агуляция (ЭЦФК). Это новейшая форма технологии лазерной циклофотодеструкции. На современном этапе развития ЭЦФК приобретает все больший интерес, а изучение данной методики становится весьма актуальным. Однако пока в ветеринарной практике встречается ограниченное количество публикаций (Bras D.,Webb T.).
Мартин Урам (Martin Uram) в 1992 году разработал интраокулярный лазерный эндоскоп. В том же году появилось первое сообщение о применении эндолазера для лечения неоваскулярной глаукомы у человека.
Суть метода состоит в той же коагуляции отростков (ЦО) цилиарного тела инфракрасным лазером, но при этом лазерная энергия доставляется непосредственно к ЦО с помощью эндозонда, что дает возможность использовать малые мощности излучения для достижения результата и минимизировать травматизацию тканей. А использование эндоскопа позволяет прецизионно выполнять процедуру, что отвечает последним веяниям в офтальмологии – минимизация хирургической травмы при эндоокулярных вмешательствах. Дополнительным преимуществом является возможность проведения ЭЦФК одномоментно с другими операциями, такими как экстракция травматической, набухающей катаракты, люксированного хрусталика и витрэктомия, когда эти состояния ассоциируются с начальной или развитой глаукомой.
Это устройство (рис. 1) имеет две основные части: консоль и лазерный эндоскоп. Консоль включает в себя 3 блока: блок генерации лазерного излучения, блок освещения мощностью 175 Вт и видеоблок. Эндоскоп состоит из трех групп волокон (для визуализации, для освещения и для лазерного излучения) и имеет три разъема для подключения к соответствующему блоку на консоли. Все три типа волокон объединены в одном наконечнике 20-го или 23-го калибра, что позволяет через один парацентез выполнять данную процедуру, не используя при этом операционный микроскоп, а контролируя свои действия, глядя на монитор.
Показаниями для ЭЦФК являются терминальные стадии первичной, вторичной, травматической, пигментной, увеальной и неоваскулярной глаукомы, болящая глаукома и неэффективность другого лечения. То есть любая глаукома, за исключением, пожалуй, связанной с неоплазией, может быть показанием к ЭЦФК. Эта процедура возможна для факичных, псевдофакичных и афакичных глаз.
Сравнение данного метода корректно с транссклеральной контактной циклофотокоагуляцией, так как в обоих случаях применяют лазерное излучение одинаковой длины волны (810 нм), при этом мощность излучения, используемая при эндоскопическом варианте, существенно меньше
(1,5–2,0 Вт и 0,05–1,0 Вт соответственно), что наряду с эндоскопическим принципом определяет целый ряд преимуществ (малые разрезы, низкая мощность излучения, хорошая визуализация, точность выполнения, короткое время процедуры, техническая простота).
Процедура проводится под общей анестезией, которая не имеет принципиальных особенностей, в комбинации с перибульбарными и ретробульбарными блокадами, а также с введением 2%-ного раствора лидокаина в переднюю камеру (ПК) глаза.
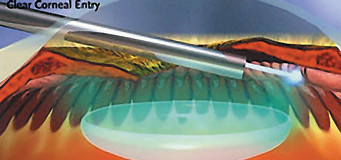
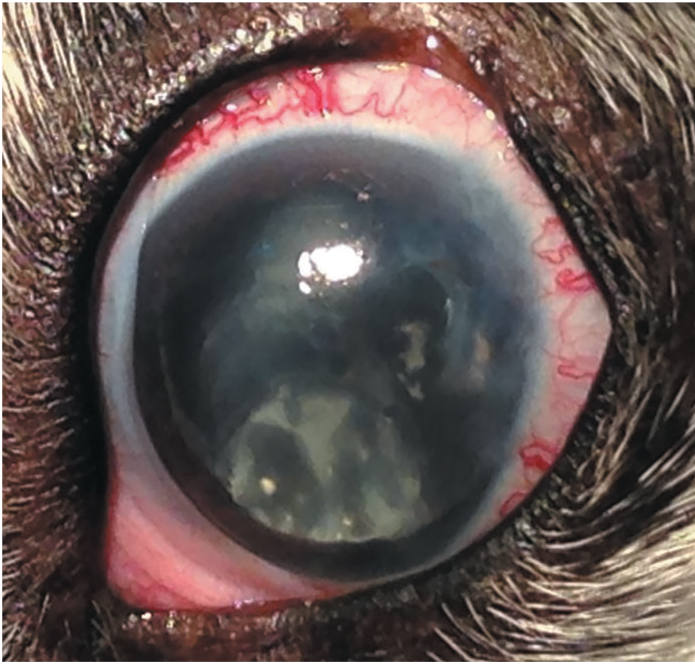
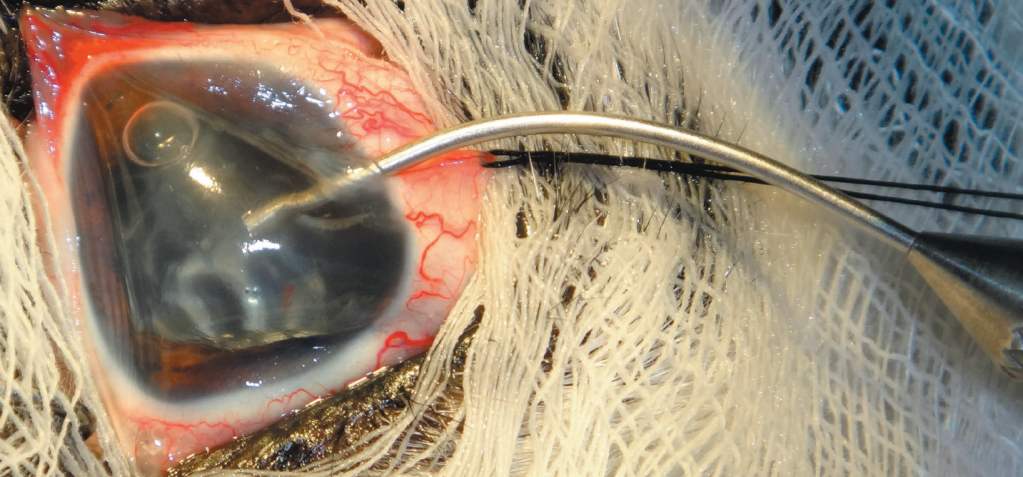
Животное укладывают в боковом положении. Сбривают шерстный покров с век и ресницы. Кожу век и поверхность конъюнктивы дезинфицируют. За день-два до процедуры рекомендуется местное применение антибиотиков широкого спектра в комбинации с противовоспалительными препаратами. С помощью швов-держалок (возможно сочетание с векорасширителем) достигают удобного положения глазного яблока в горизонтальной плоскости. После отграничения операционного поля офтальмологическим ножом типа «копье» размером 19G формируют тоннельный разрез для эндозонда шириной до 2 мм. Это лимбальный доступ (рис. 2), однако возможен доступ и через pars plana (плоская часть) цилиарного тела (рис. 3). Если же требуется коагуляция цилиарных отростков на протяжении более 180°, то контрлатерально выполняют второй лимбальный разрез.
Если для терапевтического контроля ВГД применялись аналоги простагландинов или иные миотики, их следует отменить минимум за сутки до планируемой ЭЦФК для достижения лучшего мидриаза. Хотя мидриаз и не является обязательным условием ЭЦФК, все же это создает лучшие условия для защиты радужки при манипуляциях в передней камере глаза. Мидриаза достигают путем введения раствора мезатона в ПК глаза.
Если у пациента высокий уровень ВГД, то перед выполнением тоннельного разреза с гипотензивной целью производят парацентез иглой 30G и ожидают плавного снижения ВГД.
Затем между радужкой и капсулой хрусталика вводят адгезивный вискоэластик. Он помогает поддерживать форму, предотвращая спадание глазного яблока, а также играет важную роль в нераспространении крови из цилиарного тела или радужки в случае избыточного лазерного воздействия или случайного повреждения.
Потом эндозонд вводится через сформированное отверстие, подводится к цилиарному телу. При этом нужно провести коррекцию освещения и резкости на консоли для лучшей визуализации. После чего настраивают параметры лазерного излучения, начиная с низкой мощности
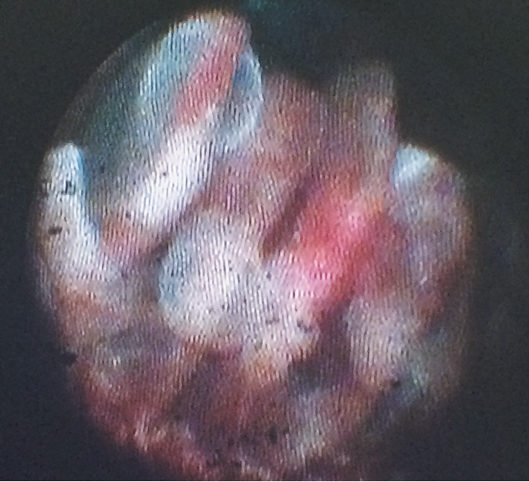
(0,2–0,3 Вт), и времени воздействия. Критериями оптимального воздействия является изменение цвета до белого поверхности ЦО и их сморщивание, далее повышение мощности воздействия следует остановить.
В зависимости от изначального уровня ВГД производят коагуляцию ЦО в секторе от 180° до 360°.
Визуализация при ЭЦФК позволяет также детально оценить состояние других интраокулярных структур, когда иные методы визуализации затруднительны. Может быть выявлена грыжа стекловидного тела, иридоцилиарная киста, интраокулярная опухоль и др.
Это наш первый опыт в ЭЦФК. На данный момент было прооперировано 8 собак разных половозрастных групп и пород, в том числе и беспородных. Все глаза были незрячими по причине развития первичной или вторичной глаукомы. Было 3 случая глаукомы на псевдофакичных глазах (в отдаленном периоде после фако-эмульсификации и имплантации искусственного хрусталика).
В послеоперационном периоде проводили интенсивную местную и системную терапию комбинацией стероидных и нестероидных противовоспалительных препаратов вплоть до интравитреальных инъекций триамцинолона. Также осуществлялся контроль ВГД с использованием местных гипотензивных препаратов, полная или частичная отмена которых была возможна уже в течение первых 3–5 недель после ЭЦФК.
Осложнения, которые мы встречали в послеоперационном периоде, включали увеит, гифему, набухающую катаракту, гипоэффект, транзиторную гипертензию.
Трудно представить объективную статистику при такой малой выборке, но все же можно сделать некоторые важные выводы:
Во всех случаях, кроме одного, когда потребовалась повторная ЭЦФК, мы получили выраженное снижение офтальмотонуса от исходного уровня (практически вдвое).
Эффективная коагуляция ЦО происходила при различных уровнях мощности лазерного излучения, что (судя по данным медицинской литературы) зависит от степени пигментации коагулируемой ткани.
Метод сразу показал свою эффективность при относительной простоте и низкой хирургической травматизации, что подтверждается (пусть и немногочисленными) литературными данными, относящимися в основном к гуманной медицине.
Выполнение ЭЦФК возможно в сочетании с другими оперативными вмешательствами (экстракция и факоэмульсификация катаракты, витрэктомия).
Преимуществами ЭЦФК бесспорно являются точное и локальное воздействие, кратковременность процедуры, быстрое послеоперационное восстановление.
Требуется дальнейшее изучение такой перспективной методики, как ЭЦФК, у мелких домашних животных, поскольку она имеет меньше осложнений по сравнению с транссклеральной циклодеструкцией.
Литература:
1. Бояринов С. А. Фармакотерапия увеальной глаукомы у собак / С. А. Бояринов, С. В. Сароян // Вопросы ветеринарии и ветеринарной биологии. – 2012. – Вып. 8. – С. 46–50.2. Бояринов С. А. Дифференциальная диагностика увеальной офтальмогипертензии и постувеальной глаукомы у собак / С. А. Бояринов, С. В. Сароян, С. В. Комаров // РВЖ. МДЖ. – 2014. – №2. – С. 15–18.
3. Essentials of veterinary ophthalmology. Еdited by Kirk N. Gelatt. — Baltimore, Md.: Lippincott Williams & Wilkins, 2000. – 595 pр.
4. David J. Maggs, Paul E. Miller, Ron Ofri. Slatter`s fundamentals of veterinary ophthalmology. Saunders Elsevier: St Louis. Mo. 2013. – 506 pр.
5. Veterinary Ophthalmology: Two Volume Set (5th edition) / Kirk N. Gelatt (Editor), Brian C.
Gilger (Editor), Thomas J. Kern (Editor) – Chichester, Wiley-Blackwell (an imprint of John
Wiley & Sons Ltd), 2013. – 2260 pр.
6. Oliver J. Canine primary glaucoma. Veterinary Times № 07 of 17/02/2014.
7. Bras I. D., Robbin T. E., Wyman M. et al. Diode endoscopic cyclophotocoagulation in canine and feline glaucoma (abstract), 36th Proceedings of the American College of Veterinary Ophthalmologists, 2005.






 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург