Регионарная анестезия стала «спасательным кругом» для контроля боли в реалиях современной российской ветеринарной медицины. Отсутствие лицензий, перебои в поставках препаратов, повышение цен на ввозимые в страну медикаменты – все это побудило ветеринарных врачей обратить пристальное внимание на локальные техники анестезии. Регионарная анестезия имеет много плюсов: качественный контроль боли, повышение комфорта пациентов и удовлетворенности владельцев, более быстрое восстановление после хирургии, низкая себестоимость. Однако местные анестетики, как и любые другие препараты, имеют ряд недостатков. Используя те или иные добавки, можно попытаться повлиять на часть из них.
Адъюванты
Адъюванты – это препараты, которые действуют синергически с местными анестетиками (МА), помогая повышать качество и эффективность регионарных методик.Адъюванты могут ускорить начало действия анальгезии, увеличить продолжительность обезболивания, улучшить качество обезболивания и снизить потенциальные побочные эффекты, связанные с местными анестетиками. Адъюванты изучаются уже несколько десятилетий с использованием различных путей, включая системное, периневральное и местное введение.
В этой статье будут рассмотрены фармакология, механизм действия, эффективность и безопасность наиболее распространенных адъювантов для регионарной анестезии.
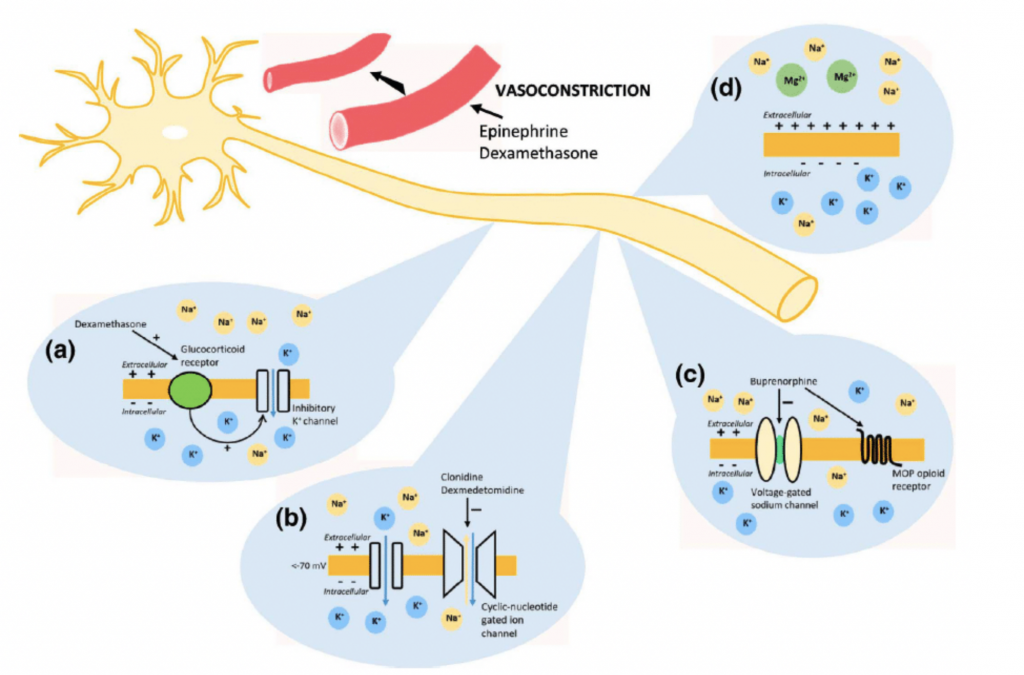
Адреналин – один из первых препаратов, который начал использоваться как адъювант в регионарной анестезии. Являясь мощным вазоконстриктором, он замедляет скорость абсорбции МА из места введения в системное русло, что может увеличивать время и мощность блокады и снижать скорость нарастания концентрации препарата в плазме крови (рис. 17).
Добавление адреналина в соотношении 1:200000 (5 мкг/мл) увеличивает длительность блокады при комбинации с низко растворимыми в жирах местными анестетиками (лидокаин) и не влияет на длительность эффекта блокады при ведении препаратов, обладающих высокой растворимостью в жирах (бупивакаин, ропивакаин). Использование адреналина может уменьшать риск возникновения системной токсичности, особенно для блокад, требующих высокой дозы МА. Однако экспериментально было доказано, что добавление вазоконстриктора может ухудшать кровообращение в нерве и увеличивать риск местного токсического влияния МА на нервную ткань1.
Также некоторые анестезиологи применяют адреналин в качестве маркера непреднамеренного внутрисосудистого введения. Даже небольшая доза адреналина при попадании в системное русло вызовет моментальное повышение ЧСС минимум на 20% от исходного1. С началом использования дексмедетомидина в качестве адъюванта адреналин отошел на второй план и в настоящее время используется редко.
Дексмедетомидин
Дексмедетомидин является селективным альфа-2-агонистом с анальгетическими и седативными свойствами. Внутривенное введение дексмедетомидина часто используется в качестве седативного средства в отделении интенсивной терапии или в периоперационных условиях для премедикации беспокойных пациентов. Его потенциальная роль как адъюванта в регионарных блокадах изучалась несколько десятилетий и, согласно мета-анализу 14 исследований в гуманной медицине с участием 848 людей, был сделан вывод, что дексмедетомидин продлевает продолжительность сенсорного и моторного блоков примерно в 1,2 раза.Механизм действия дексмедетомидина заключается, с одной стороны, в ингибировании потенциалов действия С-волокон, а с другой стороны, оказывает фармакокинетическое действие на перераспределение местных анестетиков, опосредованное сосудосуживающим эффектом на α1-рецептор (рис. 1b). Также проводились сравнительные исследования эффективности периневрального и внутривенного введения данного препарата6. И, хотя было обнаружено, что оба пути введения дексмедетомидина продлевают продолжительность действия местного анестетика, периневральное введение оказалось более эффективным, чем системное.
Возможные осложнения при периневральном использовании дексмедетомидина включают те же осложнения, что и при внутривенном введении: развитие гипотензии, брадикардии, седативный эффект и продленный реверс из анестезии.
Доза:1 мкг/1 мл раствора местного анестетика.
Гидрокарбонат натрия
Теоретическая роль бикарбоната натрия как адъюванта в препаратах для местной анестезии заключается в повышении pH анестетика. Местные анестетики имеют значения рН в диапазоне от 3,9 до 6,7. Подщелачивание приближает рН вводимого раствора к нормальному рН ткани, что позволяет анестетику находиться преимущественно в неионизированной форме.Неионизированный анестетик более эффективно проникает через липидные мембраны периферических нервов, что усиливает эффект блокады нерва и приводит к более быстрому началу действия. Количество бикарбоната натрия, необходимое для получения эффекта, варьируется из-за различий уровня показателя pH раствора между отдельными анестетиками и между производителями. Например, мепивакаин и лидокаин представляют собой два анестетика, которые легко подщелачиваются бикарбонатом натрия и могут использоваться с минимальным риском возникновения побочных эффектов. Однако с некоторыми растворами анестетиков, такими как бупивакаин или ропивакаин, для этой цели необходимо использовать бикарбонат натрия в гораздо меньших количествах, потому что анестетик будет легче осаждаться в нерастворимое основание даже при незначительном увеличении рН. Кроме того, кислые растворы более болезненны при проведении инъекций, что является важным фактором для бодрствующих пациентов или пациентов с легкой седацией. В связи с этим, повышая рH раствора местного анестетика с помощью бикарбоната натрия, можно значительно снизить дискомфорт пациента.
Дозы:
- 1 mEq на 10 мл 2%-ного раствора лидокаина;
- 0,1 mEq на 10 мл бупивакаина/ропивакаина.
Дексаметазон
Дексаметазон – синтетический кортикостероид длительного действия, обладающий широким спектром физиологических эффектов. К ним относятся, помимо прочего, иммуносупрессивные и противовоспалительные свойства, опосредованные в первую очередь предотвращением высвобождения цитокинов посредством ингибирования циклооксигеназы. В последнее время были проведены исследования для понимания его роли как адъюванта к местным анестетикам7.Периневральные кортикостероиды действуют по нескольким механизмам, включая ослабление высвобождения медиаторов воспаления, снижение эктопического разряда нейронов и ингибирование опосредованного калиевыми каналами разряда ноцицептивных С-волокон. Доказано, что дексаметазон улучшает качество и продолжительность блокады периферических нервов при введении в сочетании с местными анестетиками8.
Потенциальные побочные эффекты кортикостероидов включают подавление иммунитета, повышенный риск развития инфекции, нарушение заживления ран и гипергликемию. В нескольких исследованиях изучалось, обладает ли дексаметазон в качестве адъювантной терапии к регионарной анестезии такими же побочными эффектами. Два больших мета-анализа не показали различий в частоте инфицирования или заживлении ран в группах лечения по сравнению с контрольными1.
В своей практике мы задались вопросом возможности сочетания периневрального дексаметазона с НПВС, которые рутинно используются для послеоперационной анальгезии. На момент написания статьи более чем у 40 пациентов осложнений при таком протоколе выявлено не было.
Доза: 0,1 мг/кг.
Опиоиды
Опиоиды одними из первых начали использовать в качестве адъювантов при нейроаксиальных блокадах. В нашей практике мы применяем морфин и фентанил в сочетании с местными анестетиками при эпидуральной и кокцигеальной блокаде. Действие морфина при введении в эпидуральное пространство наступает примерно через полчаса-час после блокады и продолжается до 24 часов.Побочным эффектом введения морфина, требующим контроля, является задержка мочеиспускания.
Фентанил же начинает действовать спустя 20 минут после введения с продолжительностью в течение около 5 часов.
При блокадах периферических нервов опиоиды начали использовать вскоре после открытия периферического опиоидного рецептора. Опиоиды потенцируют антиноцицептивное действие местных анестетиков за счет рецепторов, связанных с G-белком, вызывая гиперполяризацию афферентных сенсорных нейронов. Однако в систематических обзорах гуманной медицины, опубликованных в 1997 и 2000 годах, было обнаружено мало доказательств пользы добавления опиоидов к местным анестетикам при блокаде периферических нервов. Анальгетический эффект ставится под сомнение, так как невозможно интерпретировать, оказывает ли периферический опиоид истинный периферический эффект или же он поступает в ЦНС и оказывает системный анальгетический эффект. Истинная периферически опосредованная опиоидная анальгезия может быть полезной, если она связана с улучшением местного обезболивания или уменьшением побочных эффектов по сравнению с системным введением.
Несмотря на эти неутешительные результаты, один опиоидный агонист продемонстрировал обезболивающую эффективность при периневральном введении, – это бупренорфин. Бупренорфин является частичным агонистом µ-рецепторов с очень высоким сродством к рецепторам по сравнению с фентанилом (в 24 раза) или морфином (в 50 раз). Кроме того, он обладает промежуточной растворимостью в липидах, что позволяет ему проникать через мембрану нейрона. Бупренорфин блокирует потенциал-зависимые Na-каналы и таким образом действует как местный анестетик.
Исследования показали, что применение периневрального бупренорфина вместе с местным анестетиком почти вдвое увеличивает продолжительность обезболивания при ортопедических операциях1.
Дозы опиоидов при нейроаксиальных блокадах:
- Морфин – 0,1 мг/кг;
- Фентанил – 1–5 мкг/кг;
- Буторфанол – 0,25 мг/кг.
NMDA-антагонисты
В окончаниях периферических нервов находится множество глутаматных рецепторов, которые участвуют в периферической передаче болевых сигналов. Был проведен ряд исследований, оценивающих влияние антагонистов NMDA на периферически опосредованное обезболивание у пациентов.Кетамин является неконкурентным антагонистом рецептора NMDA. Он используется для премедикации, седации, индукции и поддержания общей анестезии3. Добавление кетамина к эпидуральному лидокаину или бупивакаину увеличивает продолжительность регионарной анестезии и улучшает анальгезию. По результатам некоторых исследований кетамин ускоряет начало действия блокады4.
Доза: 2 мг/кг.
Магния сульфат. На данный момент магния сульфат является наименее изученным адъювантом в ветеринарной медицине. Данных по его рутинному использованию практически нет, однако он является еще одним антагонистом NMDA, который потенциально может использоваться в качестве адъюванта. Магний блокирует ионный канал на рецепторе NMDA при нормальных физиологических состояниях. Блокада канала рецептора NMDA введением магния позволяет снизить возбудимость периферических нервов, а также помогает местным анестетикам повышать порог возбуждения болевых волокон (рис. 1d). Несколько исследований показали, что добавление магния может пролонгировать обезболивание при блокадах периферических нервов1.
Потенциальные побочные эффекты включают гиперемию, гипотензию, вазодилатацию и сонливость. Прежде чем рекомендовать рутинное периневральное введение, необходимо провести дополнительные исследования потенциальной нейротоксичности.
Доза: 2,5–10 мг/кг.
Заключение
Практикующие врачи при лечении пациентов с периоперационной, острой или хронической болью должны быть знакомы с методами регионарной анестезии и препаратами, которые для них используются. Регионарная анестезия набирает популярность, развиваются навигационные техники: УЗИ, нейростимуляция.В данной статье мы рассмотрели наиболее часто используемые адъюванты для регионарной анестезии. Некоторые адъюванты требуют более тщательного изучения для понимания целесообразности их применения. Однако в настоящее время многие адъюванты широко изучены, и результаты опубликованных исследований доказывают, что добавление их к местным анестетикам помогает продлить обезболивающий эффект и улучшить послеоперационную анальгезию.
Будущие исследования в конечном итоге помогут стандартизировать роль адъювантов регионарной анестезии при проведении блокады нервов в клинической практике.
Список литературы:
- Dr Steve Tresierra, Dr Ian Gilron, Dr Glenio B. Mizubuti. Adjuvant Medications for Peripheral Nerve Blocks, 2023.
- Hamaseh Tayari, Pablo E. Otero, et al. Epidural Volume of Injectate Using a Dose Regimen Based on Occipito-Coccygeal Spinal Length (OCL): Randomized Clinical Study Comparing Different Ropivacaine Concentrations, with or without Morphine, in Bitches Undergoing Total Unilateral Mastectomy, 2022.
- Mohammadreza Lashgarinia, Khosro Naghibi, Azim Honarmand, Mohammadreza Safavi, and Mehdi Khazaei. Effect of ketamine as an adjuvant in ultrasound-guided supraclavicular brachial plexus block: A double-blind randomized clinical trial study, 2014.
- Ibrahim A. Y., Labib H. A., Toulan H. F. A. and Deabes E. A. Comparative Study between Ketamine and Magnesium Sulfate as Adjuvant to Bupivacaine in Ultrasound Guided Supra-Clavicular Brachial Plexus Block, 2020.
- Clément Tschopp , Martin R. Tramèr , Alexis Schneider , Maroun Zaarour , Nadia Elia. Benefit and Harm of Adding Epinephrine to a Local Anesthetic for Neuraxial and Locoregional Anesthesia: A Meta-analysis of Randomized Controlled Trials With Trial Sequential Analyses. Anesth Analg, 2018
- Hussain N., Brummett C. M., Brull R., et al. Efficacy of perineural versus intravenous dexmedetomidine as a peripheral nerve block adjunct: a systematic review. Reg Anesth Pain Med, 2021.
- Desai N., Kirkham K.R., Albrecht E. Local anaesthetic adjuncts for peripheral regional anaesthesia: a narrative review. Anaesthesia. 2021
- Colin J. L. McCartney and Stephen Choi. Analgesic Adjuvants in the Peripheral Nervous System ссылка

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург