ВК СЛОЖНОГО СЛУЧАЯ, г. Санкт-Петербург.
Продолжение. Начало в № 1/2026
В статье приведен анализ сведений о применении ESP-блокады в торакальной хирургии, а также указаны экспериментальные данные, полученные при использовании данной блокады в практике автора статьи.
ESP-блокада в торакальной хирургии: опыт применения
Оперативные вмешательства на грудной клетке характеризуются высоким уровнем интенсивности болевого синдрома. У собак и кошек после торакальных вмешательств уровень болевого синдрома при недостаточной анальгезии может варьироваться от умеренного до сильного и изнуряющего в первые 24–72 часа и более после операции11,12. Для обеспечения адекватной анальгезии рекомендуется применять системные анальгетики (опиоиды, блокаторы NMDA-рецепторов и др.) в комбинации с методами регионарной анестезии в рамках мультимодального подхода.С учетом сложностей в использовании наркотических препаратов в РФ, связанных с необходимостью наличия лицензии для их применения и их доступностью, ESP-блокада представляет собой перспективный вариант регионарной анестезии в торакальной хирургии, включая случаи, требующие продленной анальгезии.
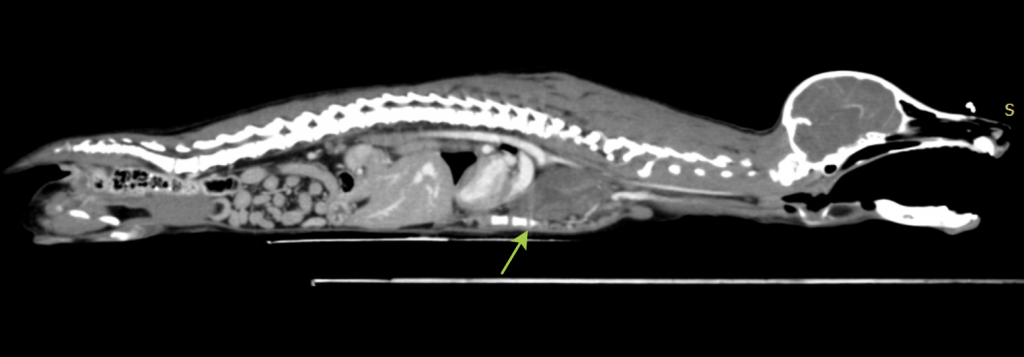
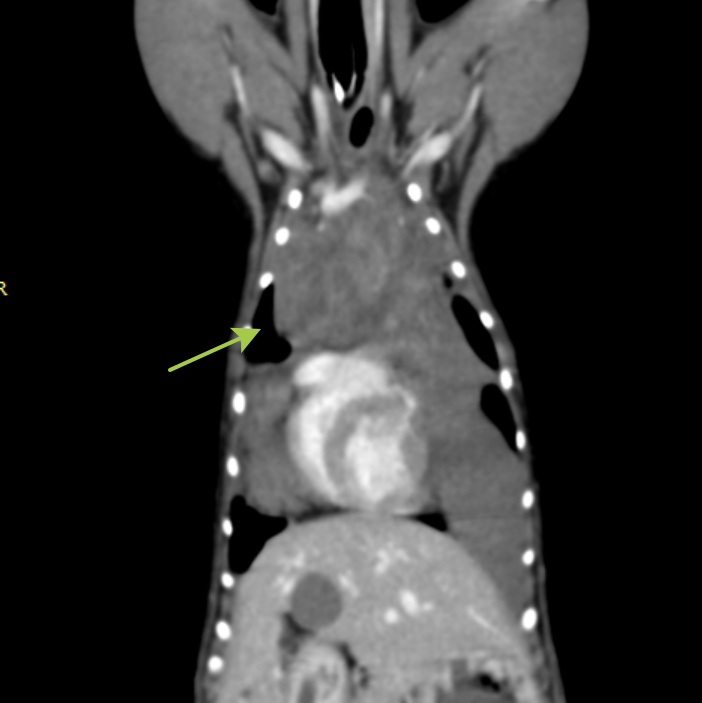
В период с октября 2024 г. по март 2025 г. в Ветеринарной клинике доктора Сотникова было выполнено 28 оперативных вмешательств на грудной клетке у 26 животных (15 собак и 11 кошек), при проведении которых в анестезиологический протокол было включено использование ESP-блокады в составе мультимодальной анальгезии. Операции включали стернальные и паракостальные торакотомии, выполненные с целью удаления новообразований органов грудной полости, хирургическое лечение спонтанного гемоторакса (рис. 8, 9) и буллезной эмфиземы легких, торакоскопию с целью лигирования грудного лимфатического протока, а также хирургическое лечение травм грудной клетки, вызванных укушенными ранами, и постановку торакальных дренажей при гидро- и пневмотораксе. У двух из 26 пациентов (1 собака и 1 кошка) потребовалось повторное оперативное вмешательство из-за пневмоторакса, вызванного несостоятельностью культи бронха после удаления доли легкого и необходимостью удаления абсцесса доли легкого, который возник спустя двое суток после постановки торакальных дренажей по причине пиоторакса. Возраст пациентов варьировался от 4 месяцев до 14 лет, а вес – от 2 до 50 кг. Все пациенты относились к IV–V классам по шкале ASA (англ. American Society of Anesthesiologists), что указывает на высокую вероятность возникновения осложнений во время проведения анестезии и в ранний постоперационный период.
Во время проведения оперативных вмешательств осуществлялся мониторинг основных показателей жизнедеятельности пациентов (ЭКГ, капнография, пульсоксиметрия, термометрия, НИАД/ИАД). Для этого использовались мониторы Mindray, тонометры Petmap и Contec. ESP-блокада выполнялась с применением одноразовых спинальных игл под УЗ-навигаций с помощью аппарата SonoScape ST-190, оснащенного линейным и конвексным датчиками для визуализации костных структур и мышц, а также для контроля распределения анестетика в межфасциальном пространстве.
Всем пациентам была выполнена индукция с использованием пропофола в дозировке 2–5 мг/кг, четырем пациентам – в комбинации с кетамином в дозе 1 мг/кг. Поддержание анестезии осуществлялось с применением ингаляционных анестетиков (изофлуран/севофлуран в концентрации 1,0–3,0 об.%).
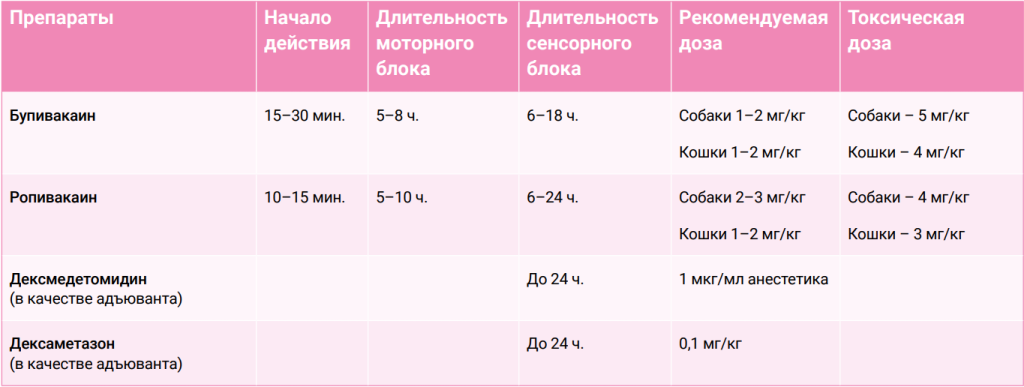
Для регионарной анестезии использовалась ESP-блокада с применением местных анестетиков длительного действия (ропивакаин/бупивакаин) в комбинации с адъювантами (дексаметазон/дексмедетомидин). При проведении торакотомий со стернальным доступом и установкой торакальных дренажей блокада выполнялась с обеих сторон. В случае паракостальных торакотомий блокада выполнялась только с той стороны, где осуществлялся хирургический доступ. У пациентов с травмами грудной клетки, вызванными укушенными ранами, инъекции проводились с одной или обеих сторон в зависимости от локализации повреждений. Точки введения анестетика варьировались в зависимости от типа хирургического вмешательства – инъекции выполнялись в области Th5, Th6 и Th7. Для проведения блокады использовались максимальные безопасные дозы местных анестетиков и адъювантов, концентрация растворов зависела от объема, необходимого для проведения блокады (0,4–0,5 мл/кг на одну точку). Интраоперационно большинству пациентов проводилась дополнительное введение опиоидов в минимальных дозировках: морфин – 0,2 мг/кг и фентанил – ИПС 2–3 мкг/кг/ч (в большинстве случаев без предварительного болюсного введения). Пациентам, которым требовалась установка торакальных дренажей, ESP-блокада интраоперационно использовалась в монорежиме. Примечательно, что двум из четырех пациентов, которым проводилась стернальная торакотомия с целью удаления новообразования тимуса, дополнительное введение опиоидов как интраоперационно, так и в послеоперационном периоде не потребовалось (планировалось введение фентанила в виде болюсов в качестве экстренной анальгезии при необходимости).
Для анальгезии в послеоперационном периоде в большинстве случаев применялся мелоксикам. Пациентам с противопоказаниями или ограничениями к использованию НПВП вводили ингибиторы ЦОГ-3 (метамизол натрия, парацетамол). 10 (из 11) пациентам, перенесшим паракостальную торакотомию, была произведена постановка инфильтрационных катетеров в области хирургического доступа, которые использовались для введения местных анестетиков в послеоперационном периоде. Интенсивность болевого синдрома в раннем послеоперационном периоде оценивалась с применением визуальной аналоговой шкалы боли (ВАШ) на протяжении всего периода пребывания пациентов в отделении реанимации и интенсивной терапии. У 22 из 26 пациентов (84,6%) болевой синдром оценивался в диапазоне 0–1 балл по ВАШ, опиоиды в ранний постоперационный период не применялись. Двум пациентам (7,7%) после хирургического лечения травм грудной клетки и стернальной торакотомии с целью удаления объемного новообразования легкого в первые 36 часов после операции потребовалась дополнительная анальгезия. Для анальгезии в вышеупомянутых случаях использовался трамадол в комбинации с НПВП, поскольку интенсивность боли достигла 2–3 баллов по ВАШ. Двум пациентам (7,7%), перенесшим стернальную торакотомию, была произведена постановка катетеров для продленной анальгезии в межфасциальное пространство между фасцией ESP и поперечными отростками грудных позвонков. У одного из этих пациентов анальгезия осуществлялась исключительно с использованием вышеупомянутых катетеров в монорежиме, при этом интенсивность болевого синдрома по ВАШ оценивалась в диапазоне от 0 до 1 балла; беспокойство, дрожь и реакция на пальпацию в области доступа наблюдались по окончании действия анестетика за 20–30 минут до расчетного времени следующего введения (видео 1).
Видео 1. Пациент спустя один час после стернальной торакотомии по причине спонтанного гемоторакса (произведено удаление тимуса и обширной гематомы в области средостения).
Во время проведения 24 из 28 хирургических вмешательств (85,7% случаев) после выполнения блокады у пациентов наблюдалась умеренная гипотензия, не требующая коррекции (отмечалось снижение артериального давления на 5–15% от исходных значений).
В 5 случаях (17,8% случаев) наблюдалась гипотермия легкой и умеренной степени тяжести (снижение температуры тела с 36,5 до 35,2 °C к моменту завершения операции). Степень гипотермии не зависела от видовых, породных, возрастных характеристик животных и продолжительности оперативного вмешательства. Во всех случаях применялись активные и пассивные методы обогрева: водные грелки, пледы, направленный поток теплого воздуха (фен) и локальное укутывание конечностей (носки).
5 из 26 пациентов погибли в период от 8 до 96 часов после операции по причинам, не связанным с анестезией (тромбоз сосудов легких и легочных артерий, напряженный пневмоторакс, септический шок и эвтаназия вследствие прогрессирования буллезной эмфиземы легких).
У одного из пациентов развился неамбулаторный парапарез тазовых конечностей после односторонней ESP-блокады с использованием бупивакаина. При проведении МР-томографии грудопоясничного отдела позвоночника у данного пациента патологий спинного мозга, его оболочек и корешков не было выявлено, однако были обнаружены дегенеративные изменения межпозвоночных дисков на уровне Th13-L2. Неврологический дефицит полностью разрешился в течение 36 часов после операции, что, вероятно, связано с попаданием местного анестетика в эпидуральное пространство.
ESP-блокада: особенности применения в торакальной хирургии
ESP-блокада может быть выполнена под УЗ-контролем или по методу анатомических ориентиров, однако предпочтение отдается ультразвуковой навигации, так как с её помощью можно визуализировать костные структуры, мышцы и контролировать распределение анестетика в межфасциальном пространстве. Раствор местного анестетика вводится в пространство между мышцами группы ESP и поперечными отростками грудных позвонков2,3.Место введения зависит от области оперативного вмешательства:
- Стернальная торакотомия – Th5 с двух сторон. Грудина иннервируется за счет вентральных ветвей межреберных нервов Th1-Th81,4. С учетом того, что после введения анестетик распространяется в краниальном и каудальном направлениях, воздействуя на ветви спинномозговых нервов 3–7 близлежащих сегментов позвоночного столба, введение анестетика в данном сегменте, по мнению автора, является предпочтительным.
- Паракостальная торакотомия – Th5-Th6 со стороны доступа.
- Постановка торакальных дренажей – Th7-Th8 со стороны доступа.
- Травмы в области грудной клетки – место введения определяется в зависимости от локализации повреждений с учетом предполагаемой площади распределения анестетика в межфасциальном пространстве.
Осложнения, описанные при выполнении ESP-блокады в грудном отделе позвоночника:
- Пневмоторакс и травматизация легких. При некорректной технике выполнения ESP-блокады существует риск пункции плевры и проникновения иглы в плевральную (грудную) полость, что может привести к травматизации легочной ткани и развитию ятрогенного пневмоторакса. Минимизация рисков возникновения данного осложнения достигается строгим соблюдением всех правил техники выполнения блокады2,3.
- Внутрисосудистое введение анестетика. Местные анестетики обладают кардиотоксическим действием и при введении в сосуд могут вызывать нарушения гемодинамики, которые проявляются нарушениями ритма (тахикардия, брадикардия, вплоть до асистолии, желудочковые нарушения ритма, переходящие в фибрилляцию желудочков), а также сердечно-сосудистый коллапс вследствие нарушения сократительной функции миокарда. Для предотвращения этих осложнений перед введением анестетика проводится аспирационная проба: при обнаружении крови в игле введение препарата прекращают и пункция выполняется заново2,3.
- Гипотензия. Несмотря на то что при проведении межфасциальных блокад местные анестетики оказывают меньшее влияние на тонус симпатической нервной системы по сравнению, например, с эпидуральным введением, локальная вазодилатация, вызванная воздействием анестетиков на близлежащие сосудистые структуры, может привести к гипотензии9. В большинстве случаев снижение АД после проведения ESP-блокады не является клинически значимым и составляет 5–15% от исходных показателей, что не требует коррекции с использованием вазоактивных препаратов. Однако у пациентов с водно-электролитными нарушениями или сниженным сосудистым сопротивлением гипотензия может быть более выраженной и требует коррекции.
- Передозировка и токсические эффекты местных анестетиков. При использовании местных анестетиков важно строго соблюдать максимальную рекомендованную дозу, рассчитанную исходя из идеальной массы тела пациента. Превышение рекомендуемой дозировки может привести к развитию системных побочных эффектов, таких как судороги, кома, гипотензия и сердечно-сосудистый коллапс. Для увеличения объема местного анестетика допустимо добавление физиологического раствора или воды для инъекций2,3.
- Неврологический дефицит. После проведения ESP-блокады у пациентов может наблюдаться монопарез или парапарез конечностей, обусловленный проникновением местного анестетика в эпидуральное/паравертебральное пространство. Как правило, данный симптом не требует специфического лечения и проходит самостоятельно после окончания моторного блока анестетика. Однако в некоторых случаях неврологический дефицит может сохраняться до 24–36 часов после проведения блокады9,3.
- Брадикардия и брадиаритмии. Согласно литературным данным, у пациентов после проведения ESP-блокады может наблюдаться синусовая брадикардия, АВ-блокада II степени, остановка синусового узла (идиовентрикулярный ритм). Брадиаритмии возникают в 5.4% случаев и требуют коррекции в ситуациях, когда они оказывают влияние на гемодинамику. Для этого используются М-холинолитики, адреномиметики и жировые эмульсии при подозрении на системную токсичность местных анестетиков.9.
- Гипотермия. После проведения ESP-блокады наблюдается периферическая вазодилатация, которая способствует увеличению потери тепла и может привести к значительной гипотермии, особенно при двусторонней инъекции. По литературным данным, частота гипотермии на 18,1% выше у пациентов, которым была проведена ESP-блокада, по сравнению с пациентами, у которых регионарная анестезия не проводилась при идентичных оперативных вмешательствах9.
Заключение
На основании экспериментальных и клинических данных можно сделать вывод о том, что ESP-блокада является эффективным методом анальгезии при торакальных операциях у кошек и собак. Использование этой блокады в составе мультимодальной анальгезии является более предпочтительным.При выполнении ESP-блокады могут развиться осложнения, однако большинство из них легко купируются и профилактируются при строгом соблюдении техники выполнения блокады. С учетом простоты техники и доступности метода эта блокада является перспективным вариантом регионарной анестезии, который может эффективно использоваться в торакальной хирургии, включая случаи, требующие продленной анальгезии.
Благодарность
Автор выражает искреннюю благодарность коллегам-врачам Дьяченко И.А., Сыропятовой М.Н. и Нестеровой С.В. за помощь в проведении исследований и подготовке данной статьи.
Список литературы:
- IMAIOS vet-anatomy. The Anatomy for veterinary imaging. https://doi.org/10.37019/vet-anatomy
- Matt Read, Luis Campoy, Berit Fischer. Small animal regional anaesthesia. 2nd edition, 2024.
- Pablo E. Otero, Diego A. Portela. Manual of small animal regional anesthesia: illustrated anatomy of nerve stimulation and ultrasound-guided nerve block. 2nd edition, 2018.
- Miller’s anatomy of the dog: fourth edition. ISBN: 978-143770812-7 Copyright © 2013, 1993, 1979, 1964 by Saunders, an imprint of Elsevier Inc.
- M.E. Herrera-Linares, Rocío Fernández-Parra , et al. Cadaveric study of the ultrasound-guided erector spinae plane block over the transverse process of the twelfth thoracic vertebra in dogs: Transversal vs longitudinal approach, 2024. https://doi.org/10.1016/j.tvjl.2024.106094
- Felipe Munoz-Leyva, Ki Jinn Chin, Wilman E. Mendiola, et al. Bonilla. Bilateral continuous erector spinae plane (ESP) blockade for perioperative opioid-sparing in median sternotomy: a case series // Journal of Cardiothoracic and Vascular Anesthesia, 2018.
- Стукалов А.В., Лахин Р.Е., Ершов Е.Н.. Клинический случай применения ESP-блока в торакальной хирургии // Регионарная анестезия и лечение острой боли, 2021. DOI:10.17816/1993-6508-2021-15-1-57-62
- Sanjib Das Adhikary, Stephanie Bernard, Hector Lopez, Ki Jinn Chin. Erector Spinae Plane Block Versus Retrolaminar Block: A Magnetic Resonance Imaging and Anatomical Study // Regional anaesthesia and acute pain, 2018. DOI: 10.1097/AAP.0000000000000798
- Inga Viilmann, Maja Drozdzynska, Enzo Vettorato. Analgesic efficacy of a bilateral erector spinae plane block versus a fentanyl constant rate infusion in dogs undergoing hemilaminectomy: a retrospective cohort study, 2022. https://doi.org/10.1186/s12917-022-03523-x
- E. Vidal, H. Giméneza, M. Foreroy, M. Fajardo. Bloqueo del plano del músculo erector espinal: studio anatómico-cadavérico para determinar su mecanismo de acción, 2018. https://doi.org/10.1016/j.redar.2018.07.004
- WSAVA Global Pain Council members and co-authors. Guidelines for recognition, assessment and treatment of pain // Journal of Small Animal Practice, 2014. DOI: 10.1111/jsap.12200
- Gaynor, J. S., Muir, W. W. Handbook of Veterinary Pain Management: 3rd ed. 2015.
- Закирова О. В. Адъюванты в регионарной анестезии // Журнал «Ветеринарный Петербург», № 4, 2023.
- Pablo E Otero, Santiago E Fuensalida, et al. Mechanism of action of the erector spinae plane block: distribution of dye in a porcine model, 2020. DOI 10.1136/rapm-2019-100964
- Холл, Дж. Э. Медицинская физиология по Гайтону и Холлу / Джон Э. Холл, Майкл Э. Холл; пер.с англ. под ред Е. В. Никениной. 3-е изд., испр. и доп. – М.: Логосфера, 2024. – 1344 с.
- Hiroo Suami, Akira Shinaoka. The methodology of lymphatic anatomy studies in a cadaver model: an overview. 2019. DOI: 10.20517/2347-9264.2019.46 https://doi.org/10.20517/2347-9264.2019.46
- Hiroo Suami, G. Ian Taylor, A.O., Wei-Ren Pan. A New Radiographic Cadaver Injection Technique for Investigating the Lymphatic System // 2005. DOI: 10.1097/01.prs.0000163325.06437.b0

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург