Носаченко А.О.1, заведующая анестезиологическим отделением, ветеринарный врач-анестезиолог;
Абызова М.В.1, заведующая кардиологическим отделением, главный ветеринарный врач филиала «Коньково»;
Александрова Ю. А.,2 к.б.н., старший научный сотрудник департамента науки; aleksandrova.y@vetmag.ru.
1Ветеринарная клиника «ВЕДА» (г. Москва).
2ООО «НВЦ Агроветзащита» (г. Москва).
Ключевые слова: переносимость, безопасность, средства для наркоза, изофлуран, кошки, собаки.
Список сокращений:
АД – артериальное давление;
АЛТ – аланинаминотрансфераза;
АСТ – аспартатаминотрансфераза;
ГАМК – гамма-аминомасляная кислота;
М – среднее значение;
m – стандартная ошибка среднего;
EtCO2 – концентрация углекислого газа в конце выдоха ( End-tidal CO2);
SpO2 – сатурация кислорода артериальной крови (Peripheral Oxygen Saturation);
ЧДД – частота дыхательных движений;
ЧСС – частота сердечных сокращений.
Введение
Ингаляционный наркоз представляет собой метод общей анестезии, при котором летучие или газообразные анестетики поступают в организм животного через дыхательные пути, вызывая комплекс фармакологических эффектов, включающий потерю сознания (наркотический сон) и миорелаксацию3,5,10. Его механизм основан на проникновении молекул анестетика через альвеолярно-капиллярную мембрану в кровоток с последующей доставкой к центральной нервной системе. Важным преимуществом метода является контроль глубины анестезии за счет регулирования концентрации анестетика во вдыхаемой смеси6.Широко применяемым в ветеринарной практике препаратом для данного вида наркоза является «Изофлуран». Как и большинство летучих анестетиков, он представляет собой галогенированное эфирное соединение, являющееся структурным изомером энфлурана2,4,9.
Несмотря на то, что он был синтезирован в 1965 году, его использование в ветеринарной практике в России началось лишь с 1997 года. На сегодняшний день «Изофлуран» широко применяется в качестве препарата первого выбора для ингаляционной анестезии у животных.
Компанией ООО «АВЗ С-П» (Россия) выпускается отечественный лекарственный препарат для ветеринарного применения «Изофлуран», относящийся к фармакотерапевтической группе «средства для наркоза». В качестве действующего вещества в 1 г содержится 1000 мг изофлурана, вспомогательные вещества отсутствуют.
По внешнему виду лекарственный препарат представляет собой прозрачную бесцветную летучую жидкость с характерным запахом.
Изофлуран, входящий в состав лекарственного препарата, являясь ингибитором рецепторов глицина и рецепторов гамма-аминомасляной кислоты (ГАМК) в центральной нервной системе, вызывает быстрое наступление общей анестезии и быстрый выход из нее.
Изофлуран постсинаптически усиливает ингибирующую синаптическую передачу, потенцируя лиганд-управляемые ионные каналы, активированные ГАМК и глицином, также действует экстрасинаптически, активируя ГАМК-рецепторы и трансмембранные ионные токи, и пресинаптически, усиливая базальное высвобождение ГАМК.
Изофлуран вызывает быстрое наступление общей анестезии, ослабление глоточных и гортанных рефлексов, умеренную миорелаксацию7.
Препарат «Изофлуран» по степени воздействия на организм относится к веществам умеренно опасным (третий класс опасности по ГОСТ 12.1.007-76).
Цель исследования: изучить безопасность и переносимость препарата «Изофлуран» при ингаляционной анестезии собак и кошек в клинических условиях.
Материалы и методы
Исследования выполнялись согласно Приказу Министерства сельского хозяйства РФ от 6 марта 2018 г. № 101 «Об утверждении правил проведения доклинического исследования лекарственного средства для ветеринарного применения, клинического исследования лекарственного препарата для ветеринарного применения, исследования биоэквивалентности лекарственного препарата для ветеринарного применения», а также в соответствии с правилами, принятыми Европейской Конвенцией по защите позвоночных животных, используемых для экспериментальных и иных научных целей (European Convention for the Protection of Vertebrate Animals Used for Experimental and other Scientific Purposes (ETS 123), Strasbourg, 1986)1-8.Статистическую обработку данных проводили с использованием программного обеспечения Microsoft Excel 2013, PKSolver и Statistica. Данные представлены в виде среднего значения и стандартной ошибки среднего (M ± m).
Исследования проводили на базе ветеринарной клиники «ВЕДА» (г. Москва). В исследовании участвовали 12 клинически здоровых животных: 6 кошек (беспородные метисы) в возрасте от 1,5 до 8 лет с массой тела 2,7–4,4 кг и 6 собак (породы бигль) в возрасте от 1,3 до 3 лет с массой тела 14,5–19 кг. Животные принадлежали Центру содержания животных ООО «СВС-Н».
После клинического обследования, включавшего эхокардиографию, общий и биохимический анализы крови, животным проводили индукцию препаратом «Пропофол» в соответствии с инструкцией. После индукции и наступления миорелаксации выполняли эндотрахеальную интубацию.
Ингаляционная анестезия поддерживалась с использованием наркозно-дыхательного аппарата Mindray. Препарат «Изофлуран» применяли в максимальных терапевтических дозах в смеси с кислородом:
Кошки: вводная анестезия – 2,0% в течение 3–5 минут, поддерживающая анестезия –
1,0-2,0% в течение 120 минут.
Собаки: вводная анестезия – 2,5% в течение 3–5 минут, поддерживающая анестезия –
1,5-2,0% в течение 120 минут.
За 3 минуты до завершения процедуры подача изофлурана прекращалась и осуществлялась ингаляция чистым кислородом для вывода из наркоза.
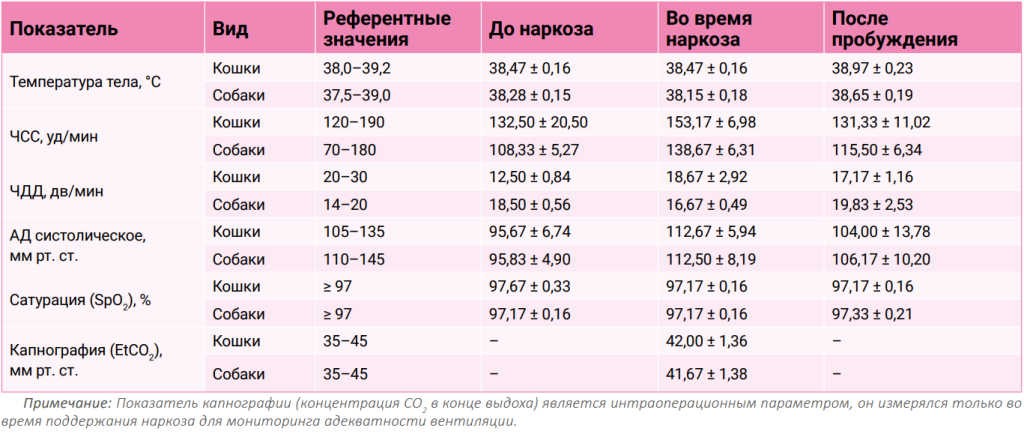
Для контроля состояния животных проводили непрерывный мониторинг (фото 1) с последующим сравнительным анализом данных в три этапа: до наркоза, во время и после пробуждения. Оценка включала физиологические показатели (температура тела, ЧСС, ЧДД, артериальное давление, сатурация и капнография), проведение лабораторных исследований (общий клинический и биохимический анализы крови) и инструментальную диагностику с помощью эхокардиографии до и после анестезии для оценки функционального состояния сердечно-сосудистой системы.
Результаты и обсуждение
Мониторинг основных физиологических параметров не выявил статистически значимых отклонений от референтных значений ни у кошек, ни у собак на всех этапах исследования. Как видно из таблицы 1, показатели температуры тела, ЧСС, ЧДД, артериального давления, сатурации и капнографии оставались в пределах физиологической нормы. Это свидетельствует о стабильности гемодинамики и функции внешнего дыхания под действием препарата. Небольшие колебания, такие как незначительное увеличение ЧСС у собак во время наркоза, являются типичной адаптивной реакцией на ингаляционные анестетики и не расцениваются как негативный эффект.Мониторинг основных физиологических параметров не выявил статистически значимых отклонений от референтных значений ни у кошек, ни у собак на всех этапах исследования. Отмечаемое у кошек до наркоза снижение частоты дыхательных движений (ЧДД) является физиологической нормой для животных в состоянии покоя и спокойствия и, вероятно, связано с эффектом индукции препаратом «Пропофол». Как видно из таблицы 1, показатели температуры тела, ЧСС, ЧДД оставались стабильными во время анестезии.
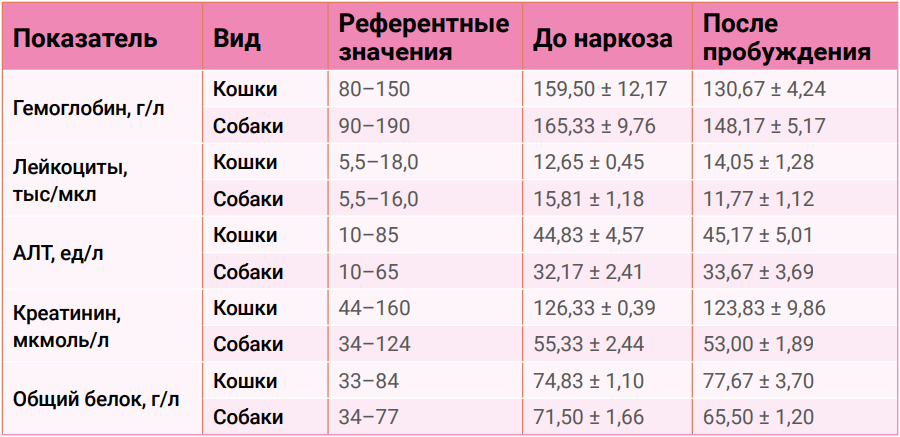
Результаты общего клинического и биохимического анализов крови, проведенных до введения в наркоз и после полного пробуждения животных, не показали клинически значимых изменений. Ключевые гематологические и биохимические параметры оставались стабильными, как показано в таблице 2.
Отсутствие признаков гепатотоксичности (нормальные уровни АЛТ, АСТ) или нефротоксичности (уровни мочевины и креатинина в норме) согласуется с данными литературы о высоком индексе безопасности изофлурана.
Как видно из таблицы 2, ключевые биохимические и гематологические показатели оставались стабильными. Следует отметить, что исходный уровень гемоглобина до наркоза у части животных находился выше референтных значений, что могло быть связано с индивидуальными особенностями или легким обезвоживанием на фоне стрессового состояния, вызванного транспортировкой. Важно, что после анестезии наблюдалась тенденция к нормализации данного показателя, а его динамика не носила патологического характера, что исключает негативное влияние изофлурана на систему крови.
Эхокардиографическое исследование, проведенное до и после анестезии, не выявило значимых изменений в геометрии камер сердца, систолической и диастолической функции миокарда как у кошек, так и у собак. Не было зафиксировано признаков легочной гипертензии, застойных явлений или изменений в клапанном аппарате. Эти данные подтверждают, что препарат «Изофлуран» не обладает кардиодепрессивным действием в применяемых дозах.
Препарат обеспечил быстрое и гладкое введение в состояние хирургической стадии наркоза с развитием умеренной миорелаксации. Время полного пробуждения животных после прекращения подачи изофлурана составило в среднем 20–30 минут для кошек и 10–15 минут для собак, что характеризует его как средство с быстрым выходом из анестезии. Побочных явлений зарегистрировано не было. При использовании Изофлурана необходимо проводить мониторинг физиологических показателей животных для контроля их состояния при ингаляционном наркозе.
Заключение
Результаты проведенного исследования свидетельствуют о благоприятном профиле переносимости и высокой безопасности лекарственного препарата «Изофлуран» (производства ООО «АВЗ С-П», Россия) при ингаляционной анестезии у собак и кошек.Применение препарата в максимальных терапевтических дозах обеспечивало управляемую анестезию с быстрым пробуждением и не сопровождалось клинически значимыми отклонениями в показателях гемодинамики, функции внешнего дыхания, газового состава крови, а также в результатах лабораторных и эхокардиографических исследований.
Таким образом, отечественный препарат «Изофлуран» продемонстрировал надежность и безопасность, соответствующие современным требованиям к ингаляционным анестетикам, и может быть рекомендован для широкого использования в ветеринарной практике.
Список литературы:
- Об утверждении правил проведения доклинического исследования лекарственного средства для ветеринарного применения, клинического исследования лекарственного препарата для ветеринарного применения, исследования биоэквивалентности лекарственного препарата для ветеринарного применения: Приказ Минсельхоза России от 06.03.2018 № 101 (ред. от 09.12.2020). – URL: ссылка
- Акчурин С. В. Основные лекарственные средства для кошек и собак в российской ветеринарной практике / С. В. Акчурин [и др.] // Известия Тимирязевской сельскохозяйственной академии. – 2023. – № 2. – С. 109–123.
- Гавриленко И. В. Применение ингаляционного наркоза в ветеринарии / И. В. Гавриленко. – М., 2022. – 32 с. – ББК 72.4 я43 М75.
- Лихванцев В. В. Механизмы действия и основные эффекты галогенсодержащих анестетиков / В. В. Лихванцев [и др.] // Вестник интенсивной терапии им. А.И. Салтанова. – 2013. – № 3. – С. 44–51.
- Сидорова К. А. Физиологическое обоснование ингаляционной анестезии животных / К. А. Сидорова [и др.] // Научная жизнь. – 2018. – № 12. – С. 189–196.
- Caulkett N. Inhalational Anesthetic Drugs / N. Caulkett, D. Pang // Fundamental Principles of Veterinary Anesthesia. – 2024. – P. 131–148.
- Eger E. I. The pharmacology of isoflurane / E. I. Eger 2nd // British Journal of Anaesthesia. – 1984. – Vol. 56. – P. 71S–99S.
- European Convention for the Protection of Vertebrate Animals Used for Experimental and other Scientific Purposes. – Strasbourg, 18.03.1986. – URL: ссылка
- Hawkley T. F. Isoflurane / T. F. Hawkley, M. Preston, C. V. Maani // StatPearls. – 2018. – URL: ссылка
- Steffey E. P. Inhalation anesthetics / E. P. Steffey, R. J. Brosnan, K. R. Mama // Veterinary Anesthesia and Analgesia: The Sixth Edition of Lumb and Jones. – 2024. – P. 489–525.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург