Введение
Портосистемные шунты – аномалии сосудов брюшной полости, при которых часть крови или вся кровь из системы воротной вены, минуя печень, попадает в основное кровеносное русло.У здорового животного воротная вена отводит кровь от желудка, тонкой и толстой кишок (исключая каудальный отдел прямой кишки) и селезенки в печень (фото 1). В печени эта кровь, содержащая продукты распада белков, подвергается детоксикации.
У животного с портосистемным шунтом кровь из воротной вены сбрасывается в общее венозное русло, не пройдя детоксикацию в печени. Продукты расщепления белков и питательных веществ, попадающие из желудочно-кишечного тракта в общее кровеносное русло, обуславливают развитие клинической картины.
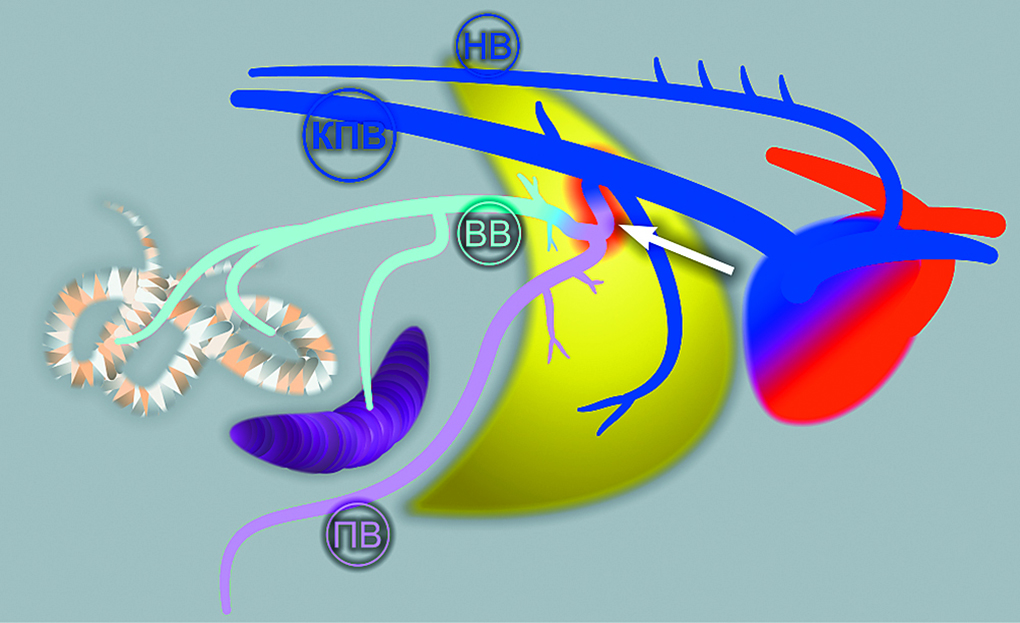
НВ – непарная вена, КПВ – каудальная полая вена, ВВ – воротная вена, ПВ – пупочная вена.
Клинические признаки
К общим клиническим проявлениям относят потерю веса, отставание в росте, плохое качество шерсти, понижение температуры тела, слюнотечение, рвоту.Помимо этого, может развиться гепатоэнцефалопатия, поражающая практически все отделы головного мозга, что проявляется вялостью, угнетением, нарушением координации, судорожными приступами, в тяжелых случаях может развиться кома. Выраженность гепатоэнцефалопатии зависит от содержания белка в пище. При переходе на низкобелковую диету состояние пациентов улучшается.
Классификация
Портосистемные шунты могут быть врожденными или приобретенными. Врожденные шунты рассматривают как сохранившиеся после рождения эмбриональные анастомозы (фото 2), являющиеся нормой для плода на той или иной стадии внутриутробного развития.Приобретенные шунты – это реакция организма на портальную гипертензию. Повышение давления в воротной вене может развиться вследствие цирроза, фиброза и других заболеваний печени, приводящих к изменению сосудистого русла паренхимы. Предполагается, что шунт при этом может развиться из нормального для эмбриона анастомоза, существовавшего у плода, но запустевшего до или после рождения.
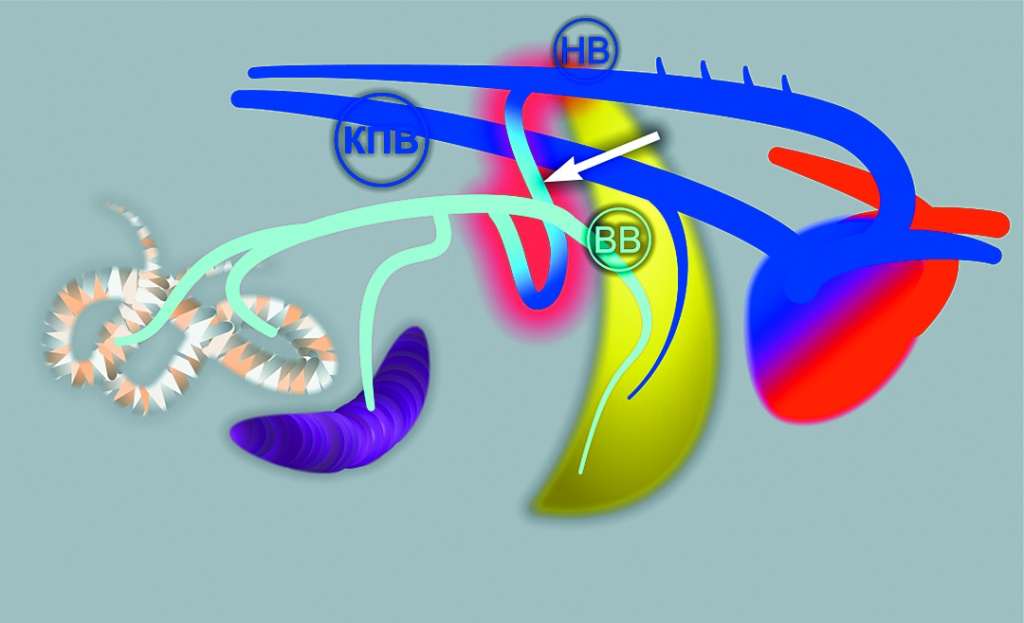
Если сосуд, шунтирующий печеночный кровоток, расположен внутри печени, его называют внутрипеченочным (фото 3), если за пределами печени – внепеченочным (фото 4).
Шунты могут быть одиночными, двойными и множественными.
Помимо открытого венозного протока и портокавального шунта, то есть анастомоза между воротной веной и каудальной полой веной, встречаются и другие топологические варианты шунтов. Шунты могут брать начало от воротной, селезеночной или желудочной вены, а сбрасывать кровь – в каудальную полую, непарную или диафрагмальную вену.
НВ – непарная вена, КПВ – каудальная полая вена, ВВ – воротная вена, ПВ – пупочная вена.
Породные предрасположенности
Внепеченочные портосистемные шунты чаще встречаются у чистопородных собак мелких пород: чихуахуа, лхасских апсо, ши-тцу, мальтийских болонок, различных мелких терьеров, миниатюрных шнауцеров и такс. Внутрипеченочные шунты обычно поражают собак крупных и средних пород: австралийских пастушьих собак, ирландских волкодавов, лабрадоров, немецких овчарок.Среди кошек наиболее часто портосистемные шунты встречаются у гималайской, домашней короткошерстной, персидской и сиамской пород. Как правило, у кошек выявляют внепеченочные шунты.
Лабораторные исследования
Биохимический анализ крови:- Гипоальбуминемия и пониженное содержание в крови общего белка.
- Низкая концентрация азота мочевины в крови.
- Низкие уровни холестерина и глюкозы в крови.
- Повышенная концентрация печеночных ферментов.
- Увеличение уровня аммиака в крови в периоды между приемами корма.
- Резкое повышение в сыворотке желчных кислот (тест проводится до и после кормления).
- У 72% собак выявляют микроцитоз с сопутствующей анемией или без нее.
- Может наблюдаться лейкоцитоз.
- Общий анализ мочи:
- Снижается плотность мочи.
- Могут быть признаки цистита.
- Наличие уратов в моче у молодого животного является показанием для проведения дальнейших исследований.
- Позволяет выявить причины, приведшие к образованию приобретенных шунтов, микроваскулярную дисплазию и другие патологии, которые не всегда удается обнаружить другими методами.
Визуальная диагностика
Клинические признаки и лабораторные исследования позволяют предположить наличие шунта. Подтвердить диагноз и оценить топологию сосудов помогают методы визуальной диагностики.Ультразвуковое исследование
Печень имеет малые размеры. Вены печени очень малы или совсем неразличимы. В почках и мочевом пузыре обнаруживаются кристаллы уратов аммония.Внутрипеченочные шунты визуализируются проще (фото 5), внепеченочные – сложнее. Допплерография позволяет обнаружить турбулентные потоки в полой и воротной венах, которые обычно возникают в области шунта.
Вероятность выявления портосистемных шунтов у животных с помощью ультразвукового сканирования варьируется в широких пределах и во многом определяется уровнем подготовки и опытом проводящего исследование специалиста.
КПВ – каудальная полая вена, ВВ – воротная вена, Ш – шунт.
Рентгенографические исследования
На обзорных рентгенограммах брюшной полости выявляют уменьшение размеров тени печени. Для визуализации границ желудка перед рентгенографией животному выпаивают водную взвесь сульфата бария. На обзорных рентгенограммах можно обнаружить тени рентгеноконтрастных камней в почках и мочевом пузыре. Кристаллы урата аммония не рентгеноконтрастны, но нередко при портосистемных шунтах образуются камни более сложного состава, являющиеся рентгеноконтрастными.
Для визуализации сосудов применяют ангиографию – введение рентгеноконтрастного препарата в кровеносные сосуды. Ангиография может быть неселективной (общей) и селективной (избирательной). При неселективной ангиографии рентгеноконтрастный препарат вводится через периферический сосуд в общее кровеносное русло. При селективной – рентгеноконтрастный препарат вводится в интересующий сосуд.
рентгеноконтрастного вещества в брыжеечную вену – норма.
Избирательное контрастирование воротной вены называют портографией. Существует несколько способов введения контрастного препарата в воротную вену.
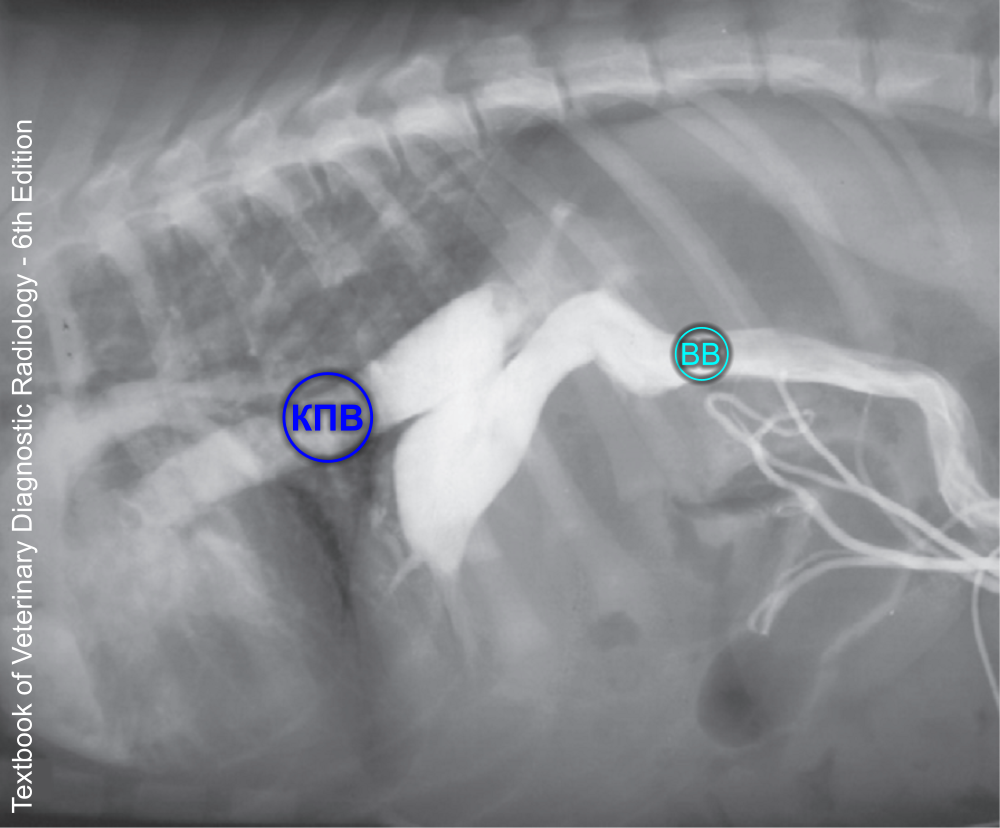
Портография с введением рентгеноконтрастного вещества в брыжеечную вену в настоящий момент является «золотым стандартом» в диагностике портосистемных шунтов. Это инвазивный метод. Животному под общим наркозом делают лапаротомию, катетеризируют брыжеечную вену, выводят магистраль от катетера за пределы брюшной полости. Далее через магистраль вводят рентгеноконтрастный препарат, который по брыжеечной вене попадает в воротную вену, и сразу же делают серию рентгенограмм (фото 6). Этот метод позволяет визуализировать воротную вену, шунт (фото 7) и сосуды печени.
ВВ – воротная вена.
КПВ – каудальная полая вена, ВВ – воротная вена.
Портография с введением рентгеноконтрастного вещества в паренхиму селезенки – менее инвазивный метод. Пункция селезенки проводится без лапаротомии, через брюшную стенку под контролем УЗИ. В паренхиму селезенки вводится рентгеноконтрастный препарат, который поступает в селезеночную вену, а из нее – в воротную вену. Делается серия рентгенограмм. Этот путь введения позволяет визуализировать те шунты, которые берут начало от селезеночной вены и от воротной вены после впадения в нее селезеночной вены.
При портографии с введением рентгеноконтрастного препарата в краниальную брыжеечную артерию не нужна лапаротомия, но требуется катетеризация бедренной артерии, по которой катетер под рентгенографическим контролем продвигается по брюшной аорте до краниальной брыжеечной артерии. Вводится контрастный препарат, который по брыжеечной артерии уходит в капилляры кишечника, а оттуда – в вены брыжейки и воротную вену.
Неселективная ангиография воротной вены неприменима при рентгенографии потому, что из-за большого количества близко расположенных в брюшной полости сосудов и контрастирования введенным препаратом петель кишечника и паренхиматозных органов невозможно интерпретировать полученное изображение.
Сцинтиграфия
Метод функциональной визуализации, заключающийся в том, что исследуемому животному вводят (ректально или внутриселезеночно) радиоактивный препарат, который попадает в воротную вену, а оттуда в печень (у здорового животного) или венозный кровоток (при наличии шунта). После введения препарата отслеживают сроки его накопления в печени и сердце. У здоровых животных печень накапливает препарат быстрее, чем сердце.Метод получил распространение в США, поскольку там находится большое количество научных центров, располагающих оборудованием для сцинтиграфии. Препарат содержит изотоп технеция с периодом полураспада около 6 часов. Его получают в изотопных генераторах непосредственно перед использованием. Для регистрации излучения применяют гамма-камеры.
Исследование неинвазивное (в случае с ректальным введением препарата), но оно позволяет только оценить, какая часть крови, поступающая от кишечника, идет в обход печени. То есть можно подтвердить наличие шунта, но не визуализировать его.
КТ-ангиография
КТ-ангиография (КТА) – метод получения изображения сосудов при помощи компьютерного томографа. Преимуществом КТ-ангиографии является то, что этот метод позволяет визуализировать сосуды брюшной полости, в том числе и воротную вену, не прибегая к селективному контрастированию. Компьютерная томография, в отличие от рентгенографии, дает возможность работать с изображениями срезов и трехмерными моделями, и для нее сложная сосудистая анатомия брюшной полости помехой не является (фото 8).При неселективной КТ-ангиографии рентгеноконтрастный препарат вводится в периферическую вену грудной конечности, откуда попадает в сердце, проходит малый круг кровообращения, возвращается в сердце и попадает в аорту. Из нисходящей аорты кровь с контрастным веществом попадает в сосуды селезенки и кишечника, а оттуда – в воротную вену. Прохождение контрастного препарата по сосудам – это динамический процесс. Обычно делается несколько серий сканирования в разные фазы прохождения контраста.
Для хорошей визуализации шунта необходимо, чтобы сканирование зоны интереса произошло во время нахождения максимального количества контрастного препарата в системе воротной вены. Время появления контрастного препарата в воротной вене зависит от скорости кровотока, которая может сильно отличаться у разных животных. На практике применяют два способа, позволяющих получить качественные изображения: измерение времени появления контраста в воротной вене по предварительной серии и болюс-трекер.
А – брюшная аорта, ВВ – часть воротной вены от кишечника до шунта, КПВ – каудальная полая вена, Ш – шунт, СВ – селезеночная вена.
Для измерения времени появления контраста в воротной вене перед предварительной серией сканирования вводят небольшое количество контрастного препарата, в момент начала введения препарата начинают сканирование одного и того же среза, расположение которого выбирают так, чтобы на нем были хорошо различимы нисходящая аорта, каудальная полая и воротная вены. Сканирование этого среза продолжается 1-2 минуты с периодичностью 1 раз в 0,5-2 секунды. По полученным изображениям определяют временной промежуток между внутривенным введением препарата и его появлением в воротной вене. На основании этого планируют и проводят серию с введением полной дозы контрастного препарата.
При методике "болюс-трекер", никаких предварительных серий не требуется, сразу вводится полная доза препарата, а используемый протокол исследования состоит из отслеживающей серии и серий спирального сканирования. Во время отслеживающей серии с периодичностью 1 раз в 1-2 секунды сканируется один и тот же срез, по которому сразу же автоматически определяется рентгеновская плотность крови в просвете выбранного сосуда. Как только плотность превысит указанный порог (то есть в сосуде появится достаточное количество рентгеноконтрастного препарата), начинается спиральное сканирование зоны интереса. Последующие серии начинаются через заданное время после начала первой серии. Как правило, делается несколько серий сканирования в разные сосудистые фазы. Визуализируются крупные артерии и вены брюшной полости.
КТ-ангиография позволяет не только обнаружить шунт, но и всесторонне описать его топографию: исследовать, между какими сосудами происходит сброс крови, описать локализацию шунта, оценить его размеры, выявить наличие множественных шунтов, оценить перфузию печени.
МРТ-ангиография
Магнитно-резонансная ангиография (МРА) – метод получения изображения сосудов при помощи магнитно-резонансного томографа. Метод позволяет оценивать как анатомические, так и функциональные особенности кровотока. МРА основана на отличии сигнала подвижной ткани (крови) от окружающих неподвижных тканей, что позволяет получать изображения сосудов без использования каких-либо рентгеноконтрастных средств. Для получения более четкого изображения при МР-ангиографии могут быть использованы рентгеноконтрастные препараты (на основе солей гадолиния), вводимые в периферическую вену.Лечение и прогноз
Консервативное лечение направлено на уменьшение количества токсинов, поступающих из желудка и кишечника в воротную вену. Заключается в подборе корма, энтеросорбентов и назначении процедур, направленных на восстановление водного, глюкозного и электролитного баланса организма. Предполагает также профилактику печеночной энцефалопатии.Хирургическое лечение заключается в частичном или полном, одномоментном или постепенном лигировании патологического сосуда. Для внепеченочных шунтов используют амероидные констрикторы и целлофановые лигатуры, для внутрипеченочных шунтов применяют эмболизацию внутрисосудистыми спиралями.
Литература:
1. А. Гоф, А. Томас. Породная предрасположенность к заболеваниям у собак и кошек. М., «Аквариум», 2005.
2. К. Пратчке. Портосистемные шунты у собак: обзор подходов к диагностике и лечению. Veterinary Focus, 2010, 20.3
3. Дж. Д. Бонагура, Р. Кирк. Современный курс ветеринарной медицины Кирка. М., «Аквариум», 2005.
4. D. E. Thrall et al. Textbook of Veterinary Diagnostic Radiology, Sixth Edition. Elsevier, 2013.
5. T. Schwarz, J. Saunders. Veterinary Computed Tomography. Wiley-Blackwell, 2011.
6. A. Bruehschwein et al. Contrast-enhanced magnetic resonance angiography for diagnosis of portosystemic shunts in 10 dogs. Vet RadiolUltrasound 2010, 51.
7. N. C. Nelson, L. L. Nelson. Anatomy of extrahepatic portosystemic shunts in dogs as determined by computed tomography angiography. Vet Radiol Ultrasound 2011, 52.
8. S. E. Kim et al. Comparison of computed tomographic angiography and ultrasonography for the detection and characterization of portosystemic shunts in dogs. Vet Radiol Ultrasound. 2013, 54.
9. A. Zwingenberger. CT diagnosis of portosystemic shunts. Vet Clin North Am Small Anim Pract. 2009, 39.
10. G. Bertolini et al. Three-dimensional multislice helical computed tomography techniques for canine extra-hepatic portosystemic shunt assessment. Vet Radiol Ultrasound. 2006, 47.
2. К. Пратчке. Портосистемные шунты у собак: обзор подходов к диагностике и лечению. Veterinary Focus, 2010, 20.3
3. Дж. Д. Бонагура, Р. Кирк. Современный курс ветеринарной медицины Кирка. М., «Аквариум», 2005.
4. D. E. Thrall et al. Textbook of Veterinary Diagnostic Radiology, Sixth Edition. Elsevier, 2013.
5. T. Schwarz, J. Saunders. Veterinary Computed Tomography. Wiley-Blackwell, 2011.
6. A. Bruehschwein et al. Contrast-enhanced magnetic resonance angiography for diagnosis of portosystemic shunts in 10 dogs. Vet RadiolUltrasound 2010, 51.
7. N. C. Nelson, L. L. Nelson. Anatomy of extrahepatic portosystemic shunts in dogs as determined by computed tomography angiography. Vet Radiol Ultrasound 2011, 52.
8. S. E. Kim et al. Comparison of computed tomographic angiography and ultrasonography for the detection and characterization of portosystemic shunts in dogs. Vet Radiol Ultrasound. 2013, 54.
9. A. Zwingenberger. CT diagnosis of portosystemic shunts. Vet Clin North Am Small Anim Pract. 2009, 39.
10. G. Bertolini et al. Three-dimensional multislice helical computed tomography techniques for canine extra-hepatic portosystemic shunt assessment. Vet Radiol Ultrasound. 2006, 47.






 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург