Перевод: Гареева Л. А., ветеринарный врач-кардиолог. Ветеринарный госпиталь «Панацея», г. Челябинск.
Ключевые слова:
фибрилляция предсердий (ФП);
застойная сердечная недостаточность (ЗСН);
миксоматозная дегенерация митрального клапана (МДМК);
прогнозы.
Миксоматозная дегенерация митрального клапана (МДМК) является наиболее распространенным заболеванием сердца у собак и характеризуется утолщением клапанных створок, пролапсом и сопутствующей регургитацией, приводящей к вторичным изменениям структуры и функций сердца. Распространенность заболевания коррелирует с возрастом и породой1. Только у некоторых собак с МДМК наблюдается прогрессирование до застойной сердечной недостаточности (ЗСН)2. Предикторы плохой выживаемости собак мелких пород с ЗСН из-за МДМК хорошо задокументированы и включают разрыв сухожильных хорд, разрыв стенки левого предсердия и различные виды аритмий2-5.
МДМК также встречается у собак средних и крупных пород, хотя характеристики заболевания несколько отличаются от таковых у собак мелких пород. МДМК у собак крупных пород часто проявляется меньшей степенью утолщения атриовентрикулярного (АВ) клапана, а эхокардиографические признаки легкой или умеренной систолической дисфункции левого желудочка (например, увеличение конечного систолического размера левого желудочка (КСР ЛЖ)) обычно присутствуют на момент диагностики ЗСН5,6. Кроме того, фибрилляция предсердий (ФП) чаще встречается у собак крупных пород с МДМК5.
ФП является наиболее распространенной наджелудочковой тахиаритмией у собак и особенно распространена у животных с тяжелыми сердечно-сосудистыми заболеваниями. Структурные изменения сердца, которые увеличивают напряжение стенки предсердий, предрасполагают к развитию ФП7. Электрическое ремоделирование в предсердиях (сокращение рефрактерного периода, замедление скорости проводимости, изменение уровня экспрессии ионных каналов) также играет роль в развитии ФП8. ФП вызывает ряд неблагоприятных последствий. В экспериментальных моделях было выявлено, что хроническая тахикардия (частота сердечных сокращений (ЧСС) > 180 уд/мин) приводит к систолической дисфункции левого желудочка и вторичному расширению камер сердца9. Снижение сократительной способности предсердий и сокращение времени диастолического наполнения из-за нерегулярной и обычно быстрой реакции желудочков при ФП могут снизить сердечный выброс и повысить давление наполнения предсердий, что в конечном итоге может привести к ухудшению СН и снижению качества и продолжительности жизни10.
ЗСН является основным фактором риска развития ФП и сокращения времени выживания у людей11-13. Сочетание ФП и ЗСН имеет наиболее худший прогноз, чем каждая из них по отдельности. Насколько известно авторам, прогностическое значение ФП для определения времени выживания у собак средних и крупных пород с МДМК и ЗСН, а также ее распространенность неизвестны.
Целями данного ретроспективного исследования являлись:
- оценка распространенности ФП у собак средних и крупных пород с ЗСН, вызванной МДМК;
- анализ влияния ФП на выживаемость этих животных, позволяющий определить, улучшает ли контроль частоты желудочковых сокращений показатели выживаемости.
Материалы и методы
Животные и критерии
Была изучена база данных учебной ветеринарной клиники им. Уильяма Р. Притчарда при Калифорнийском университете в Дэвисе (UCD VMTH) за период с 1 января 2005 г. по 31 декабря 2010 г. для выявления собак среднего и крупного размеров (> 15 кг) с ЗСН (как текущей, так и в анамнезе), ассоциированной с МДМК. Всего было идентифицировано 435 медицинских записей, содержащих ключевые термины застой, клапан и дегенерация. Проанализированные данные включали результаты аускультации сердца, массу тела (МТ), биохимические показатели крови, дозировки принимаемых сердечных препаратов, эхокардиографические измерения и электрокардиографические данные. Из-за значительного варьирования биохимических показателей и дозировок медикаментов на протяжении всего периода лечения отдельных пациентов для анализа данных последнего обследования, предшествующего смерти, был применен метод максимального правдоподобия (англ. maximum likelihood analysis).У собак крупных пород дифференцировать тяжелую форму МДМК и дилатационную кардиомиопатию может быть проблематично. Для верификации тяжелой МДМК как причины развития ЗСН у каждой собаки необходимо учитывать ряд критериев: фракция укорочения левого желудочка, превышающая 22%; наличие признаков тяжелой митральной регургитации (МР) при цветном доплеровском картировании; нормальное или гипердинамическое движение межжелудочковой перегородки; нормальное или незначительно увеличенное значение митрально-септальной сепарации (англ. E-point septal separation; EPSS). Тяжелая МР определялась на основании визуализации больших эксцентрических струй регургитации с использованием цветного доплеровского картирования и значительного увеличения размеров левого предсердия. У собак с устойчивой формой ФП средняя частота сердечных сокращений (ЧСС) в покое должна была превышать 160 уд/мин на момент проведения электрокардиографии (ЭКГ). Время включения в исследование определялось как дата постановки диагноза ЗСН, а диагноз проверялся и подтверждался сертифицированными ветеринарными кардиологами.
Критерии исключения: инфекционный эндокардит, врожденные пороки сердца, дилатационная кардиомиопатия (с признаками значительного увеличения КСР ЛЖ и фракцией выброса (FS) < 20%), собаки пород боксер и доберман-пинчер, собаки без указанных эхокардиографических данных, критериев или те животные, у которых ранее не было зафиксировано ЗСН, наличие кардиостимулятора, изолированная ФП, сопутствующие желудочковые аритмии, сопутствующие системные заболевания (например, эндокринопатии, рак, первичная почечная недостаточность), смерть, не связанная с сердечно-сосудистыми заболеваниями, а также случаи, когда пациенты были живы или потеряны для наблюдения на момент проведения исследования.
Определения
ЗСН определялась как наличие отека легких, асцита и/или плеврального выпота в сочетании с тяжелой сердечной патологией (выраженное расширение левого, правого или обоих предсердий), требующей введения диуретиков (фуросемида). Отек легких был диагностирован на основании клинических признаков (кашель, тахипноэ, одышка, ортопноэ), рентгенологической картины и/или повышенной частоты дыхания во сне (ЧДД), которая снизилась после начала лечения диуретической терапией (фуросемидом) у всех собак со значительно увеличенным левым предсердием.Электрокардиографическая оценка осуществлялась посредством регистрации поверхностной электрокардиограммы в исследуемой зоне. Средняя ЧСС в состоянии покоя определялась как среднее значение трех независимых измерений ЧСС, зарегистрированных в трех различных областях ЭКГ. Для расчета ЧСС за минуту количество комплексов QRS подсчитывалось за 6 секунд и умножалось на 10. Для контроля частоты ФП применялись антиаритмические средства: дилтиазем, дилтиазем пролонгированного действия (например, «Дилакор XR»), дигоксин и атенолол. Препараты использовались как по отдельности, так и в комбинации. Адекватный контроль ЧСС при ФП определялся как средняя ЧСС в покое ≤ 160 уд/мин в зоне исследования и подтверждался записями в базе данных ветеринарной клинической больницы (UCD VMTH) или других направляющих ветеринарных клиник, сделанными отдельно по каждому пациенту на протяжении всего периода лечения.
В процессе корректировки доз лекарственных средств, включая препараты с отрицательным хронотропным эффектом, проводилась повторная оценка ЭКГ через 5–7 дней для определения адекватности контроля ЧСС при ФП. Оценка проводилась клиницистом ветеринарной клинической больницы (UCD VMTH) либо направившим пациента лечащим врачом.
Наблюдение за исходами
Первичной конечной точкой была смерть от сердечно-сосудистых заболеваний. Смерть, связанная с сердечно-сосудистыми заболеваниями, определялась как совокупность случаев, включающих внезапную смерть или эвтаназию, обусловленную ухудшением состояния животного или рефрактерной хронической сердечной недостаточностью. Все собаки, включенные в исследование, достигли этой конечной точки. Для оценки времени выживания с момента постановки диагноза ЗСН до смерти, связанной с сердечно-сосудистыми заболеваниями, использовались данные из медицинских карт. Информация о последующем наблюдении за собаками, у которых данные о времени выживания отсутствовали в медицинских записях (статус выживаемости, конечное значение ЧСС для собак с ФП, причина и дата смерти), была получена посредством телефонных интервью с владельцами или лечащими ветеринарными врачами.Статистический анализ
Для оценки адекватности распределения данных использовался тест Шапиро – Уилка. Данные с нормальным распределением выражались в виде среднего и стандартного отклонений. Для данных с ненормальным распределением использовались медиана и диапазон. Демографические и клинические показатели анализировались на предмет различий между группами пациентов с ФП и без ФП. Для сравнения непрерывных переменных, таких как возраст, применялся Т-критерий Уилкоксона. Категориальные данные, включая распространенность ФП у определенного пола, анализировались с использованием точного критерия Фишера. Для оценки влияния клинических факторов на выживаемость применялся регрессионный анализ пропорциональных рисков Кокса. Рассчитывались отношение рисков (ОР) и 95% доверительные интервалы (ДИ). Результаты считались статистически значимыми при P < 0,05 и коэффициенте риска с 95% ДИ, отличным от 1. Для сравнения медианы выживаемости (времени, по истечении которого 50% собак в каждой группе были мертвы) и 95% ДИ между группами использовался метод Каплана – Мейера (КМ). Для определения статистически значимых различий в кривых выживаемости применялся логарифмический ранговый тест (логранговый тест). Для анализа взаимосвязи между дозировкой каждого антиаритмического препарата и степенью снижения ЧСС был проведен простой линейный регрессионный анализ. В качестве критерия статистической значимости для всех анализов было установлено значение P < 0,05.Результаты
Общие демографические данные и клинические результаты
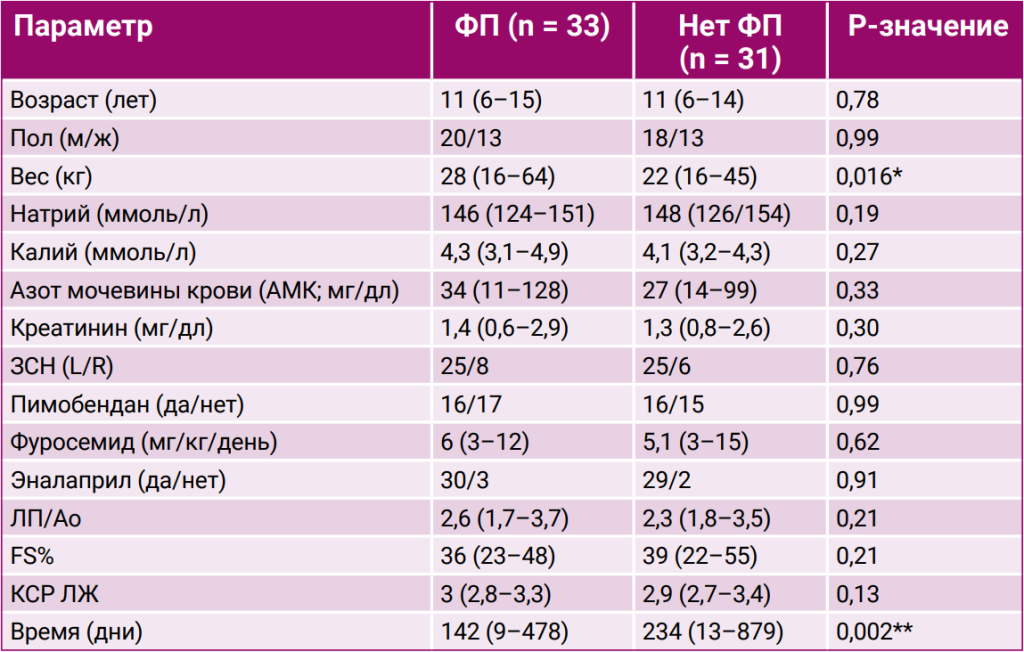
Критериям включения в исследование в общей сложности соответствовали 64 собаки. Наиболее распространенными породами были австралийская овчарка (n = 16), немецкая овчарка (n = 9) и лабрадор-ретривер (n = 7). Также была выявлена еще 21 порода, по 1–3 собаки в каждой. Средний возраст на момент постановки диагноза ЗСН составил 11 лет (диапазон: 6–15 лет). Средняя масса тела (МТ) составила 24 кг (диапазон: 16–64 кг). 38 собак были кобелями и 26 – суками. У большинства животных (n = 50) наблюдалась левосторонняя ЗСН, а у 14 – как левосторонняя, так и правосторонняя ЗСН. Всем собакам (n = 64) вводили фуросемид, средняя суточная доза составляла 5,6 мг/кг/день (диапазон: 3–15 мг/кг/день). Большинству собак (n = 59) вводили эналаприл, средняя доза составляла 0,45 мг/кг каждые 12 часов (диапазон: 0,43–0,56 мг/кг каждые 12 часов). Половине животных (n = 32) вводили пимобендан в средней дозе 0,23 мг/кг каждые 12 часов (диапазон: 0,21–0,27 мг/кг каждые 12 часов). Другими препаратами для лечения сердечной недостаточности, которые применялись одновременно, были гидрохлоротиазид (n = 3) и спиронолактон (n = 3). Среднее соотношение ЛП/Ao, измеренное в конце зубца T, составило 2,5 (диапазон: 1,7–3,7). Медианные значения фракции выброса (FS%) и нормализованного КСР (КСР(н)/МТ1/3) составили 36% (диапазон: 22–55%) и 2,9 (диапазон: 2,7–3,4) соответственно (табл. 1).Медиана времени выживания (MST) с момента постановки диагноза ЗСН до смерти, связанной с сердечной патологией, всех 64 собак составила 172 дня (диапазон: 9–879 дней). У тридцати трех собак (52%) была диагностирована ФП. На момент постановки диагноза ЗСН ФП регистрировалась у 21 животного, у 12 собак она развилась в течение последующего наблюдения, при этом средний интервал от постановки диагноза ЗСН до развития ФП составил 63 дня (диапазон: 5–267 дней). Медиана времени с момента регистрации ФП до смерти от сердечной патологии составила 75 дней (диапазон: 3–470 дней). У 31 собаки (48%) сохранялся синусовый ритм с момента начала наблюдения до смерти, связанной с сердечной патологией. Анализ не выявил значимых различий в клинических параметрах между собаками с наличием и отсутствием ФП за исключением массы тела и времени выживания (табл. 1). Собаки с ФП (медиана МТ: 28 кг, диапазон: 16–64 кг) имели большую массу тела по сравнению с собаками без ФП (медиана МТ: 22 кг, диапазон: 16–45 кг; P = 0,0155). Медиана выживаемости у собак с ФП составила 142 дня (диапазон: 9–478 дней), в то время как у собак без ФП – 234 дня (диапазон: 13–879 дней; P = 0,002).
Анализ пропорциональных рисков Кокса для оценки влияния клинических переменных на время выживания
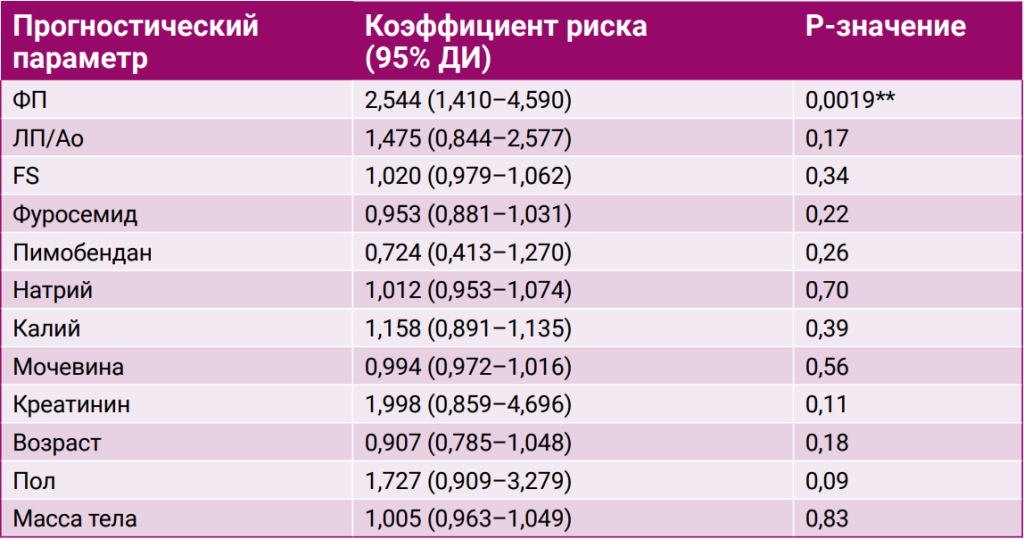
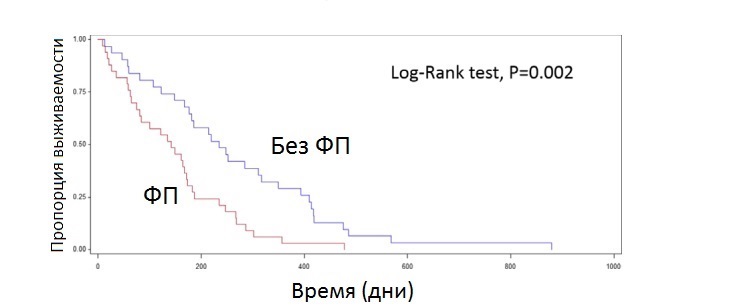
Для выявления факторов риска, существенно влияющих на время выживания, был проведен одномерный анализ 12 переменных величин (ФП, ЛП/Ао, FS%, фуросемид, пимобендан, концентрация натрия в сыворотке, концентрация калия в сыворотке, азот мочевины крови (АМК), концентрация креатинина в сыворотке, возраст, пол, масса тела). Фибрилляция предсердий оказалась значимым фактором риска для достижения первичной конечной точки – сердечно-ассоциированной смерти (ОР = 2,544; 95% ДИ = 1,41–4,59; P = 0,0019) по сравнению с собаками без ФП. Ни одна другая переменная не была связана с положительным или отрицательным клиническим исходом (табл. 2). Поскольку ФП была единственной значимой клинической переменной, выявленной в одномерном анализе, дальнейший многомерный анализ не проводился. Логранговый тест для кривых выживаемости по методу Каплана – Мейера (КМ) подтвердил статистически значимую разницу во времени выживания между собаками с ФП и собаками без ФП (P = 0,002; рис. 1).
Влияние терапии ФП препаратами с отрицательным хронотропным эффектом на выживаемость
Основной целью антиаритмической терапии при фибрилляции предсердий (ФП) является снижение частоты желудочковых сокращений (ЧСС).
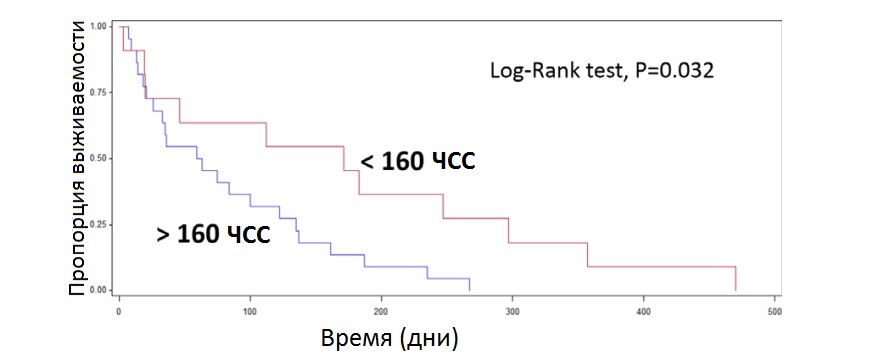
В данном исследовании оценивалось влияние эффективности достижения среднего значения ЧСС < 160 уд/мин на выживаемость собак с ЗСН (рис. 2). Адекватный контроль ЧСС определялся как поддержание ЧСС < 160 уд/мин, а неадекватный контроль – как ЧСС > 160 уд/мин. В рамках исследования было выявлено, что MST у собак с ФП и адекватно контролируемой ЧСС значительно выше по сравнению с собаками, которые не реагировали на использование препаратов с отрицательным хронотропным эффектом. MST с момента постановки диагноза ЗСН до смерти от сердечно-сосудистых заболеваний у собак со средним значением ЧСС < 160 уд/мин (n = 13) составила 171 день, тогда как у собак со средним значением ЧСС > 160 уд/мин (n = 20) этот показатель составил 61 день (P = 0,032; рис. 2).
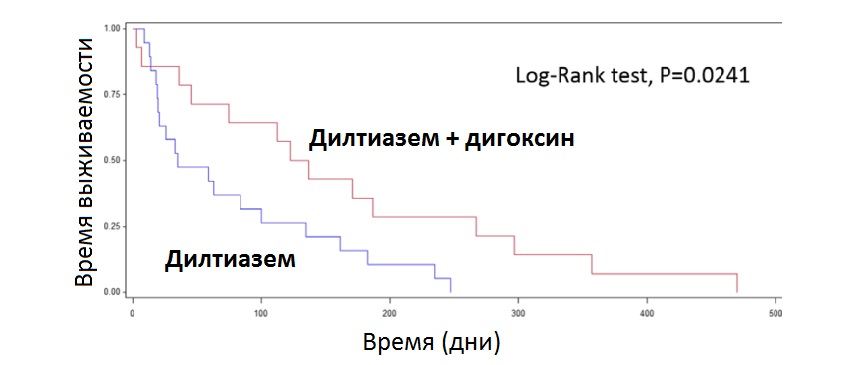
Девять собак из 13 с адекватным контролем ЧСС получали дилтиазем и дигоксин. У собак с ФП медиана FS% и КСР ЛЖ при ЧСС < 160 уд/мин не отличались от таковых у собак с ЧСС > 160 уд/мин. Медиана ЧСС до введения любых препаратов с отрицательным хронотропным эффектом у собак с ФП составляла 220 уд/мин (диапазон: 160–270 уд/мин). Монотерапия дилтиаземом являлась наиболее распространенным методом лечения. Средняя доза составила 1 мг/кг каждые 8 часов (диапазон: 0,5–2 мг/кг каждые 8 часов). Медиана ЧСС после применения только дилтиазема составила 180 уд/мин (диапазон: 120–240 уд/мин). Было обнаружено статистически значимое снижение медианы ЧСС после применения только дилтиазема (P = 0,006). Анализ пропорциональных рисков Кокса не выявил статистически значимой связи между применением дилтиазема и MST (P = 0,669). Однако у собак, получавших дилтиазем в комбинации с дигоксином, средняя ЧСС контролировалась лучше (медиана: 144 уд/мин, диапазон: 84–218 уд/мин) по сравнению с собаками, получавшими только дилтиазем (медиана: 180 уд/мин, диапазон: 120–240 уд/мин). Анализ по методу Каплана – Мейера показал, что введение дигоксина в сочетании с дилтиаземом значительно улучшило выживаемость: MST у 13 собак при комбинированной терапии составила 130 дней против 35 дней при монотерапии дилтиаземом
(P = 0,0241; рис. 3). Средняя доза дигоксина составляла 0,004 мг/кг каждые 12 часов (диапазон: 0,003–0,006 мг/кг каждые 12 часов). Две собаки получали дилтиазем пролонгированного действия («Дилакор XR», 3 мг/кг каждые 12 часов) в сочетании с дигоксином (0,003 мг/кг каждые 12 часов), что также обеспечило адекватное снижение ЧСС (диапазон: 140–160 уд/мин). Не было выявлено значимого улучшения среднего показателя ЧСС в состоянии покоя у трех собак при монотерапии атенололом в дозе 0,3–1,5 мг/кг каждые 12 часов (ЧСС до лечения – 220–250 уд/мин; после – 200–240 уд/мин).
Обсуждение
Фибрилляция предсердий (ФП) часто встречается у собак с ЗСН, обусловленной миксоматозной дегенерацией митрального клапана (МДМК), и связана с более коротким временем выживания у собак среднего и крупного размеров с МДМК и ЗСН.У всех 64 собак, соответствующих критериям включения, было выявлено значительное увеличение левого предсердия (среднее соотношение ЛП/Ao составило 2,5), и примерно у 52% из них (n = 33) развилась ФП. Патология предсердий, включая их дилатацию, предрасполагает к развитию ФП. Это обусловлено тем, что растяжение предсердий приводит к увеличению дисперсии рефрактерности и нарушению распространения электрического импульса14,15.
В данном исследовании MST собак с тяжелой митральной регургитацией (МР), вызванной МДМК, но без фибрилляции предсердий (ФП) составляла примерно 8 месяцев. Этот показатель согласуется с ранее опубликованными данными о MST у собак мелких пород с тяжелыми формами МДМК и ЗСН, где конечная точка была определена как смерть, связанная с сердечно-сосудистыми заболеваниями, и составляла 9 месяцев2. Однако медиана выживаемости у собак с ФП в этом исследовании была значительно короче (4,7 месяцев).
Фармакологический контроль ЧСС остается ключевым элементом долгосрочной терапии ФП у собак. В этом исследовании менее половины собак (42%) в группе с ФП достигли адекватного контроля ЧСС на ЭКГ в зоне исследования (ЧСС < 160 уд/мин) при применении препаратов с отрицательным хронотропным эффектом. Медиана выживаемости была короче у собак, не достигших целевого уровня ЧСС 160 уд/мин и меньше. Длительная тахикардия (ЧСС > 180 уд/мин) в течение более 2–4 недель у собак приводит к недостаточности миокарда, индуцированной тахикардией16,17.
Считается, что основной терапевтической целью при ФП является предотвращение миокардиальной недостаточности, вызванной тахикардией, путем контроля ЧСС либо восстановления синусового ритма (контроль ритма)15. Клинические исследования, проводимые на людях, показали, что использование обоих подходов (контроль ЧСС и ритма) приводит к сопоставимым показателям заболеваемости и смертности18. Таким образом, контроль частоты сердечных сокращений не менее эффективен, чем контроль ритма, с точки зрения клинических результатов19.
Хотя фракция выброса (FS%) не является наиболее точной и последовательной эхокардиографической переменной для оценки функции левого желудочка (ЛЖ), она часто используется как разумная альтернатива для оценки систолической насосной функции ЛЖ (англ. LV systolic pump function)20. Ранее сообщалось, что у собак мелких пород (< 15 кг) с МДМК и тяжелой сердечной недостаточностью наблюдалась гипердинамическая функция ЛЖ (средний показатель FS% – примерно 52%) из-за выраженного увеличения КСР и нормального или слегка увеличенного КСР5. В данном исследовании медиана FS% была намного ниже, но находилась в пределах референтного диапазона (36%), что обусловлено заметным увеличением КСР ЛЖ и (чаще всего) умеренным увеличением КСР ЛЖ, которые являются характерными признаками тяжелой МР у собак среднего и крупного размеров с МДМК и ЗСН5,6. Поскольку FS% и индексированное значение КСР ЛЖ не различались у собак с ФП и собак без ФП, снижение времени выживания у собак с ФП может быть больше связано с отсутствием вклада предсердий в сердечную функцию, чем с систолической дисфункцией левого желудочка.
Доступные фармакологические методы контроля ЧСС при ФП можно в целом разделить на недигидропиридиновые блокаторы кальциевых каналов (например, дилтиазем), дигоксин и бета-адреноблокаторы (например, атенолол, соталол). Хотя «Дилакор ХR» применялся только у двух собак в исследовании, его антиаритмическая активность и свойство пролонгированного высвобождения делают его привлекательным вариантом для контроля частоты ФП. Эти признанные фармакологические методы лечения оказывают свой положительный эффект посредством модуляции АВ-узловой проводимости путем продления рефрактерного периода узла и замедления проводимости через него. Средняя ЧСС в покое, зафиксированная на электрокардиограмме (ЭКГ) в условиях стационара и составляющая менее 160 уд/мин, была предложена в качестве целевой ЧСС для контроля частоты ФП21. Обоснование данного ограничения связано с тем, что миокардиальная недостаточность, вызванная тахикардией, развивается при частоте сердечных сокращений 180 уд/мин и выше16,17. Тот факт, что в данном исследовании пороговое значение 160 уд/мин привело к значительной разнице в выживаемости, усилил аргумент в пользу потенциальной достоверности предложенного порогового значения, поэтому существует вероятность, что даже более низкий порог может быть более целесообразным. Оптимальный уровень контроля заболеваемости и смертности еще предстоит определить.
Результаты исследования показывают, что выживаемость была значительно лучше у собак с адекватным контролем ЧСС (< 160 уд/мин) по сравнению с собаками с плохим контролем ЧСС (рис. 2). Строгого контроля ЧСС, по-видимому, было трудно достичь с помощью одного препарата, такого как дилтиазем. Неизвестно, была ли более высокая доза дилтиазема у какой-либо конкретной собаки полезной и хорошо переносимой. У собак, которым одновременно вводили дигоксин и дилтиазем, целевая ЧСС достигалась чаще, чем при использовании только дилтиазема, и анализ по методу Каплана – Мейера подтверждает вывод о том, что введение дигоксина вместе с дилтиаземом значительно улучшало показатели выживаемости (рис. 3). Это наблюдение согласуется с предыдущим сообщением о том, что комбинация дилтиазема и дигоксина обеспечивает лучший контроль ЧСС, чем любой из препаратов по отдельности, у собак с ФП22.
Остается вопрос, улучшает ли прогноз еще более строгий контроль ЧСС (целевая ЧСС < 140 уд/мин). Также остается открытым вопрос относительно того, могут ли повышенные дозы лекарственных препаратов и комбинированная терапия несколькими средствами увеличивать риск развития побочных эффектов. Недавние клинические исследования, проведенные на людях, показали, что менее строгий контроль ЧСС может быть не менее эффективным в отношении выживаемости по сравнению со строгим контролем, при этом его достижение требует меньших усилий23.
Ограничениями исследования являются ретроспективный дизайн исследования и его потенциальная систематическая ошибка отбора. Данные о динамике заболевания (продольные данные) были ограничены у некоторых собак. Слабая статистическая мощность, обусловленная нерандомизированным распределением собак по группам (с ФП и без ФП), ограничивает возможность обобщения результатов исследования на более широкую популяцию. Также важно подчеркнуть, что собаки, включенные в исследование, находились под наблюдением разных врачей в течение 6 лет. Хотя основной целью исследования было определение прогностической значимости ФП у собак с МДМК и ЗСН, успешное лечение ЗСН и различные схемы лечения в качестве сопутствующих параметров могли повлиять на результаты выживаемости. Адекватность контроля ЧСС при антиаритмическом лечении ФП оценивалась только по данным ЭКГ. Суточное амбулаторное мониторирование ЭКГ (холтеровское мониторирование) для оценки среднесуточной ЧСС до и после лечения не проводилось. Некоторые даты постановки диагноза ЗСН и смерти от сердечно-сосудистых заболеваний были основаны исключительно на воспоминаниях владельцев, однако большая часть информации была собрана благодаря медицинским записям.
Вывод
Распространенность ФП была высокой у собак среднего и крупного размеров с МДМК и ЗСН, и ФП значительно повышала риск смерти от сердечно-сосудистых заболеваний у этих собак. Более низкая медиана выживаемости (MST) у собак с ФП и неоптимальным контролем ЧСС позволяет предположить, что адекватный контроль ЧСС является критически важным элементом в определении долгосрочной выживаемости. Адекватный контроль частоты сердечных сокращений, достигнутый путем введения дигоксина и дилтиазема, оказал благоприятное влияние на MST. Необходимо провести проспективное клиническое исследование для определения эффективных методов лечения и прогностических преимуществ оптимального контроля ЧСС при лечении ФП.Список литературы:
- Haggstrom J, Hansson K, Kvart C, et al. Chronic valvular disease in the cavalier King Charles spaniel in Sweden. Vet Rec 1992;131:549–553.
- Borgarelli M, Savarino P, Crosara S, et al. Survival characteristics and prognostic variables of dogs with mitral regurgitation attributable to myxomatous valve disease. J Vet Intern Med 2008;22:120–128.
- BENazepril in Canine Heart disease Study Group. The effect of benazepril on survival times and clinical signs of dogs with congestive heart failure: results of a multicenter, prospective, randomized, double-blinded, placebo-controlled, long-term clinical trial. J Vet Cardiol 1999;1:7–18.
- Serres F, Chetboul V, Tissier R, et al. Chordae tendineae rupture in dogs with degenerative mitral valve disease: prevalence, survival, and prognostic factors (114 cases, 2001–2006). J Vet Intern Med 2007;21:258–264.
- Borgarelli M, Zini E, D’Agnolo G, et al. Comparison of primary mitral valve disease in German Shepherd dogs and in small breeds. J Vet Cardiol 2004;6:27–34.
- Cornell CC, Kittleson MD, Della Torre P, et al. Allometric scaling of M-mode cardiac measurements in normal adult dogs. J Vet Intern Med 2004;18:311–321.
- Hunter RJ, Liu Y, Lu Y, et al. Left atrial wall stress distribution and its relationship to electrophysiologic remodeling in persistent atrial fibrillation. Circ Arrhythm Electrophysiol 2012;5:351–360.
- van den Berg MP, Tjeerdsma G, Jan de Kam P, et al. Longstanding atrial fibrillation causes depletion of atrial natriuretic peptide in patients with advanced congestive heart failure. Eur J Heart Fail 2002;4:255–262.
- Shinbane JS, Wood MA, Jensen DN, et al. Tachycardiainduced cardiomyopathy: a review of animal models and clinical studies. J Am Coll Cardiol 1997;29:709–715.
- Burashnikov A, Antzelevitch C. New developments in atrial antiarrhythmic drug therapy. Nat Rev Cardiol 2010;7:139–148.
- Wang TJ, Larson MG, Levy D, et al. Temporal relations of atrial fibrillation and congestive heart failure and their joint influence on mortality: the Framingham Heart Study. Circulation 2003;107:2920–2925.
- Ehrlich JR, Nattel S, Hohnloser SH. Atrial fibrillation and congestive heart failure: specific considerations at the intersection of two common and important cardiac disease sets. J Cardiovasc Electrophysiol 2002;13:399–405.
- Cha YM, Redfield MM, Shen WK, et al. Atrial fibrillation and ventricular dysfunction: a vicious electromechanical cycle. Circulation 2004;109:2839–2843.
- Solti F, Vecsey T, Kekesi V, et al. The effect of atrial dilatation on the genesis of atrial arrhythmias. Cardiovasc Res 1989;23:882–886.
- Wann LS, Curtis AB, Ellenbogen KA, et al. 2011 ACCF/ AHA/HRS focused update on the management of patients with atrial fibrillation: a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol 2011;57:1330–1337.
- Armstrong PW, Stopps TP, Ford SE, et al. Rapid ventricular pacing in the dog: pathophysiologic studies of heart failure. Circulation 1986;74:1075–1084.
- Wilson JR, Douglas P, Hickey WF, et al. Experimental congestive heart failure produced by rapid ventricular pacing in the dog: cardiac effects. Circulation 1987;75:857–867.
- Perez A, Touchette DR, DiDomenico RJ, et al. Comparison of rate control versus rhythm control for management of atrial fibrillation in patients with coexisting heart failure: a costeffectiveness analysis. Pharmacotherapy 2011;31:552–565.
- Roy D, Talajic M, Nattel S, et al. Rhythm control versus rate control for atrial fibrillation and heart failure. N Engl J Med 2008;358:2667–2677.
- Bonagura JD, Schober KE. Can ventricular function be assessed by echocardiography in chronic canine mitral valve disease? J Small Anim Pract 2009;50(Suppl 1):12–24.
- Kittleson MD, Kienle RD. Small Animal Cardiovascular Medicine. St Louis, MO: Mosby Inc; 1998:473.
- Gelzer AR, Kraus MS, Rishniw M, et al. Combination therapy with digoxin and diltiazem controls ventricular rate in chronic atrial fibrillation in dogs better than digoxin or diltiazem monotherapy: a randomized crossover study in 18 dogs. J Vet Intern Med 2009;23:499–508.
- Van Gelder IC, Groenveld HF, Crijns HJ, et al. Lenient versus strict rate control in patients with atrial fibrillation. N Engl J Med 2010;362:1363–1373.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург