1Ветеринарный врач-кардиолог, ВК Сложного случая, г. Санкт-Петербург.
2Ветеринарный врач-анестезиолог, ВК Сложного случая, г. Санкт-Петербург.
Список сокращений:
BAS – баллонная атриосептостомия (Balloon Atrial Septostomy);
DMVD – дегенеративная болезнь митрального клапана (Degenerative Mitral Valve Disease);
LVIDd – конечно-диастолический внутренний диаметр левого желудочка (Left Ventricular Internal Diameter in Diastole);
TAPSE – систолическая экскурсия кольца трикуспидального клапана (Tricuspid Annular Plane Systolic Excursion);
МАК – минимальная альвеолярная концентрация (Minimum Alveolar Concentration, MAC);
ИПС – инфузия с постоянной скоростью (Constant Rate Infusion, CRI);
АПФ – ангиотензинпревращающий фермент; ингибиторы АПФ – ингибиторы ангиотензинпревращающего фермента (ACE inhibitors);
С-дуга – рентгеновская С-дуга (C-arm).
Аннотация
В статье рассматривается применение метода эндоваскулярной баллонной атриосептостомии (BAS) у собак с терминальной стадией дегенеративной болезни митрального клапана (DMVD). Представлены патофизиологические обоснования метода, показания, техника выполнения и анализ клинических случаев. Внимание уделено критериям отбора, осложнениям и послеоперационному ведению. Результаты демонстрируют клиническую эффективность и безопасность метода при соблюдении условий отбора пациентов.Ключевые слова: атриосептостомия, митральная регургитация, сердечная недостаточность, ветеринарная кардиология, собаки, баллонная дилатация, паллиативная помощь.
Введение
Дегенеративная болезнь митрального клапана (Degenerative Mitral Valve Disease, DMVD) является одной из наиболее распространенных причин хронической сердечной недостаточности у собак преимущественно мелких и средних пород1. Согласно данным Американского колледжа ветеринарной медицины внутренних болезней (American College of Veterinary Internal Medicine, ACVIM)5, DMVD составляет до 75% всех приобретенных заболеваний сердца у собак. Прогрессирование митральной регургитации приводит к объемной перегрузке левых отделов сердца и увеличению давления в легочных капиллярах, что в результате способствует развитию кардиогенного отека легких1,5.На терминальных стадиях заболевания (C/D по классификации ACVIM5), несмотря на применение комплексной медикаментозной терапии, пациенты могут страдать от рецидивирующих эпизодов декомпенсации, требующих частых госпитализаций1,3,5. Это значительно ухудшает качество жизни как самих животных, так и их владельцев. В таких клинических ситуациях обоснованным является поиск паллиативных решений2,3.
Одно из таких решений – баллонная атриосептостомия (BAS), ранее апробированная в неонатальной кардиохирургии человека для коррекции врожденных пороков сердца. Принцип метода заключается в создании контролируемого межпредсердного шунта, что позволяет разгрузить левое предсердие и стабилизировать гемодинамику (рис. 1). В ветеринарной практике использование BAS является новым направлением, требующим систематизации клинического опыта2,3.
Материалы и методы
Настоящее исследование основано на анализе клинических случаев пяти собак с терминальной стадией дегенеративной болезни митрального клапана (DMVD), которым была выполнена эндоваскулярная баллонная атриосептостомия (BAS) в период с 2024 по 2025 год.Все пациенты поступили в ВК Сложного случая с выраженной клиникой застойной сердечной недостаточности, рефрактерной к медикаментозной терапии.
Критерии включения в исследование были следующими:
- документально подтвержденный диагноз «дегенеративная болезнь митрального клапана (DMVD) стадии D» (по классификации Американской коллегии ветеринарных специалистов в области интернальной медицины [ACVIM], 2020);
- частые эпизоды кардиогенного отека легких (более одной госпитазилации по причине основного заболевания);
- выраженное расширение левого предсердия;
- увеличение конечно-диастолического размера левого желудочка [LVIDd], превышающее нормативные значения для конкретной породы;
- признаки венозного застоя в малом круге кровообращения по данным эхокардиографии.
Перед процедурой всем животным проводилось базовое обследование, включавшее клинический и биохимический анализы крови, эхокардиографию (ЭхоКГ).
Процедура баллонной атриосептостомии выполнялась под общей анестезией.
Анестезиологическое обеспечение процедуры баллонной атриосептостомии является критически важным компонентом успеха вмешательства ввиду тяжести состояния пациентов.
Предоперационная подготовка и премедикация
Перед процедурой животные проходили подготовку в условиях отделения реанимации и интенсивной терапии (ОРИТ). Для премедикации с целью седации наиболее часто применялся ацепромазин в дозе 0,1 мг/кг перорально. Спустя 5–10 минут внутривенно вводился диазепам («Реланиум») в дозе 1 мг/кг для усиления седативного эффекта и миорелаксации.Индукция и поддержание анестезии
Индукцию анестезии проводили с использованием пропофола в дозе 2–3 мг/кг внутривенно до снижения уровня мышечного тонуса нижней челюсти, обеспечивающего успешное выполнение эндотрахеальной интубации. Поддержание хирургической стадии анестезии осуществлялось с помощью ингаляционных анестетиков – изофлурана или севофлурана – в минимальной альвеолярной концентрации (МАК), необходимой для поддержания гемодинамической стабильности пациента.Гемодинамическая поддержка и анальгезия
Ввиду высокого риска развития гипотонии и брадикардии в процессе катетеризации сердца всем пациентам при переводе в операционный блок начинали постоянную инфузию инотропных и вазопрессорных препаратов, в частности применяли адреналин в дозе 0,02 мкг/кг/мин для обеспечения люзитропного эффекта и добутамин в дозе 2–5 мкг/кг/мин.Для обеспечения адекватной анальгезии применялся комплексный подход, который включал блокаду корешков спинномозговых нервов C2–C4 и/или непрерывную инфузию (ИПС) фентанила по следующей схеме: болюсное введение в дозе 2 мкг/кг с последующей поддерживающей инфузией со скоростью 2 мкг/кг/час.
Мониторинг
На протяжении всей процедуры осуществлялся непрерывный мониторинг жизненно важных функций: электрокардиография (ЭКГ), частота сердечных сокращений (ЧСС), сатурация кислорода артериальной крови (SpO2), температура тела, капнометрия. Артериальное давление контролировалось параллельно двумя методами: инвазивным (через артериальный катетер) и осциллометрическим.Коррекция интраоперационных осложнений
В процессе проведения манипуляции частыми осложнениями были аритмии, индуцированные катетеризацией. Для их купирования применяли болюсное введение лидокаина в дозе 1–2 мг/кг.Вследствие высокой чувствительности пациентов с кардиологическими заболеваниями к вазодепрессивным эффектам ингаляционных анестетиков часто регистрировалась артериальная гипотензия. Для ее коррекции в первую очередь увеличивали скорость инфузии инотропной поддержки (добутамин), а также проводили болюсную нагрузку кристаллоидными растворами. При резистентной гипотонии дополнительно применяли вазопрессорную терапию: фенилэфрин («Мезатон») болюсно в дозе 0,001–0,004 мг/кг и/или норадреналин в виде инфузии в дозе 1–5 мкг/кг/мин.
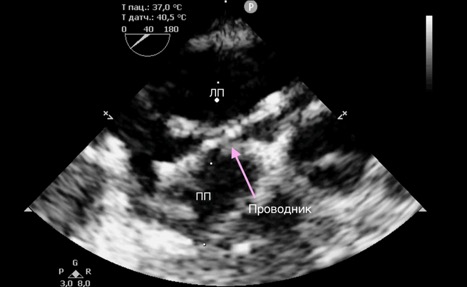
После достижения необходимой анестезии устанавливали интродьюсер, через который в правое предсердие вводился проводниковый катетер. Наведение проводника на межпредсердную перегородку осуществлялось под контролем чреспищеводной эхокардиографии. В большинстве случаев выбирали область овальной ямки (лат. fossa ovalis) как наиболее анатомически безопасную и предсказуемую зону для пункции. Пункция перегородки выполнялась обратной (тупой) стороной проводника, что снижало риск повреждения окружающих структур (рис. 2). После успешного проникновения в левое предсердие по проводнику заводился баллонный катетер (диаметром от 12 до 14 мм).
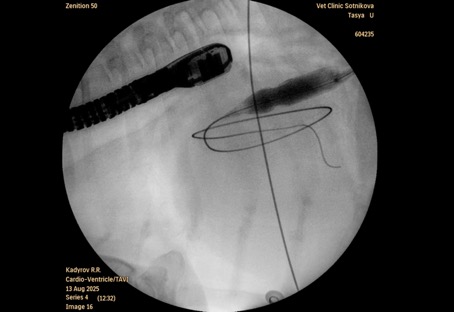
Баллон раздувался до рабочего давления (8–10 атм) в течение 10–15 сек. для создания постоянного сообщения между предсердиями. В ряде случаев требовалась повторная инсуффляция для достижения адекватного диаметра дефекта. В ходе процедуры осуществлялся интраоперационный контроль положения проводника и баллона с использованием эхокардиографического контроля и С-дуги (рис. 3).
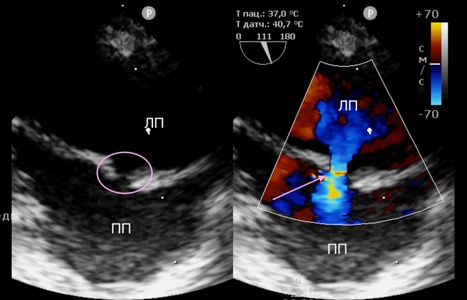
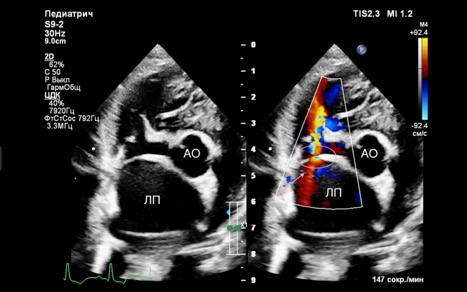
Объективным критерием успешности проведения процедуры являлось наличие сброса слева направо, подтвержденного методом цветного доплеровского сканирования(рис. 4), а также снижение давления в левом предсердии, которое оценивалось с помощью катетера, вводимого в левое предсердие. После завершения инсуффляции баллон и проводник удалялись, а сосуд ушивался непрерывным швом.
После завершения процедуры пациенты переводились в послеоперационный стационар для круглосуточного мониторинга в течение первых 24–48 ч. В этот период продолжалась терапия пимобенданом, а предоперационная доза мочегонных средств снижалась на 14–50%. Прием ингибиторов АПФ и спиронолактона временно прекращался, или их дозы уменьшались из-за риска развития гипонатриемии. У некоторых пациентов гипонатриемия проявлялась уже в раннем послеоперационном периоде. Кроме того, всем пациентам назначался ривароксабан в профилактической дозе для предотвращения тромбообразования в зоне дефекта на срок 4–6 недель.
Результаты
Во всех пяти случаях, включенных в исследование, после выполнения атриосептостомии была зафиксирована положительная динамика клинического состояния животных в течение первых 24–72 ч.- Гемодинамические показатели:
- уменьшение давления в левом предсердии на 28–43% (по данным интраоперационного катетерного мониторинга);
- снижение признаков венозного застоя в малом круге кровообращения (по данным эхокардиографии);
- обратное ремоделирование сердца в раннем послеоперационном периоде.
- Клинические проявления:
- отсутствие повторных эпизодов кардиогенного отека легких в течение минимум 4 недель после вмешательства у всех пациентов;
- улучшение общего состояния: исчезновение одышки в покое, снижение ЧДД до физиологического уровня, восстановление аппетита и активности;
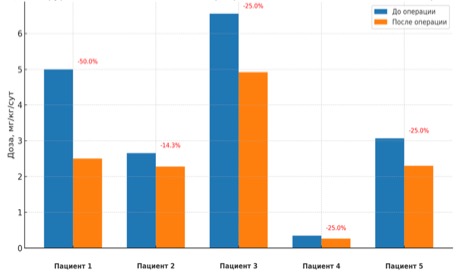
- уменьшение доз диуретиков (рис. 5).
- Побочные эффекты и осложнения:
- у одного пациента развился гемоперикард, не потребовавший проведения перикардиоцентеза;
- у другого пациента во время проведения баллонной дилатации возникла фибрилляция предсердий, успешно купированная синхронизированной кардиоверсией;
- в одном случае дефект межпредсердной перегородки полностью закрылся через 28 дней, что потребовало проведения повторной процедуры (после повторного вмешательства устойчивый клинический эффект сохранялся в течение 3 месяцев наблюдения);
- развитие гипонатриемии в послеоперационном периоде.
- Продолжительность наблюдения
- Минимальный срок послеоперационного наблюдения составил 30 дней, максимальный – 120 дней. У всех пациентов на протяжении всего периода наблюдения сохранялась компенсация сердечной недостаточности без повторной госпитализации.
- Контрольные данные ЭхоКГ
- В течение первых суток, а также на 14-й и 30-й дни после оперативного вмешательства на эхокардиографии выявлялось устойчивое наличие межпредсердного шунта со сбросом слева направо без признаков значимой объемной перегрузки правого желудочка (рис. 6).
Обсуждение
Полученные данные подтверждают высокую эффективность баллонной атриосептостомии как паллиативного метода у собак с терминальной стадией DMVD. Процедура позволяет добиться контроля над симптомами без постоянной госпитализации.Ключевым фактором успеха является строгое соблюдение критериев отбора. Функциональная состоятельность правого желудочка – важнейшее условие для предотвращения перегрузки правых отделов и развития правожелудочковой недостаточности, также важно отсутствие тяжелой легочной гипертензии.
Устойчивость клинического эффекта при отсутствии тяжелых осложнений у большинства пациентов делает технику перспективной для применения в ветеринарной практике. Данное оперативное вмешательство не приводит к выздоровлению пациента, а лишь временно стабилизирует его состояние.
Наблюдавшаяся в послеоперационном периоде гипонатриемия, вероятно, обусловлена изменением преднагрузки и реабсорбцией жидкости (после снижения давления наполнения левого предсердия) и требует мониторинга.
Выводы
- Баллонная атриосептостомия – эффективный паллиативный метод при терминальной стадии DMVD у собак.
- Метод позволяет достичь устойчивой декомпрессии левого предсердия, снизить потребность в медикаментах и повысить качество жизни пациентов.
- Соблюдение критериев отбора и технической точности является критически важным для успешного проведения процедуры.
- Требуется дальнейшее расширенное исследование эффективности баллонной атриосептостомии и долгосрочного прогноза после ее проведения.
- Borgarelli M., Häggström J. Canine degenerative myxomatous mitral valve disease: natural history, clinical presentation and therapy. Vet Clin North Am Small Anim Pract. 40(4): 651–663, 2010.
- Caivano D., Rishniw M., Birettoni F., et al. Use of balloon atrial septostomy for palliation in a dog with left-sided congestive heart failure. J Vet Cardiol, 44:12–20, 2022.
- Pelizzaro M., Bussadori R., Santilli R. A. New interventional options in end-stage mitral valve disease in dogs. Vet Interv Cardiol, 2(1):25–32, 2024.
- Kellum H. B., Stepien R. L., Brown D. J. ACVIM consensus statement: Guidelines for the diagnosis, classification, treatment, and monitoring of pulmonary hypertension in dogs. J Vet Intern Med, 34(2): 549–573, 2020.
- Keene B. W., Atkins C. E., Bonagura J. D., Fox P. R., Häggström J., Luis Fuentes V., et al. ACVIM consensus guidelines for the diagnosis and treatment of myxomatous mitral valve disease in dogs. J Vet Intern Med, 33(3): 1127–1140, 2019.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург