Введение
Термические ожоги с обширным поражением кожи приводят ко многим метаболическим и органическим изменениям в организме. Обширные ожоги – это чрезвычайно сложные медицинские случаи, сопровождающиеся патологиями работы дыхательной и сердечно-сосудистой систем, электролитными, метаболическими нарушениями, а также изменениями в работе иммунной системы и энергетических обменов в организме. Все эти процессы требуют правильного понимания их патофизиологии, чтобы обеспечить пациента необходимым лечением.Кожа выполняет различные функции в нормальной физиологии организма: является основным барьером для инфекций, поддерживает температуру тела, контролирует испарение жидкости. При ожогах все эти функции нарушаются, что в свою очередь само по себе может привести к гибели пациента (1).
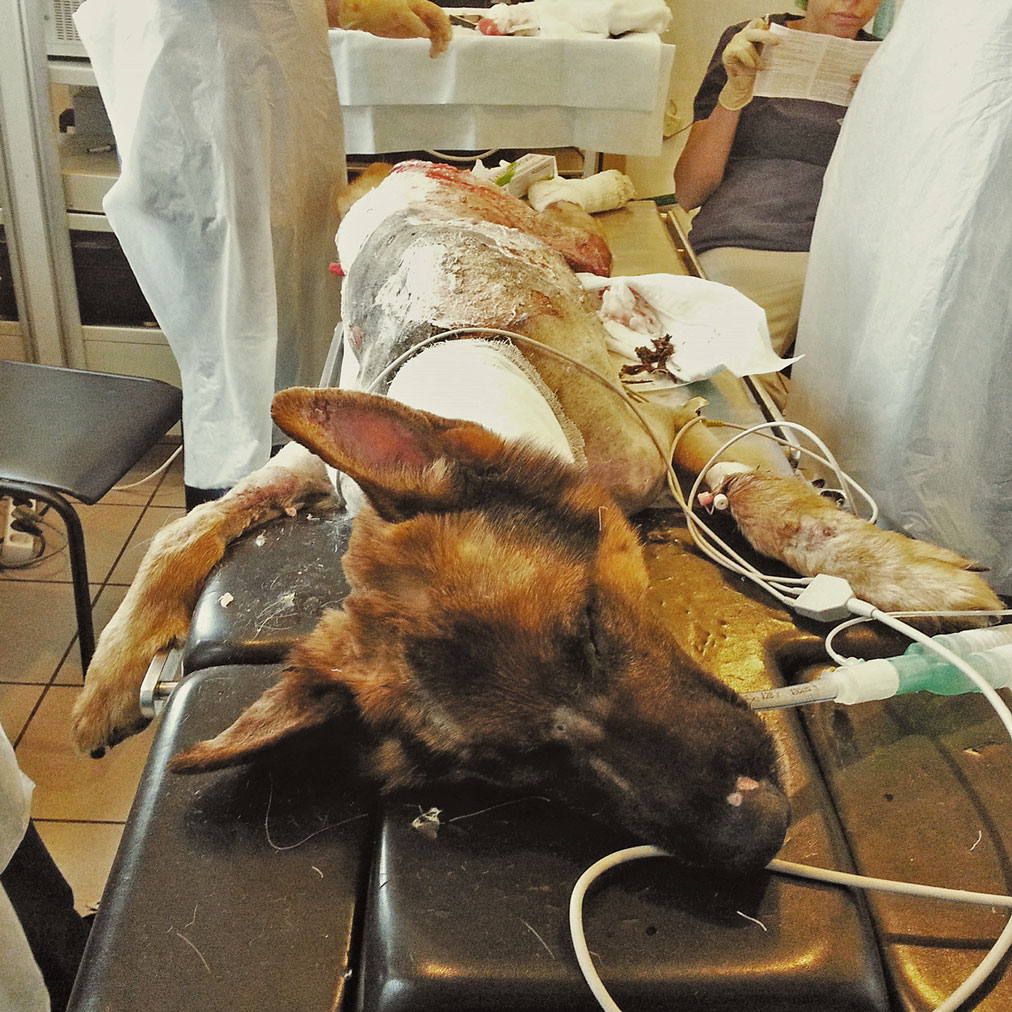
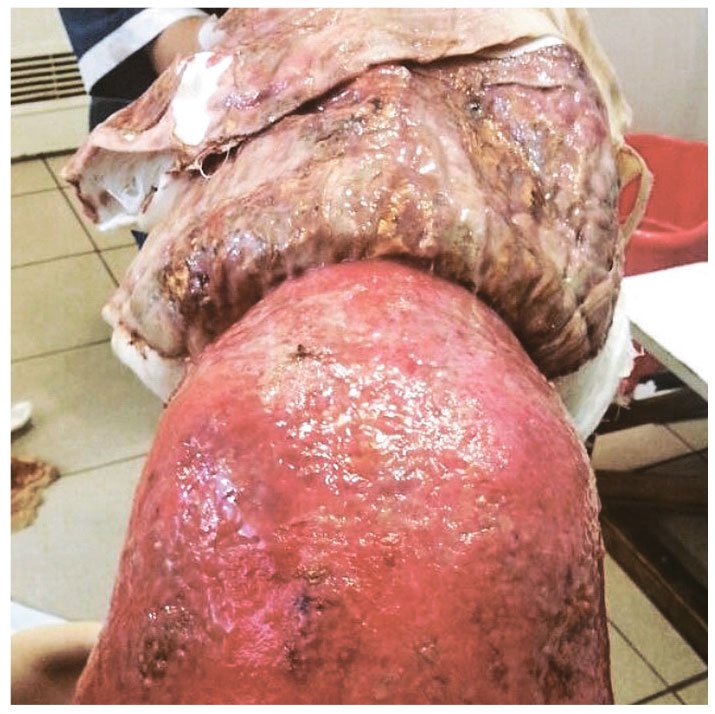
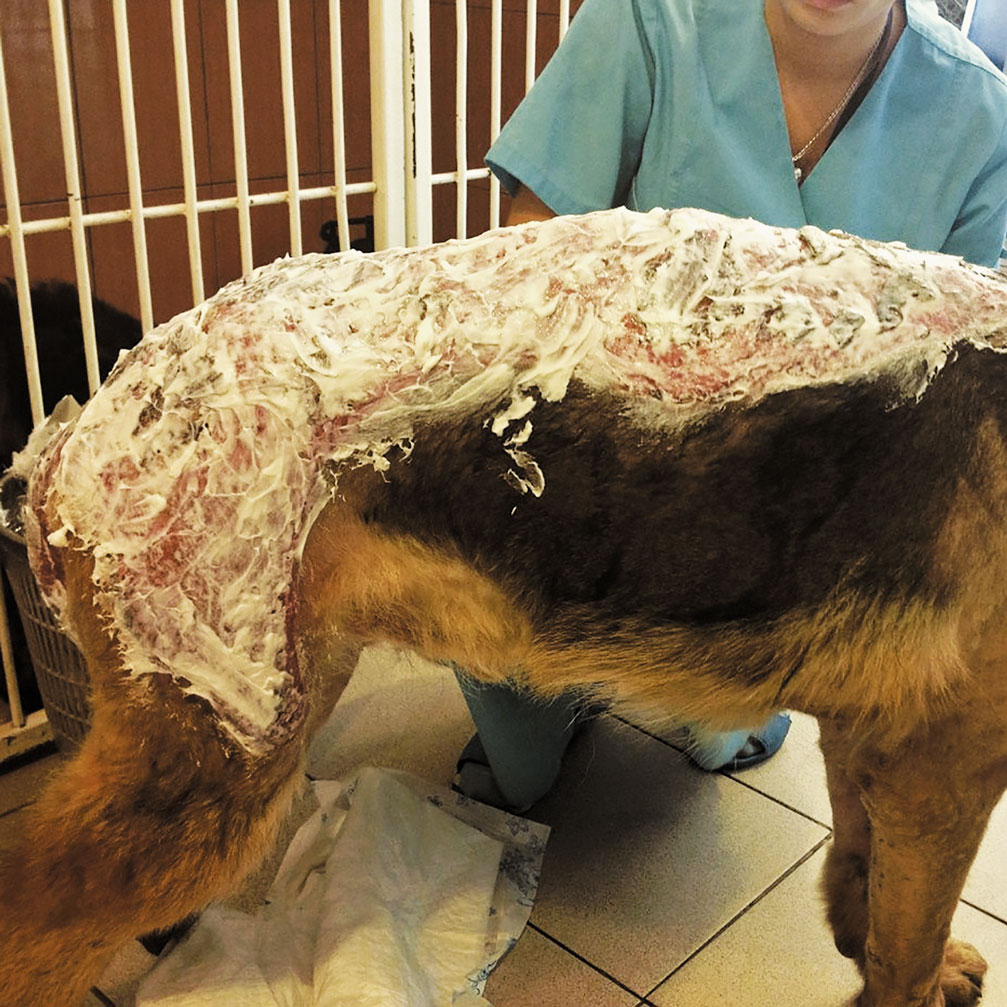
В качестве иллюстраций в статье использованы фотографии лечения и ухода за собакой породы немецкая овчарка по кличке Зет (возраст 5 лет), получившей ожоги во время пожара. Подробное описание данного клинического случая опубликовано в №2/2015 журнала «Ветеринарный Петербург» (Лечение пациентов с термическими ожогами. Хирургический подход).
Патофизиология ожогов
Патофизиология основных термических повреждений обусловлена серьезными метаболическими нарушениями в тканях ожоговой раны. При обширных ожогах (более 20% поверхности) второй и третьей степени могут возникнуть следующие проблемы:– отек легких (3);
– SIRS (синдром системного воспалительного ответа) (5);
– гиповолемический ожоговый шок (2);
– выпот жидкости из сосудов в межклеточное пространство;
– деструкция эритроцитов;
– миокардиальная депрессия (отрицательная инотропия, т.е. уменьшение сократимости миокарда);
– аритмии и сердечная недостаточность;
– послеожоговая пневмония;
– острая респираторная недостаточность и пневмония;
– иммуносупрессия с нарушением деятельности лейкоцитов, макрофагов и Т-лимфоцитов, ретикулоэндотелиальных клеток;
– нарушение баланса циркулирующей жидкости и электролитов;
– кислотно-щелочной дисбаланс;
– диссеминированное внутрисосудистое свертывание и тромбоэмболия;
– нарушение функций печени и почек;
– недостаточность адреналина;
– повышенная проницаемость слизистой оболочки желудка и кишечника с нарушением интестинального барьера;
– гастроинтестинальные изъязвления или трофические язвы Курлинга;
– ожоговый сепсис;
– гиперметаболизм;
– незаживающие раны;
– контрактуры;
– язвы Марголина (плоскоклеточная карцинома);
– образование рубцов;
– косметические дефекты(3).
Гипопротеинемия из-за потери белка является серьезной проблемой, а в сочетании с патологическим перераспределением жидкости в организме и гиповолемией вызывает тяжелый шок и гипотонию. Гиповолемия уменьшает сердечный выброс, что приводит к снижению перфузии органов и тканей, а также к клеточной гипоксии. Многие органы и ткани страдают одновременно. Почки особенно чувствительны к снижению артериального давления. Острая почечная недостаточность является частым осложнением у тяжелых пациентов, профилактика и мониторинг этой патологии обязательно должны быть включены в протокол диагностики и лечения пациентов с ожогами. Кроме того, постоянные гиповолемия и гипотония могут привести к острой ишемической недостаточности других органов, таких как легкие, печень и желудочно-кишечный тракт (1).
Термические ожоги вызывают сильную боль, ощутимую даже при поражении всей толщины кожи с разрушением ноцицепторов. Период гипометаболизма сразу после травмы сменяется периодом гиперметаболизма, в ходе которого расход энергии увеличивается более чем на 100% по сравнению с нормой. Это происходит вследствие нарушения барьерной функции кожи: большое количество воды из организма испаряется, а вместе с ней и значительная часть тепла. После ожогов центр терморегуляции в гипоталамусе повышает температуру тела на 1–2 °С в ответ на высвобождение цитокинов и эйкозаноидов в процессе развития воспаления. Из-за усиленного термогенеза увеличивается расход энергии.
Белковый и углеводный обмены также изменяются после ожогов. Для производства энергии увеличивается расход аминокислот, таким образом, вследствие процессов катаболизма теряется мышечная масса. Эта отрицательная энергия и азотистый баланс организма существенно отличаются от простого голода. При простом голодании организм обеспечивает свои потребности за счет жировой ткани на 90%, на долю мышечной массы тела приходится лишь 5–8%. В пост-ожоговом периоде развивается относительная инсулинорезистентность, вызванная повышением катаболических гормонов (глюкагона, кортизола и катехоламинов). Это приводит к совершенно иному механизму потребления энергии: только 50% энергетических потребностей организма обеспечиваются за счет жировой ткани и 30% – за счет мышечной массы тела (5).
Классификация по периодам оказания экстренной помощи пациенту:
1. От момента прибытия (происшествия) до 36 часов.2. Ранний период: от 36 часов до 5 дней.
3. Период воспаления/инфицирования: после первых 7 дней (1).
1. Первая стадия
Первоначальная оценка состояния должна включать физикальное обследование, выявление системных изменений, определение площади поражения кожных покровов, а также степени локального повреждения. В медицине большинство случаев с летальным исходом связаны с падением концентрации кислорода в окружающей среде, вдыханием окиси и двуокиси углерода, а также с токсичностью цианида. Подобные ситуации редко встречаются среди случаев с мелкими животными, вероятно, по причине того, что они, находясь почти на уровне пола, не страдают от отравления угарным газом.Отравившиеся угарным газом животные должны быть обеспечены 100%-ным кислородом сразу после прибытия в отделение интенсивной терапии. Вдыхание горячего воздуха и тепла может привести к обструкции верхних дыхательных путей и, как следствие, к развитию отека в соответствующих структурах.
Ранняя интубация трахеи имеет решающее значение в оказании первой помощи пациенту и должна быть выполнена сразу после физикального обследования, если были выявлены признаки ожога дыхательных путей или признаки развития острого респираторного дистресс-синдрома (ОРДС). Важно учитывать, что пульсоксиметрия будет необъективна для оценки степени гипоксемии, потому что этот метод не способен отличить гемоглобин от карбоксигемоглобина (1).
Пациенту следует незамедлительно обеспечить подачу кислорода со скоростью 100–150 мл/кг в минуту, а также ввести центральный венозный катетер в яремную вену. Необходимо возместить потери жидкости ИПС - 4 мл/кг в час для собак и 2 мл/кг в час для кошек. Препаратами первого выбора являются изотонические кристаллоиды, сбалансированные по электролитному составу, такие как Рингера лактат или физиологический раствор. Избегайте введения растворов глюкозы, поскольку пациенты с ожогами склонны к гипергликемии и глюкозурии (1).
Ожоги на протяжении последующих 2–3 часов все еще продолжают распространяться на окружающие их ткани. Поэтому, чтобы предотвратить дальнейшую травматизацию, необходимо активно охладить поврежденную поверхность тела пациента. Сделать это можно, например, с помощью купания животного в холодной воде или стерильном 0,9%-ном растворе NaCl, а также посредством распыления охлаждающей жидкости на кожу пациента из пульверизатора. Орошение должно осуществляться под небольшим напором, чтобы не вызывать излишний дискомфорт у пациента. Оптимальная температура воды для этой процедуры – от 3 °C до 17 °C. Длительность манипуляции не должна превышать 30 минут, чтобы не привести к системной гипотермии. Не используйте лед как альтернативное средство охлаждения – это спровоцирует дальнейшее сужение сосудов, снижение микроциркуляции и усилит повреждение тканей (6).
В течение первых 24 часов вследствие разрушения клеток в обгоревших тканях обычно развивается серьезная гиперкалиемия, поэтому необходимо контролировать уровень калия, а также осуществлять мониторинг скорости образования мочи пациента, уровня белка в сыворотке крови, гематокрита, гемоглобина, электролитов и газов крови. Если развивается гипопротеинемия, следует добавить к инфузии свежую плазму или коллоиды. Ацидоз может быть скорректирован введением бикарбоната натрия. При падении у пациента уровня гематокрита ниже 20% и/или гемоглобина ниже 7 г/дл приступайте к гемотрансфузии или трансфузии эритроцитарной массы. Стремитесь к уровню гематокрита выше 30%.
После обезболивания пациента сбрейте шерсть вокруг ожоговых ран и обработайте раны антисептиком, например повидон-йодом или хлоргексидином. Удалите все некротические ткани, инородные материи и прочие загрязнения из раны. Ожоги первой или второй степени требуют перевязок и местного применения антибиотиков; препаратом выбора в данном случае будет мазь с серебром. При ожогах третьей степени участки некроза должны быть удалены в кратчайшие сроки, а раны – ежедневно обрабатываться. Поскольку это очень болезненная процедура, заранее подумайте о возможности обезболивания и седации пациента.
Под удаленными струпами должна визуализироваться здоровая грануляционная ткань. Системные антибиотики не проникают в струп, поэтому системная терапия всегда должна сочетаться с применением антибактериальных мазей и кремов. Гентамицин, Полимиксин, Неомицин, Бацитрацин, а также фторхинолоны весьма эффективны против контаминации ожоговых ран вторичной микрофлорой (1).
2. Ранний период
Этот период времени характеризуется переходом из фазы течения шока в фазу развития гиперметаболизма. Главными задачами на этой стадии являются:• решение проблем с легкими;
• стабилизация гемодинамики;
• правильный уход за ожоговыми ранами;
• контроль боли и беспокойства.
Основной проблемой легких обычно является обструкция дыхательных путей из-за теплового или химического ожога слизистой оболочки. Объективная ларингоскопия может быть очень полезной для оценки реального ущерба. Если доступна механическая вентиляция, то таким пациентам показана длительная интубация трахеи.
Также в этот период распространены кашель и увеличение производства мокроты, связанные с раздражением слизистой. Повреждение и нарушение работы ресничек приводит к развитию инфекций, таких как бактериальный трахеобронхит, пневмония или бронхопневмония. Бакпосев с определением чувствительности к антибиотикам секрета со слизистой дыхательных путей является первоочередным выбором для лечения этих осложнений.
Испарение влаги через ожоговые раны становится основной причиной жидкостных потерь. Оценка патологических потерь позволяет обеспечить пациента необходимой инфузионной терапией. Анемия вследствие разрушения эритроцитов, а также угнетения функции производства красного костного мозга является еще одним распространенным осложнением.
Для инфузионной терапии показаны растворы с добавлением 5% глюкозы и небольшого количества натрия, потому что на этой стадии уже нет серьезной гипонатриемии. Агрессивная инфузионная терапия в настоящее время не является оптимальным выбором. Нужно стремиться к среднему АД 60–70 мм рт. ст., к темпу диуреза 1–2 мл/кг/час. При назначении гемотрансфузии старайтесь достигнуть уровня альбумина около 2,5 г/дл, а гематокрита – более 30%.
Важно помнить, что вследствие ожогов у животных развиваются серьезные нарушения в работе иммунной системы, связанные со снижением активности клеточно-опосредованного иммунитета, угнетением функций нейтрофилов и гуморального иммунитета. С учетом всех этих изменений инфицирование ран является серьезным осложнением в ходе лечения пациентов с ожогами. Для осуществления контроля над конкретной инфекцией нужно провести биопсию материала из раны с посевом на чувствительность к антибиотикам. Очищение и иссечение раны, а также некрэктомия должны проводиться регулярно, полученный материал может быть использован для бакпосева.
Чрезвычайно важным является ограждение мелких животных с ожогами от стресса, беспокойства и боли (1).
3. Период воспаления/инфицирования
Для этого периода характерно развитие сепсиса, синдрома системного воспалительного ответа (ССВО) и септического шока. Очень важна адекватная пищевая поддержка (1). Первоначальная калорийность рациона должна исходить из расчета энергетических потребностей пациента в покое. Диета должна быть высококалорийная, с большим количеством белка; объем корма может быть увеличен при хорошей переносимости диеты пациентом. Лучше всего, если пациент потребляет корм самостоятельно, но, если животное получает недостаточное количество корма, рекомендовано размещение эзофагостомического зонда или полное парентеральное питание. Чтобы компенсировать гипоперфузию желудочно-кишечного тракта и вторичное появление язв, назначают гастропротекторы, например Фамотидин 0,5–1 мг/кг перорально или внутривенно каждые 12–24 часа (4). Легочные инфекции и ОРДС остаются основной причиной смертности в этот период. При необходимости частичная ИВЛ может быть весьма полезна (1).Инфузионная терапия при термических ожогах
Существует формула расчета необходимой инфузионной терапии: 4 мл/кг массы тела × % TBSA (площадь поврежденной поверхности тела). Требования к назначению инфузионной терапии всегда должны быть адаптированы под каждого конкретного пациента. В первую очередь необходимо стремиться к стабильности гемодинамики (4), ЦВД 3–7 см водного столба (2) и диурезу 1 мл/кг/час (4). Терапия должна учитывать реакцию пациента на проводимое лечение, основные показатели состояния организма (пульс, дыхание, температура), ментальный статус, периодические анализы крови, анализ газов крови, ЦВД, диурез и анализы мочи.Коррекция скорости введения жидкостей должна основываться на периодическом измерении этих параметров.
Масса тела, объем выделяемой мочи, показатели гематокрита, уровень общего белка и альбумина сыворотки крови, электролиты, уровень мочевины крови и креатинин, уровень глюкозы в крови, определение газов крови, показатели осмоляльности сыворотки крови и мочи должны регулярно определяться для корректировки объемов вводимых жидкостей. Мочевину, гематокрит, общий белок и количество глюкозы в крови следует определять по несколько раз в день до тех пор, пока биохимический профиль не приобретет нормальный вид (3).
Контроль боли
Используйте такие наркотические препараты, как Морфин, Оксиморфон, Буторфанол и низкие дозы бензодиазепинов. Избегайте использования фенотиазинов ввиду риска развития у пациентов таких побочных эффектов, как экстрапирамидные расстройства (1). Чаще всего трудно достичь полного комфорта пациента, и в большинстве случаев требуется комплексная терапия. Инфузии с постоянной скоростью (ИПС) играют важную роль в поддержании непрерывного обезболивания пациентов с ожогами. Это можно осуществить, используя специальные капельные дозаторы (buretrol) или шприцевые насосы, но только под постоянным наблюдением. При различных нейропатических болях ИПС ненаркотических анальгетиков можно сочетать с наркотическими ИПС. Для последовательного введения или непрерывной инфузии анальгетиков могут быть использованы эпидуральные катетеры. Пациентам с ожоговыми повреждениями нижней трети туловища, ниже поясничной области показана эпидуральная анестезия (6).Обезболивание ожоговых пациентов должно быть обеспечено с помощью чистых μ-агонистов, таких как Фентанил (3–10 мкг/кг/ч, ИПС), Гидроморфон (0,025 мг/кг/ч, ИПС) или Морфин (0,5–1 мг/кг, подкожно каждые 4 часа). Лидокаин (1,5–3 мг/кг/ч, ИПС) может быть использован в качестве как дополнительного, так и самостоятельного анальгетика у собак, у кошек его следует использовать с особой осторожностью. Кетамин (загрузочная доза 0,5 мг/кг внутривенно; поддерживающая доза 2–5 мкг/кг/мин, ИПС) и Габапентин (7–10 мг/кг, внутрь каждые 12 часов) также показаны для обезболивания ожогов. Габапентин – это препарат, направленный против гипералгезии, который избирательно действует на чувствительность центральной нервной системы. Адекватное обезболивание пациентов с ожогами должно быть мультимодальным, сочетая в себе купирование ноцицептивной и нейропатической боли одновременно (2).
Дополнительные клинические наблюдения
У целого ряда направленных к нам пациентов, площадь ожоговой поверхности которых определялась как 20% и более, отмечалось вполне стабильное состояние (часто через несколько дней после ожога) несмотря на то, что инфузионная терапия не проводилась или проводилась в недостаточном объеме. Это может объясняться тем, что большинство собак и кошек имеют очень свободную, эластичную кожу и врачи могут преувеличить площадь обожженной поверхности.Надлежащую медикаментозную терапию следует проводить для того, чтобы как можно лучше подготовить организм пациента к проведению хирургического вмешательства, направленного на закрытие кожных дефектов (3).
Коррекция гиперметаболической фазы течения
В попытке ослабления гиперметаболического ответа организма на термическое повреждение было разработано несколько схем лечения. Для снижения катаболических эффектов, развившихся в результате термического повреждения, была успешно применена фармакологическая поддержка с помощью введения гормона роста, инсулиноподобного фактора роста-1 (IGF-1), оксандролона (анаболический стероид), тестостерона, инсулина и пропранолола. Эти методы находятся на ранних этапах развития в медицине, но вполне возможно, что ветеринарные врачи смогут достичь тех же положительных результатов назначения пропранолола, инсулина и оксандролона у своих пациентов в будущем. Тем не менее пока что не существует ветеринарных исследований, оценивающих применение этих препаратов у животных с ожогами, поэтому рекомендовать их к использованию преждевременно (2).
Выводы
Лечение термических поражений является активной областью исследований в медицине (2). Например, последний обзор 1818 пациентов, зарегистрированных в Бостонском ожоговом центре «Шрайнерс» (Shriners), выявил снижение смертности с 1991 по 1997 гг. на 88% по сравнению с периодом 1974–1980 гг., а также сокращение на 57% смертности в случаях с наиболее обширными ожогами (поражения от 60 до 100% поверхности тела). Эти успехи были отнесены к появлению агрессивной инфузионной терапии, ранней некрэктомии, улучшению качества профилактики сепсиса и контроля боли, а также назначению энтеральной поддержки пациентов (5).С исследованием патофизиологии воспаления при ожогах развиваются новые стратегии лечения. Хотя по этой теме в ветеринарной литературе существует очень мало публикаций, многое можно экстраполировать из исследований гуманной (человеческой) медицины. Понимание патофизиологии термической травмы является необходимым условием для разработки эффективных стратегий лечения (2).
Литература:
- Luis H. Tello, MV, MSc, DVM. Severe Burns in Small Animals. Proceedings of the 36th World Small Animal Veterinary Congress WSAVA. http://www.ivis.org/proceedings/wsava/2011/165.pdf
- Katie Frantz, DVM, Christopher G. Byers, DVM, DACVECC, DACVIM (SAIM). Thermal Injury. https://www.vetlearn.com/_preview?_cms.fe.previewId=9e302330-2503-11e1-816d-0050568d3693&WT.mc_id=AA...
- Michael M. Pavletic, DVM. Atlas of Small Animal Wound Management and Reconstructive Surgery. Third Edition. © 2010.
- Deborah C. Silverstein, Kate Hopper. Small animal critical care medicine. © 2009 by Saunders, an imprint of Elsevier Inc.
- Bojrab M. J., Monnet E. Mechanisms of Disease in Small Animal Surgery, Third Edition. Publisher: Teton NewMedia, Jackson, WY, USA ( www.tetonnm.com/). Internet Publisher: International Veterinary Information Service, Ithaca NY (www.ivis.org). Burns M. Bohling and S. F. Swaim. Last updated: 21-May-2014. http://www.ivis.org/advances/bojrab/chap62/chapter.asp?LA=1
- Donohoe C. Thermal Burns. NAVC Proceedings 2007, North American Veterinary Conference (Eds). Publisher: NAVC ( www.tnavc.org). Internet Publisher: International Veterinary Information Service, Ithaca NY ( www.ivis.org), Last updated: 13-Jan-2007. http://www.ivis.org/proceedings/navc/2007/VT/024.asp?LA=1



 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург