Введение
Атриовентрикулярная блокада – это нарушение проводимости импульсов через атриовентрикулярный (АВ) узел, которое может быть постоянным или преходящим. Предсердные импульсы могут проводиться с задержкой или полностью блокироваться в АВ-узле в зависимости от анатомических или функциональных нарушений проводящей системы.Различают следующие виды нарушения атриовентрикулярной проводимости:
- Атриовентрикулярная блокада 1-й степени,которая характеризуется замедлением проведения электрического импульса по АВ-узлу и выражается в удлинении интервала PQ, длительность которого составляет 0,06–0,13 сек. у собак и 0,05–0,09 сек. у кошек (рис. 1).
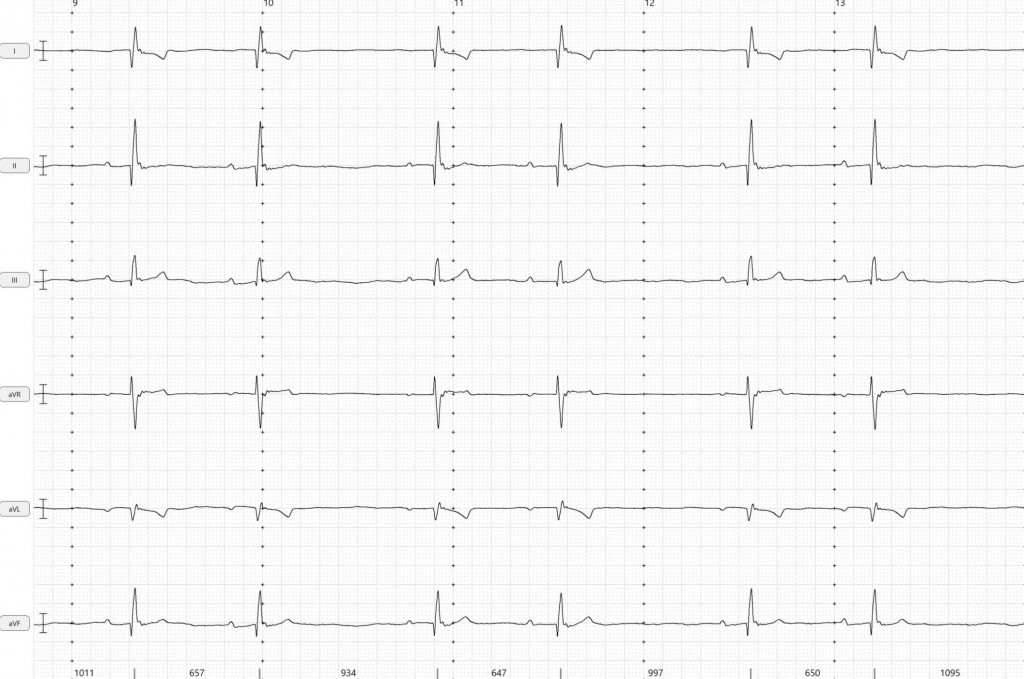 Рис. 1. Атриовентрикулярная блокада 1-й степени у собаки. Интервал PQ удлинен и составляет 0,14 сек.
Рис. 1. Атриовентрикулярная блокада 1-й степени у собаки. Интервал PQ удлинен и составляет 0,14 сек.
- Атриовентрикулярная блокада 2-й степени характеризуется преходящим нарушением АВ-проводимости, которая характеризуется периодическим выпадением комплекса QRS. Каждое второе проведение деполяризации через АВ-узел выражается в виде соотношения 2:1, каждое 3-е, 4-е – 3:1, 4:1, что является АВ-блокадой высокой градации.
- Тип Мобитц I (типичный Венкебах), который, чаще всего, имеет физиологические причины. Его характерной чертой является постепенное удлинение интервала PQ и сокращение длительности интервала RR, которые предшествуют полному выпадению комплекса QRS, после чего интервал PQ укорачивается.
- Тип Мобитц II – периодическая блокада; интервал РQ имеет постоянную длину нормальной или увеличенной длительности.
- Блокада 2:1, при которой каждый второй импульс от предсердий достигает желудочков;
- АВ-блокада 2-й степени высокой градации, при которой каждый третий или каждый четвертый и т. д. импульс достигает желудочков (проводится через АВ-узел). Комплексы QRS могут быть неправильной формы, что свидетельствует об одновременной блокаде ножек пучка Гиса.
- Атриовентрикулярная блокада 3-й степени характеризуется полным отсутствием проведения через АВ-узел, когда ни один импульс из предсердий не достигает желудочков. На ЭКГ отражается полная диссоциация зубцов Р с комплексами QRS. Желудочковый ритм происходит из нижележащих участков проводящей системы (пучок Гиса, волокна Пуркинье). Частота сокращений желудочков, чаще всего, значительно ниже частоты сокращений предсердий (рис. 2).
Нередко атриовентрикулярная блокада у собак во второй половине жизни является дополнительным проявлением дегенеративного заболевания проводящей системы сердца – синдрома слабости синусового узла (СССУ)2.
Синдром слабости синусового узла – это генерализованное заболевание проводящей системы сердца. Синдром характеризуется различной степенью дисфункции синоатриального (СА) и/или атриовентрикулярного узла и часто сопровождается снижением (нарушением) автоматизма вторичного водителя ритма. У пациентов с СССУ может возникать асистолия в результате остановки СУ. Синдром слабости синусового узла может иметь ряд проявлений, таких как периоды наджелудочковой тахикардии, чередующихся с брадиаритмией, поэтому он получил название «синдром бради-тахи».
СССУ был описан у людей и собак. Наиболее частой причиной возникновения патологии у людей является идиопатический дегенеративный фиброз ткани синусового узла. При этом патогенез может быть многофакторным, поскольку также описаны дегенерация артерии синусового узла, изменения иннервации или регуляции CА-узла, антитела к белкам в СА-узле и изменения ионных каналов внутри СА-узла.
Природа СССУ у собак, чаще всего, носит идиопатический характер. Предполагается, что генетически предрасположены к этому заболеванию представители таких пород, как вест-хайленд-уайт-терьер, миниатюрный шнауцер и кокер-спаниель, от среднего до пожилого возраста10,7.
В зависимости от средней суточной ЧСС симптомы могут варьироваться от отсутствия каких-либо признаков до частых эпизодов синкопе, снижения переносимости малейших нагрузок и даже ремоделирования камер сердца.
Клинический случай
На прием к врачу-дерматологу обратились владельцы 19-летней собаки породы американский кокер-спаниель с массой тела 10 кг. Причиной обращения было наличие хронического отита у питомца. Ранее в сторонней клинике собаке была проведена отопластика левого наружного слухового прохода. На момент приема на постоянной основе использовали препарат «Отибиовин». Также владельцы наблюдали значительное снижение толерантности к нагрузкам, которое они связывали с возрастом собаки. Одышки, кашля у питомца владельцы не замечали, аппетит был хороший, жалобы на рвоту и диарею отсутствовали.При проведении отоскопии врач-дерматолог обнаружил следующее:
в правом ухе – стеноз наружного слухового канала, наличие выраженной гиперплазии тканей;
в левом ухе – наличие гнойного отделяемого при надавливании на ушную раковину (отоскопия была затруднена).
Результаты микроскопии мазков из ушей: правое ухо – малассезия ++, кокки ++; левое ухо – малассезия +++, кокки ++ и нейтрофильное воспаление.
Был рекомендован прием у хирурга для планирования дальнейшей тактики лечения.
Результаты осмотра пациента хирургом:
Правый наружный слуховой проход (НСП) – экссудация незначительная. Вход в НСП значительно сужен, наблюдается выраженная гиперплазия кожи наружного слухового хода. В глубине видны изгибы ушного хряща, слуховой канал – без признаков оссификации.
Левый наружный слуховой проход (ранее была проведена отопластика наружного слухового хода по Хинцу) – диаметр входа в горизонтальную часть – около 4–5 мм, из просвета выделяется мутный экссудат (гной?), слуховой канал – без признаков оссификации.
Рекомендовано проведение видеоотоскопии с возможной последующей резекцией левого наружного слухового канала. Поскольку данная процедура осуществляется под общей анестезией, перед ее проведением пациенту были назначены общий клинический и биохимический анализы крови, а также консультация анестезиолога. В полученных результатах анализа крови не было выявлено значимых отклонений
При аускультации грудной клетки собаки в течение одной минуты анестезиолог не выявил патологических шумов, но зафиксировал низкую частоту сердечных сокращений (около 36 уд/мин) и два внеочередных сокращения.
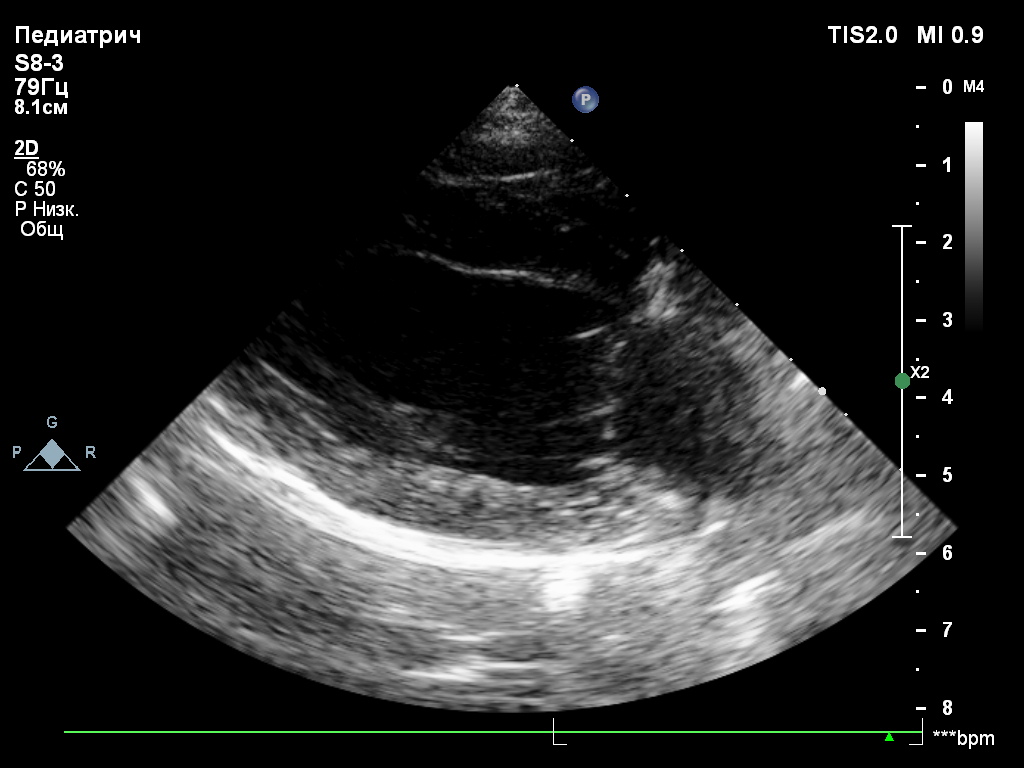
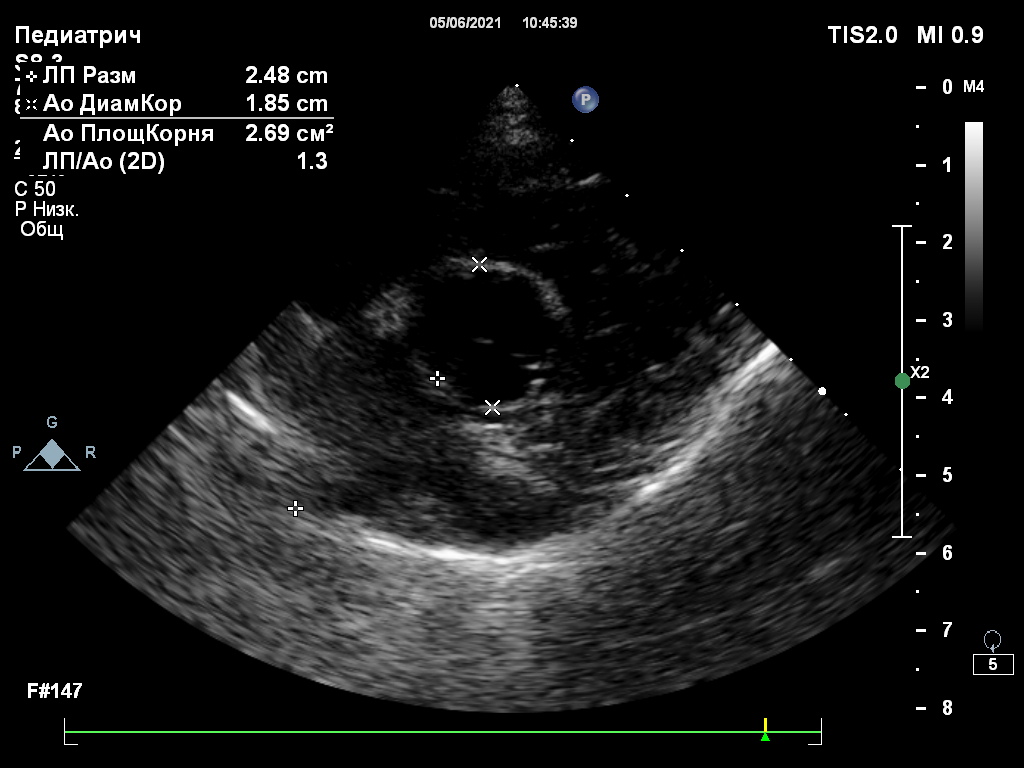
Следующим этапом был рекомендован прием у кардиолога: была проведена эхокардиография, по результатам которой не было обнаружено изменений геометрии камер и каких-либо признаков застойной сердечной недостаточности, а также признаков новообразований сердца и смежных структур (рис. 3, 4).
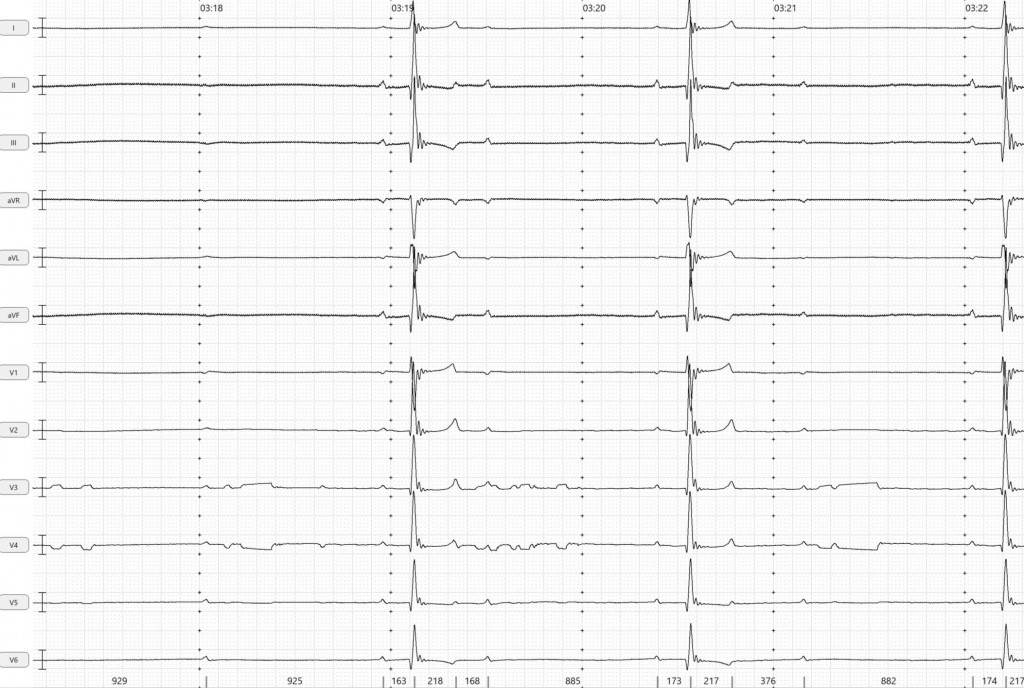
Результаты электрокардиографии (представлены на рис. 5):
ЧСС – 30–46 уд/мин (референтный интервал для собак: 60–180 уд/мин)
Ритм – синусовая брадикардия
QRS – 0,06 сек. (< 0,07 сек.)
Регулярность RR – регулярные
ЭОС – +60 (+40–100)
Р – 0,04 сек. (< 0,04 сек., для гигантских пород: < 0,05 сек.)
Р – 0,3 mV (< 0,4 мВ, для гигантских пород: < 0,5 мВ)
PQ – 0,15 сек. (< 0,13 сек.)
QT – 0,22 сек. (0,15–0,22 сек.)
Q – 0,5 mV
R – 2,4 mV (< 3 мВ)
Тa-волна – присутствует
Т – 0,4 mV
ST-сегмент изоэлектричен
Заключение: брадиаритмия с ЧСС 30–46 уд/мин, ЭОС не отклонена, признаки нарушения ритма в виде одиночных левожелудочковых экстрасистол (ЛЖЭС), признаки нарушения проводимости в виде АВ-блокады 2-й степени высокой градации (2:1, 3:1), эпизоды остановки синусового узла.
Дифференциальные диагнозы: синусовая брадикардия (вагус-индуцированная?); СА-блокада; остановка СУ (СССУ).
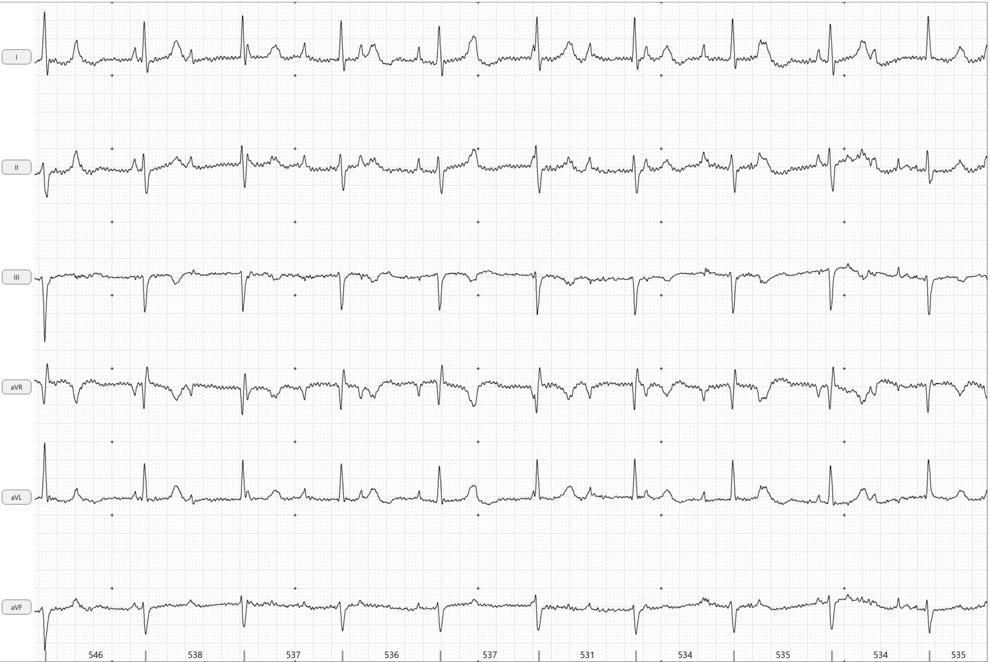
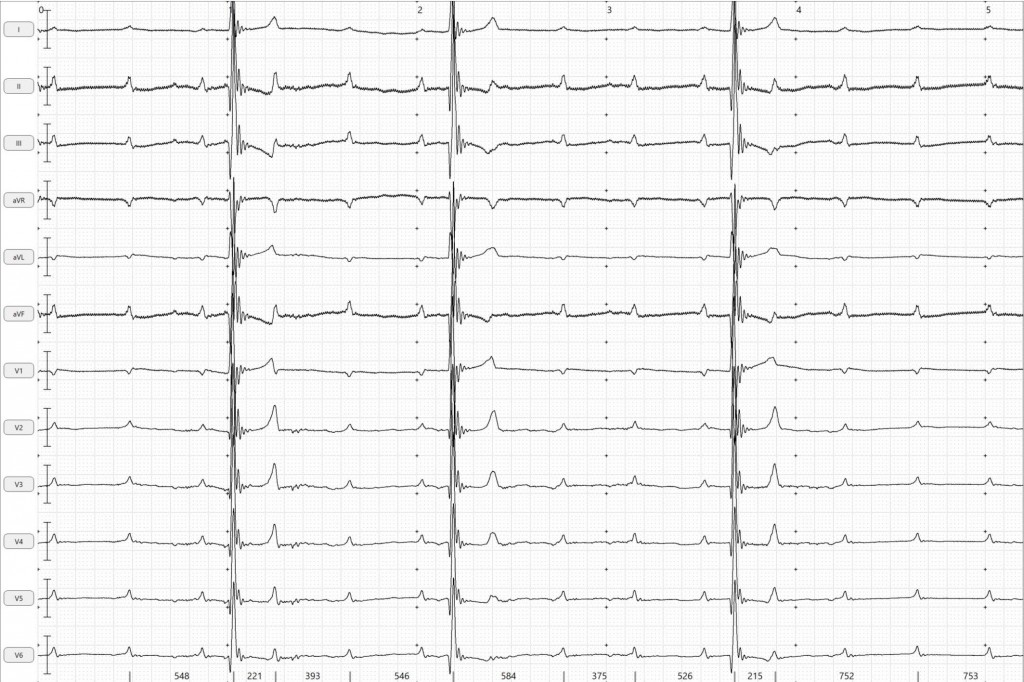
Далее был проведен тест с атропином – 0,04 мг/кг подкожно, после которого через 40 минут наблюдался относительный положительный эффект – синусовый ритм с ЧСС – 100 уд/мин, с сохраняющейся АВ-блокадой 2-й степени (2:1) (рис. 6, 7).
Гериатрический пациент породы кокер-спаниель с подобными характеристиками ЭКГ с высокой долей вероятности может иметь СССУ. Золотым стандартом для подтверждения диагноза является суточный мониторинг ЭКГ по Холтеру. Вагус-индуцированная синусовая брадикардия также может быть в списке дифференциальных диагнозов, поскольку собака имеет хронический отит, который является причиной постоянного раздражения/стимуляции блуждающего нерва. Хроническое раздражение блуждающего нерва также является одной из причин дисфункции синоатриального узла.
Блуждающий нерв отдает краниальные и каудальные сердечные ветви. Окончания парасимпатических нервов распределяются в основном в области СА и АВ узлов, в меньшей степени – в миокарде предсердий, и совсем мало их в миокарде желудочков, поэтому стимуляция парасимпатических нервов способна замедлить и даже блокировать сердечный ритм. При стимуляции вагуса происходит выделение медиатора ацетилхолина из нервных окончаний. Ацетилхолин оказывает два основных влияния на сердце: замедление синусового ритма и уменьшение возбудимости волокон АВ-проводящей системы, что приводит к замедлению передачи импульса от предсердий к желудочкам.
Этот медиатор увеличивает проницаемость клеточных мембран для ионов калия. Последние проникают из проводящих волокон во внеклеточную жидкость, что приводит к увеличению отрицательного заряда внутри клетки (гиперполяризации). Таким образом, возбудимость проводящих волокон снижается, и частота сердечных сокращений уменьшается. Также оптические измерения мембранных потенциалов в исследованиях собак6 показали, что изопротеренол (ISO) ускоряет синусовый ритм, тогда как ацетилхолин (ACh) имеет противоположное действие – оказывает отрицательные хронотропный и дромотропный эффекты. Более того, перфузия ISO и ACh обычно приводит к предпочтительному использованию верхних или нижних (быстрых или медленных) путей проведения предсердий, соответственно, нижний и верхний пути могут иметь разные проводящие свойства и различную чувствительность к вегетативным стимуляциям. Выделение ацетилхолина во время тахикардии может объяснять механизм возникновения пауз после тахиаритмий (синдром бради-тахи при СССУ).
Рекомендуемая терапия
При СССУ может быть использована пробная терапия препаратами из группы ингибиторов фосфодиэстеразы («Теофиллин» 10 мг/кг каждые 24 ч), но присутствует риск прогрессирования дегенеративного процесса проводящей системы сердца, поэтому оптимальным лечением является имплантация электрокардиостимулятора (ЭКС). Основным показанием к установке ЭКС является следующая клиническая картина: преходящая потеря сознания, слабость и непереносимость физической нагрузки вследствие установленной тяжелой брадикардии7. Данный метод лечения значительно улучшает качество жизни питомцев.Владельцы пациента из данного клинического случая, к сожалению, отказались как от пробного консервативного лечения, так и от имплантации электрокардиостимулятора. Дальнейшая судьба этой собаки нам неизвестна.
Выводы
При осмотре пациентов во время аускультации сердца важно обращать внимание не только на наличие патологических шумов, но и на ЧСС и регулярность ритма. Также важно помнить о генетической предрасположенности к СССУ во второй половине жизни у представителей пород группы риска: вест-хайленд-уайт-терьеров, миниатюрных шнауцеров, кокер-спаниелей.При выявлении брадикардии у пациента и отсутствии факторов, вызывающих снижение ЧСС (гипотермия, влияние опиоидных препаратов, метаболические нарушения, такие как гиперкалиемия, гипотиреоидизм), рекомендуется проводить ЭКГ, ЭхоКГ.
Для исключения вагус-индуцированной брадикардии проводят тест с атропином (0,04 мг/кг подкожно). Результат считается положительным, если ЧСС повышается от 150 уд/мин и больше, частичным – при повышении ЧСС на 25%, отрицательным – при отсутствии изменений ЧСС. В случае положительного результата может быть назначена медикаментозная терапия (см. выше) и должны быть исключены причины, вызывающие стимуляцию блуждающего нерва. При отрицательном ответе на атропин и при наличии симптомов, связанных с критически низкой ЧСС рекомендована имплантация ЭКС.
Список использованной литературы:
- Медицинская физиология / А. К. Гайтон, Дж. Э. Холл / Пер. с англ.; Под ред. В. И. Кобрина. – М.: Логосфера, 2008. – 1296 с.
- Электрокардиография собак и кошек. Формирование и интерпретация сердечного ритма – Сантилли Р., Перего М., Аквариум, 2017. – 280 с.
- Saunders A. B., Gordon S. G., Rector M. H., DeMaster A., Jackson N., et al. Bradyarrhythmias and pacemaker therapy in dogs with Chagas disease. Vet Intern Med, Jul-Aug 2013.
- Kalyanasundaram A., Li N., Hansen B. J., Zhao J., Fedorov V. V. Canine and human sinoatrial node: Differences and Similarities in Structure, Function, Molecular Profiles and Arrhythmia. J Vet Cardiol, Apr 2019.
- Vadim V. Fedorov, Roger Chang, Alexey V. Glukhov, Geran Kostecki, Richard B. Schuessler, Igor R. Efimov. Complex interactions between the sinoatrial node and ftrium during reentrant arrhythmias in the canine heart. Circulation, 2010.
- Vadim V. Fedorov, Alexey V. Glukhov and Roger Chang. Conduction barriers and pathways of the sinoatrial pacemaker complex: their role in normal rhythm and atrial arrhythmias. «Circulation» 01 May, 2012.
- Santilli R. A., Giacomazzi F., Porteiro Vázquez D. M., Perego M. Indications for permanent pacing in dogs and cats. J Vet Cardiol, Apr 2019.
- Heather Burrage. Sick sinus syndrome in a dog: Treatment with dual-chambered pacemaker implantation. Can Vet J, May 2012.
- Alexey V. Glukhov, Lori T. Hage, Brian J. Hansen, Adriana Pedraza-Toscano, et al. Sinoatrial node reentry in a canine chronic left ventricular infarct model: role of Intranodal fibrosis and heterogeneity of refractoriness. Arrhythmia and Electrophysiology, 2013.
- Machida N., Hirakawa A. J. The Anatomical Substrate for Sick Sinus Syndrome in Dogs. Comp Pathol, Epub Nov 20, 2021.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург