Автор: Каратаев Павел Сергеевич, ветеринарный врач, невролог, ВК «Zоолюкс», г. Киев.
Дополнительная диагностика пациентов с ЧМТ
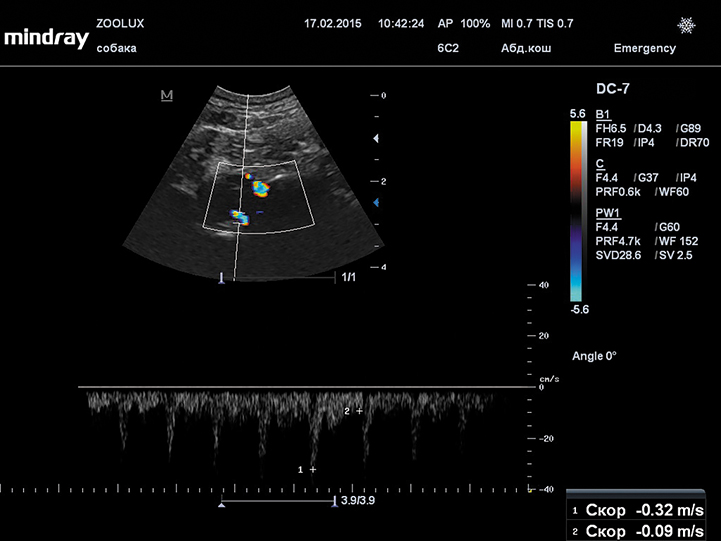
Рентген головы может помочь выявить переломы черепа (рис. 10), но не дает никакой информации относительно состояния паренхимы мозга. Рентген позвоночника поможет определить или исключить возможные сопутствующие переломы.УЗИ головного мозга можно провести через костные дефекты или через затылочное отверстие. С помощью данного метода диагностики на ранних стадиях выявляются гипоэхогенные гематомы, которые со временем могут становиться гиперэхогенными.
Также с помощью допплерографии можно косвенно оценить внутричерепное давление, измеряя индекс резистентности базилярной артерии. Индекс резистентности повышается при повышении ВЧД. Очень важным является его измерение в динамике в процессе лечения пациента [7, 15]. Индекс резистентности (ИР) можно высчитать по формуле: ИР = систолическая скорость – диастолическая скорость / систолическая скорость (рис. 11).
КТ позволяет хорошо визуализировать костные структуры, а также гематомы в острый период (рис. 12), сильный отек или изменения в размере желудочков, смещение срединной линии и др. Также с помощью режима 3D-реконструкции возможно более тщательное хирургическое планирование лечения переломов. Преимуществом данного метода перед МРТ является быстрота его проведения.
МРТ позволяет очень хорошо визуализировать мягкие ткани головного мозга. В зависимости от проявлений на МРТ можно выделить 6 степеней поражения (от 1 – нормальная структура мозга, до 6 – двустороннее поражение ствола мозга). Степень проявления поражений на МРТ коррелирует с тяжестью симптомов (рис. 13) [6].
А – степень 1 – нормальная паренхима. В – степень 2 – поражение затрагивает полушария мозга, мозжечка (или оба) без сдвига средней линии. С – степень 3 – поражение затрагивает только полушария мозга, мозжечка (или оба) со сдвигом средней линии. D – степень 4 – поражение затрагивает таламус, мозолистое тело, базальные ядра с наличием или отсутствием других поражений (характерных для других степеней). Е – степень 5 – унилатеральное поражение ствола мозга с наличием или отсутствием других поражений. F – степень 6 – билатеральное поражение ствола мозга с наличием или отсутствием других поражений.
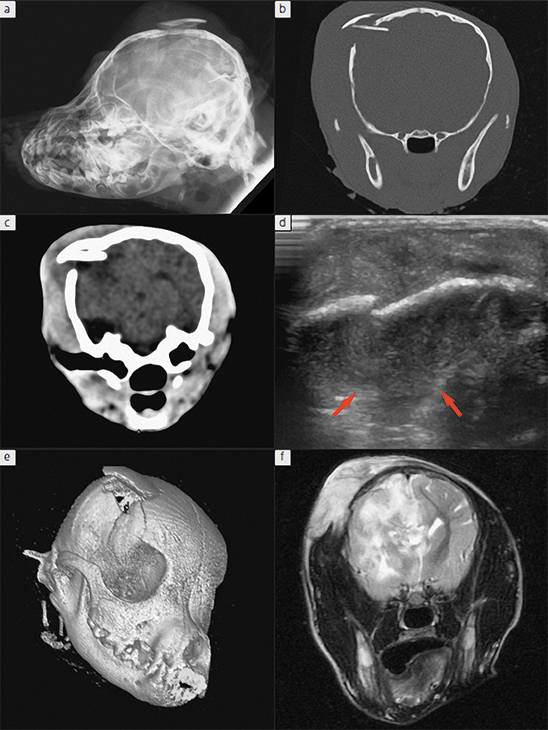
На рис. 14 показано сравнение разных исследований головного мозга у одного пациента. На рентгене можно увидеть перелом черепа, но нельзя оценить паренхиму головного мозга, а также точно назвать количество осколков. На КТ (b, c, e) уже видно, что есть 2 осколка, а также в мягкотканном режиме видно наличие гипоинтенсивного сигнала под этими осколками, что может быть связано с отеком. На УЗИ также виден гипоэхогенный участок, что говорит об отеке/гематоме. И только на МРТ можно четко оценить структуру головного мозга, наличие сильного отека, срединного смещения и т.д. Измерение ВЧД часто используется в гуманной медицине, но в ветеринарной медицине использование этого метода пока ограничено.
Лечение ЧМТ
После выявления всех сопутствующих жизнеугрожающих состояний нужно приступать к консервативному лечению ЧМТ, которое включает в себя борьбу с вторичными повреждениями.Обязательными являются контроль температуры, ЧСС, ЧДД, артериального давления, сатурации крови, а также гликемии. Следует избегать как гипо-, так и гипергликемии. Выявлено, что уровень гипергликемии коррелирует с тяжестью ЧМТ. Повышенный уровень глюкозы может ухудшать неврологический статус пациента, поэтому также стоит избегать ятрогенной гипергликемии [2]. Глюкозу пациентам с ЧМТ нужно вводить только при подтвержденной гипогликемии.
Пациент с политравмой также нуждается в адекватном обезболивании.
При возникновении у пациента с ЧМТ судорог после травмы необходима их терапия. В случае эпистатуса нужно также действовать по протоколу лечения эпистатуса (диазепам 0,5–2 мг/кг внутривенно, фенобарбитал 2–4 мг/кг внутривенно; инфузия пропофола. Более подробную информацию можно найти в соответствующих руководствах).
Использование стероидов (преднизолона, дексаметазона) при ЧМТ не рекомендовано в гуманной и ветеринарной медицине, т.к. в исследованиях выявлено увеличение количества летальных исходов и вероятности развития инвалидности у людей [8].
Предложена схема интенсивного 3-уровневого лечения пациентов с ЧМТ. Первый уровень применяется для всех пациентов. Второй – для пациентов с оценкой менее 8 (по модифицированной шкале комы Глазго) и при отсутствии улучшений на первом уровне. Третий – для пациентов с оценкой менее 8 и при отсутствии улучшений на втором уровне.
Уровень 1
Достижение нормоволемии (среднее АД 80–100 мм рт. ст.) у пациентов с ЧМТ осуществляется посредством жидкостной терапии. Для этого используется протокол низкообъемной инфузии (low-volume fluid resuscitation), который заключается в комбинации введения гипертонических кристаллоидных растворов и синтетических коллоидов. Гипертонические кристаллоидные растворы показали очень хорошие результаты в снижении ВЧД при транстенториальной грыже мозга, также они улучшают мозговой кровоток [3].Гипертонические растворы (4–5 мл/кг 7%-ного физраствора, введенного в течение 5–10 минут) быстро повышают объем циркулирующей крови, за счет своей гипертоничности вызывая переход жидкости из интерстициального пространства в сосуды. Противопоказанием к их использованию являются дегидратация, гипернатриемия.
Коллоидные растворы (5–10 мл/кг, введенных в течение 5–10 минут) содержат крупные молекулы, которые долго удерживают жидкость в сосудистом русле. Использование такой комбинации позволяет добиться повышения давления на достаточно длительное время. При отсутствии эффекта повышения давления используются вазоконстрикторы (допамин).
Очень важным является положение пациента. Размещать его необходимо на ровной поверхности, наклоненной под углом 30 градусов, головой вверх (рис. 15). При этом нельзя ничего подкладывать под голову, т.к. пережатие яремных вен приведет к повышению ВЧД и может вызвать ухудшение неврологического состояния. Такое положение пациента снижает ВЧД без снижения мозгового кровотока [4, 11, 13].
Кислородная поддержка является очень важной частью лечения пациентов с ЧМТ. Контроль уровня кислорода и углекислого газа осуществляется с помощью пульсоксиметрии, капнографии и газов крови. Цель кислородной и дыхательной поддержки – достичь РаO2 более 90 мм рт. ст., РаCO2 – 35–40 мм рт. ст. Доставку кислорода можно осуществлять с помощью кислородной камеры или маски. Нужно помнить, что страх при использовании масок или чихание при использовании назальных катетеров может приводить к повышению ВЧД и ухудшению неврологического состояния.
Уровень 2
Когда состояние пациента изначально тяжелое (менее 8 баллов) или нет улучшений от предыдущего лечения, возможно использование осмотических диуретиков. Вводить их можно только после нормализации давления.После внутривенного введения маннитол увеличивает ОЦК, улучшает реологические свойства крови и, как следствие, доставку кислорода к мозгу. Также он связывает свободные радикалы, вследствие осмотического эффекта снижает количество жидкости в интерстициальном пространстве, что приводит к снижению ВЧД.
Маннитол (0,5–2 г/кг) вводится болюсно в течение 15–20 минут. При использовании меньших доз осмотический эффект также будет выражен, но с меньшей продолжительностью. Маннитол снижает отек головного мозга через 15–30 минут после введения, его эффект длится около 2–5 часов. Частое введение маннитола может вызвать усиление диуреза, снижение ОЦК, увеличение осмолярности, дегидратацию, гипотензию, ишемию. Поэтому рекомендовано параллельное введение кристаллоидных и коллоидных растворов.
Введение фуросемида 0,7 мг/кг перед маннитолом может иметь синергичный эффект на снижение ВЧД.
Уровень 3
Используется при отсутствии улучшений в процессе предыдущего лечения. В этом случае показано проведение дополнительной диагностики (визуализации головного мозга).Исследования по поводу эффективности последующих вариантов лечения в ветеринарной медицине не проводились; в гуманной медицине имеются спорные данные.
Гипервентиляция. С помощью ИВЛ можно добиться гипокапнии (снижение РаCO2 менее 35 мм рт. ст.), как следствие, развивается вазоконстрикция и происходит быстрое снижение ВЧД. Следует избегать длительной гипокапнии, т.к. длительная вазоконстрикция приведет к снижению мозгового кровотока и ишемии.
Гипотермия – экспериментальное лечение в гуманной медицине. Эффект основан на том, что во время контролируемой гипотермии (и индуцированной комы, например, с помощью барбитуратов) значительно снижается уровень метаболизма в головном мозге. Гипотермия достигается охлаждением пациента до 32–35 градусов, что приводит к снижению метаболизма, потребления кислорода, а также – снижению мозгового кровотока и ВЧД. На сегодняшний день данный метод не имеет практического применения в ветеринарной медицине, т.к. необходим тщательный контроль как самого процесса охлаждения, так и состояния пациента (возможны побочные эффекты – аритмии, коагулопатии, электролитные нарушения, гиповолемия и др.).
Прогестерон в экспериментах на крысах и людях вызывал снижение отека головного мозга, а также обладал нейропротекторным действием, основанным на снижении эффекта глутамата и усилении эффекта ГАМК (тормозящего медиатора нервной системы).
Хирургическое лечение используется в ветеринарной медицине нечасто. Показаниями могут быть удаление гематом, переломы черепа. Использование хирургической декомпрессии при диффузной черепно-мозговой травме является спорным в гуманной медицине, т.к. пока не показало преимуществ перед консервативным лечением [9]. Хирургическое вмешательство у собак и кошек стоит рассматривать в случае ухудшения неврологического статуса, несмотря на интенсивное консервативное лечение [12].
Прогноз при ЧМТ зависит от многих факторов, в первую очередь – от тяжести лечения и динамики на фоне лечения. Для более объективной оценки прогноза и динамики рекомендуется использовать модифицированную шкалу комы Глазго. Еще одним прогностическим моментом является степень изменений на МРТ (например, собаки без срединного смещения имеют более благоприятный прогноз).
После выздоровления у пациентов может оставаться неврологический дефицит.
- Michael D. Lorenz. Handbook of veterinary neurology.
- Hyperglycemia in dogs and cats with head trauma: 122 cases (1997–1999). J Am Vet Med Assoc. 2001 Apr 1; 218(7): 1124–9.
- Treatment of transtentorial herniation unresponsive to hyperventilation using hypertonic saline in dogs: effect on cerebral blood flow and metabolism. J Neurosurg Anesthesiol. 2002 Jan; 14(1): 22–30.
- Effect of head elevation on intracranial pressure, cerebral perfusion pressure, and cerebral blood flow in head-injured patients. J Neurosurg. 1992 Feb; 76(2): 207–11.
- The prognostic value of the modified Glasgow Coma Scale in head trauma in dogs. J Vet Intern Med. 2001 Nov-Dec; 15(6): 581–4.
- Prognostic value of early magnetic resonance imaging in dogs after traumatic brain injury: 50 cases. J Vet Intern Med. 2014; 28: 1256–1262.
- Evaluation of intracranial pressure by transcranial Doppler ultrasonography in dogs with intracranial hypertension. J Vet Med Sci. 2000 Mar; 62(3): 353–5.
- Final results of MRC CRASH, a randomised placebo-controlled trial of intravenous corticosteroid in adults with head injury-outcomes at 6 months. Lancet. 2005 Jun 4-10; 365(9475): 1957–9.
- Decompressive craniectomy in diffuse traumatic brain injury. N Engl J Med. 2011 April 21; 364: 1493–1502.
- Mokri B. The Monro-Kellie hypothesis: applications in CSF volume depletion. Neurology. 2001 Jun 26.
- Intracranial pressure and cerebral perfusion pressure responses to head elevation changes in pediatric traumatic brain injury. Pediatr Crit Care Med. 2012 Jan; 13(1): 39–47.
- Curtis W. Dewey. Practical guide to canine and feline neurology.
- Effect of head elevation on intracranial pressure, cerebral perfusion pressure, and regional cerebral oxygen saturation in patients with cerebral hemorrhage. Rev Esp Anestesiol Reanim. 2008 May; 55(5): 289–93.
- Platt S., Garosi L. Small animal neurological emergencies.
- Relationship among basilar artery resistance index, degree of ventriculomegaly, and clinical signs in hydrocephalic dogs. Vet Radiol Ultrasound. 2003 Nov-Dec; 44(6): 687–94.





 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург