Лабораторная диагностика
Все методы лабораторной диагностики, которые мы рассмотрим в статье, преследуют цель помочь клиницисту подтвердить или опровергнуть свои предположения в отношении возможности гиперальдостеронизма, а также провести дифференциальную диагностику (особенно это актуально в случае наличия сочетанных патологий или сопутствующих заболеваний).Типичными биохимическими аномалиями у кошек с гиперальдостеронизмом являются умеренная или тяжелая гипокалиемия и нормальные или слегка повышенные концентрации натрия. При этом всегда следует правильно интерпретировать концентрации ионов калия, способные привести к симптомам гипокалиемии. Биохимическая гипокалиемия не всегда тождественна клинически значимой. Так, концентрация калия в сыворотке крови < 3.5 мг-экв/л соответствует биохимической гипокалиемии. При этом симптомы гипокалиемической миопатии у кошек проявятся при концентрации ионов калия в сыворотке крови < 3.0 мг-экв/л.
Немаловажно, что под воздействием альдостерона усиливается экскреция калия с одновременной активацией при этом перемещения калия из внутриклеточного пула во внеклеточную жидкость. Это становится компенсаторным механизмом для поддержания нормокалиемии. Данный механизм способен маскировать потери ионов калия. Но при этом также усиливаются внутриклеточный транспорт и потеря почками ионов водорода, что, в свою очередь, способствует метаболическому алкалозу. Прогрессия гипокалиемии приводит к прогрессии жажды и алкалоза.
Также осторожно следует интерпретировать результаты определения концентрации ионов натрия в сыворотке крови. Вторично по отношению к задержке натрия реабсорбируется вода. Следовательно, повышенные концентрации натрия «разбавляются», и уровень этого электролита редко бывает повышен. Иногда повышается общее содержание натрия в организме при нахождении концентрации ионов натрия в референтном диапазоне на верхней его границе.
Эти данные делают необходимой крайне осторожную и тщательную интерпретацию концентрации электролитов в сыворотке крови. Ни в коем случае при получении цифр, находящихся в референтных диапазонах, такая информация не должна стать поводом для окончательного исключения диагноза. К сожалению, восприятие гипокалиемии и гипернатриемии как обязательных последствий гиперальдостеронизма кошек является одной из причин ошибок диагностики.
При наличии такого симптома, как гипокалиемическая миопатия, концентрация креатинкиназы в сыворотке крови у кошек обычно заметно повышена. Могут также иметься признаки болезни почек, к которым относятся гипостенурия, протеинурия и повышенные концентрации в сыворотке креатинина и мочевины. У кошек, которые первоначально не имели данных о ХБП, она может прогрессировать в связи с тем, что гиперальдостеронизм является важным медиатором прогрессирующей болезни почек [2].
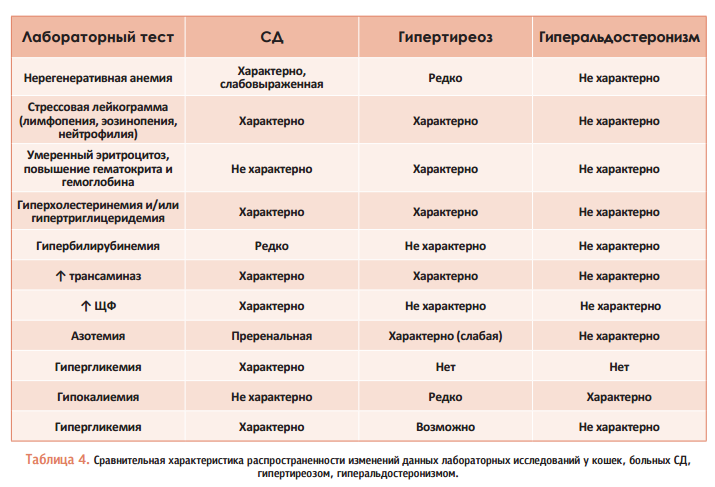
По аналогии с предыдущими таблицами, в таблице 4 приведены основные лабораторные данные, помогающие при дифференциальной диагностике.
Альдостерон – невидоспецифичный гормон. Референтный диапазон у кошек составляет 194–388 нг/дл [10]. На практике его исследование может проводиться в адаптированных медицинских лабораториях, поскольку в ветеринарных лабораториях проведение данного теста не распространено. Для исследования пригодна гепаринизированная плазма или сыворотка с ЭДТА. Плазма крови стабильна до 7 суток при температуре 2–8°C [14]. У здоровых кошек и у кошек с вторичным гиперальдостеронизмом могут быть значительные суточные колебания концентрации альдостерона в сыворотке крови. Но обычно его содержание увеличивается и при первичном, и при вторичном заболевании. В случае сочетания гипокалиемии и высокой концентрации альдостерона с достаточно большой долей вероятности можно подозревать у кошки гиперальдостеронизм, но этих данных не может быть достаточно для определения характера патологии. Максимально высокие концентрации альдостерона характерны для кошек с первичным гиперальдостеронизмом [2]. В одном из исследований концентрация альдостерона в плазме у 10 кошек с первичной патологией варьировалась от 1253 нг/дл до 3329 нг/дл [10].
При вторичном гиперальдостеронизме, поскольку патология обусловлена чрезмерной стимуляцией РААС, увеличивается концентрация не только альдостерона, но и ренина. Таким образом, при обнаружении сочетания повышенного содержания альдостерона и ренина следует подозревать возможность вторичного гиперальдостеронизма. При этом необходимо отбирать достаточно большой объем крови и немедленно замораживать отделенную плазму. Следует избегать применения гепарина, но можно использовать пробирки с ЭДТА. Эти особенности не позволяют широко использовать данный тест в ветеринарной медицине. Как и в случае с исследованием уровня альдостерона, в ветеринарных лабораториях проведение данного теста не распространено. На активность ренина также могут влиять различные лекарственные препараты, которые получает пациент (например, ингибиторы АПФ, бета-блокаторы), а также потребление соли с пищей.
К сожалению, на сегодняшний день мы очень далеки от идеальных лабораторных возможностей. Тем не менее как клиницисты мы должны понимать, что невозможность определения ренина не должна приводить к безысходности в диагностике, поскольку ни один универсальный и идеальный лабораторный тест не способен заменить суждение врача и объективные данные о наличии патологии.
Также следует упомянуть об изменении концентрации других гормонов в сыворотке крови пациентов с гиперальдостеронизмом. По мере усиления синтеза минералокортикоидов происходит активирование всего пути биосинтеза стероидов.
В результате можно отметить повышение концентрации в сыворотке крови пациентов с гиперальдостеронизмом не только альдостерона, но и стероидов-предшественников, например дезоксикортикостерона, кортикостерона, 18-гидроксикортикостерона. На сегодняшний день эти данные представляют более научный, нежели практический интерес. Безусловно, если у кошки есть новообразование надпочечника/ов смешанного характера, одновременно секретирующее, например, альдостерон и прогестерон, то при проведении лабораторного исследования уровня циркулирующих гормонов мы можем столкнуться также и с превышением референтных диапазонов прогестерона.
Визуальная диагностика
Методы визуализации, которые мы можем использовать в ходе проведения дифференциальной диагностики, также способны дать немало подсказок клиницисту как в случае заболевания первичным, так и в случае заболевания вторичным гиперальдостеронизмом.
Визуальная диагностика необходима при подозрении на первичный гиперальдостеронизм, так как только она способна дать более точную информацию о том, поражен один надпочечник или оба. Этот вопрос особенно важен в связи с тем, что унилатеральный первичный гиперальдостеронизм потенциально можно излечить хирургически, тогда как билатеральное или подтвержденное метастатическое заболевание следует лечить медикаментозно.
При обнаружении новообразования надпочечника (или надпочечников) визуальные методы должны быть использованы также для выявления отдаленных и регионарных неопластических поражений других органов и тканей. «Опухоли надпочечников редко видны при использовании рентгенографии, и если опухоль видна, то она наиболее вероятно является адренокортикальной карциномой» [2, стр. 41]. При рентгенографическом исследовании грудной полости следует обратить внимание на наличие новообразований, при проведении УЗИ, КТ, МРТ брюшной полости также – на возможность инвазии опухоли правого надпочечника в КПВ и окружающие структуры.
По данным BSAVA [1, стр. 149] поперечный размер надпочечников у кошек составляет 2.8–5.5 мм. Медианный дорсовентральный размер левого надпочечника составляет от 3 до 5,3 мм; правого надпочечника – от 2,9 до 4,5 мм [2, стр. 41]. По данным Penninck D., d`Andre M., продольный размер надпочечников кошек составляет 10–11 мм, максимальный диаметр – 4.3 +/- 0.3 мм [18, стр. 388]. Референтные диапазоны применимы ко всем кошкам, независимо от их размера или возраста. Самыми частыми находками при первичном гиперальдостеронизме у кошек становятся новообразования надпочечников, кальцификация надпочечников и изменения их эхогенности (рис. 4).
В случае одностороннего поражения надпочечника контралатеральный надпочечник может быть или нормальным, или гипотрофированным. В случае уменьшения размеров такой надпочечник не всегда обнаруживается при проведении УЗИ. При этом крайне важно понимать, что обнаружение измененного надпочечника не является дефинитивным параметром для постановки окончательного диагноза «первичный гиперальдостеронизм». Дифференциальными диагнозами, способными привести к исходным изменениям, являются нефункциональные новообразования надпочечников, феохромоцитомы, кортизол-секретирующие и прогестерон-секретирующие опухоли. Наряду с этим при использовании доступных методов визуализации (КТ, МРТ, УЗИ) надпочечники могут выглядеть абсолютно нормально, и их размеры могут соответствовать референтным диапазонам даже при наличии функциональных новообразований и/или клинически значимой гиперплазии.
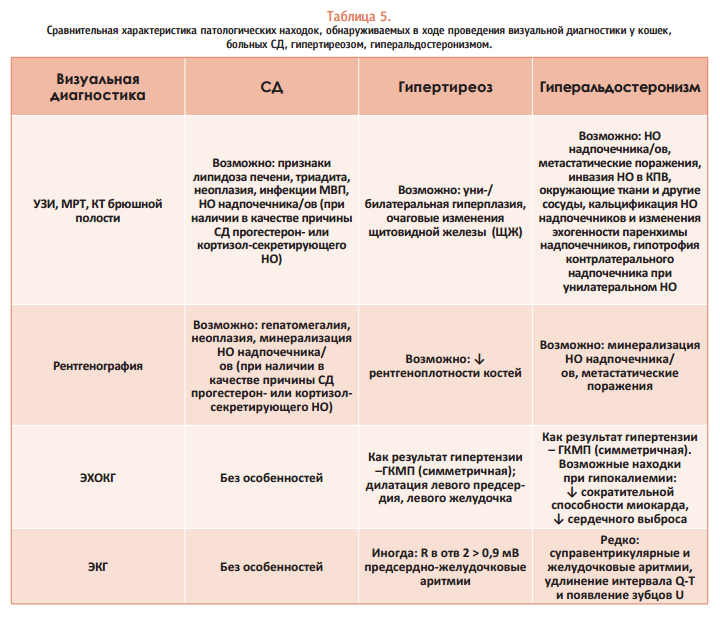
Возможные находки, которые характерны для гиперальдостеронизма и могут быть обнаружены врачом визуальной диагностики, приведены в таблице 5. Сравнение с данными, обнаруживаемыми при заболевании кошек СД и гипертиреозом, может помочь провести дифференциальную диагностику.
Дифференциальные диагнозы
Безусловно, гиперальдостеронизм не единственное заболевание, которое можно заподозрить у кошки при наличии сочетания гипокалиемии и артериальной гипертензии. При наличии гипокалиемии следует учитывать следующий список болезней, способных привести к данной патологии: ХБП; СД в самом начале инсулинотерапии; быстро растущие новообразования; алиментарные патологии; гипертиреоз.Среди указанных патологий к артериальной гипертензии нередко приводят ХБП, СД, гипертиреоз. Таким образом, порой перед нами может возникнуть сложная задача: определить, какая из болезней стала истинной причиной для того или иного симптома (особенно это касается клинических случаев, сопровождающихся неспецифическими симптомами).
В статье «Изменения концентрации калия: гипер- и гипокалиемия» («Ветеринарный Петербург» 2014, № 5) был предложен и обсужден общий диагностический план в случае, если пациент – взрослая кошка старше 8-летнего возраста. Там же был приведен перечень патологий (помимо гипокалиемии), способных привести к мышечной слабости. Стоит уточнить, что в протокол исследования пациента с подозрением на гиперальдостеронизм или при наличии сомнительных симптомов, наводящих на подозрение о возможности артериальной гипертензии, обязательно должно быть включено измерение артериального давления.
Осложнения и последствия
Осложнения и последствия, связанные с гиперальдостеронизмом, обусловлены в первую очередь артериальной гипертензией. К ним можно отнести следующие патологии:
– ГКМП. Заподозрить данную патологию можно, услышав патологические шумы при аускультации, обнаружив признаки кардиомегалии при проведении рентгенографии грудной клетки (однако данные находки вовсе не являются обязательными для кошек с ГКМП). Патология подтверждается только путем проведения эхокардиографии (ЭХОКГ) и носит обычно симметричный характер. Изменения сердца соответствуют повреждению, вызванному гипертензией, вторичной по отношению к увеличенному внутрисосудистому объему.
– ХБП. Альдостерон способен участвовать в развитии и прогрессии повреждения почек, способствуя тромбозу сосудов и фиброзу. Кроме того, как альдостерон, так и ангиотензин II способствуют поддержанию гипертензии и дальнейшей фибропролиферативной деструкции почек [2, стр. 39].
Лечение
В статье «Изменения концентрации калия: гипер- и гипокалиемия» («Ветеринарный Петербург» 2014, № 5) было подробно рассмотрено симптоматическое лечение гипокалиемии кошек. В случае тяжелой гипокалиемии необходимо внутривенное введение солей калия, в других ситуациях возможно использование пероральных препаратов калия.Сохранение гипокалиемии невыясненной этиологии, несмотря на суплементацию калием, должно навести на подозрение о возможности гиперальдостеронизма у кошек и расширить диагностические манипуляции, используемые для данных пациентов. Безусловно, в этом случае мы не сможем рассчитывать на успех лечения, если своевременно не выявим и не попытаемся устранить первопричину гипокалиемии. В случае заболевания первичным гиперальдостеронизмом одно медикаментозное лечение вряд ли может нормализовать концентрации калия в циркулирующей крови. Но в подобных ситуациях обычно удается обеспечить контроль клинических симптомов, связанных с миопатией.
В любом случае, как при первичном, так и при вторичном гиперальдостеронизме следует устранять первоисточник болезни.
В качестве дополнительных средств корректировки гипокалиемии при гиперальдостеронизме рекомендовано использовать также ингибиторы ангиотензинпревращающего фактора (ИАПФ) и калийсберегающие диуретики (антагонисты альдостерона). Применение этих препаратов возможно как в режиме монотерапии, так и совместно с препаратами калия, если их недостаточно для контроля концентрации ионов калия.
Спиронолактон – это конкурентный антагонист альдостерона, вызывающий задержку калия и экскрецию натрия. Рекомендованная доза для кошек – 2–5 мг/кг орально 1–2 раза в сутки.
С целью контроля артериальной гипертензии можно использовать амлодипина бесилат («Амловас», «Амлодипин», «Нормодипин», «Веро-Амлодипин»). Этот препарат первого выбора – антагонист кальция, блокирующий входящий трансмембранный поток ионов кальция и являющийся вазодилататором, снижающим периферическое сосудистое сопротивление, а за счет этого – кровяное давление. Инотропный эффект амлодипина очень слабый. Доза на кошку составляет от 0,625 до 1,25 мг 1 раз в сутки, но некоторым пациентам требуется увеличение дозы. Также нередко в рекомендациях можно встретить дозу 0.125–0.25 мг/кг 1 раз в сутки. Со временем подобранная доза может стать недостаточной, и тогда кошке потребуется дополнительно применение ИАПФ в сочетании с амлодипином.
Контроль пациента с симптомами гипертензии и гипокалиемии
Эффективные дозы препаратов калия и гипотензивных средств всегда должны подбираться индивидуально. Следует проводить тщательный мониторинг электролитов и артериального давления в течение пяти-семи дней ежедневно после каждого изменения дозы используемых лекарственных средств или после начала применения новых лекарственных средств, пока кошка не станет нормокалиемичной и нормотензивной. Целью лечения является сначала снижение, а затем устранение клинических симптомов и последствий гипокалиемической миопатии и артериальной гипертензии.
Хирургическое лечение
Летальность при проведении унилатеральной адреналэктомии составляет порядка 33%. Такая летальность может быть обусловлена тяжелым кровотечением из КПВ. Относительно высокий процент периоперационных летальных исходов ограничивает выбор данного метода лечения в качестве первостепенного. Но выбор терапевтического лечения в данном случае приведет лишь к паллиативной терапии.Тем не менее при унилатеральном поражении надпочечника новообразованием адреналэктомия может стать самым предпочтительным вариантом лечения. Естественно, это лечение актуально при отсутствии видимых метастатических поражений. Успешная адреналэктомия способна вылечить пациента, в том числе без необходимости применения последующей терапии. Подготовка пациента к хирургическому лечению включает в себя обязательное устранение последствий и симптомов, связанных с ведущими последствиями гиперальдостеронизма, – гипокалиемии и артериальной гипертензии.
Кроме кровотечения из КПВ, также сообщается о следующих осложнениях: интраабдоминальное кровотечение, острая почечная недостаточность, сепсис, тромбоэмболия.
Контроль концентрации электролитов в сыворотке крови и АД должен регулярно проводиться во время адреналэктомии, а также в ближайший послеоперационный период. Также подобные исследования могут оказаться полезными на протяжении нескольких послеоперационных дней. В случае сохранения гипертензии или гипокалиемии после адреналэктомии стоит продолжать симптоматическую терапию до купирования этих патологий.
В заключение хочется отметить, что редкая диагностируемость гиперальдостеронизма может быть обусловлена не только редкой встречаемостью патологии, но и тем, что в некоторых случаях болезнь остается невыясненной, а диагноз – неверифицированным ввиду ограничения лабораторных и технических возможностей. Вероятно, пропаганда информации о болезни среди врачей и расширение границ лабораторной диагностики поспособствуют большей инцидентности данной патологии кошек.
Список использованных литературных источников:
1. Бенчкроун Г. и Розенберг Д. Атипичные эндокринные заболевания собак и кошек // Veterinary Focus. – Vol. 21, № 1. – 2011. – С. 35–40.2. Бэксфилд Н. Гиперальдостеронизм у кошек / Материалы Санкт-Петербургской ветеринарной терапевтической конференции. – 2013. – С. 38–47.
3. Макинтайр Д., Дробац К., Хаскингз С., Саксон У. Скорая помощь и интенсивная терапия мелких домашних животных. – М.: Аквариум, 2013. – 560 с.
4. Нельсон Р., Фельдман Э. Эндокринология и репродукция собак и кошек. – «Софион», 2008. – 1256 с.
5. Современный курс ветеринарной медицины Кирка / под ред. Дж. Д. Бонагура; пер. с англ. – М.: Аквариум-Принт, 2005. – 1376 с.
6. Торранс Э. Д., Муни К. Т. Эндокринология мелких домашних животных. – М.: Аквариум, 2006. – 311 с.
7. Burkitt Creedon J. М., Davis Н. Advanced Monitoring and Procedures for Small Animal Emergency and Critical Care. – Wiley-Blackwell, 2011. – 888 р.
8. Cochran Phillip E. Veterinary Anatomy & Physiology: A Clinical Laboratory Manual, 2nd Edition. – Delmar Cengage Learning, 2011. – 380 p.
9. Ettinger S., Feldman E. Textbook of Veterinary Internal Medicine Expert Consult, 7th Edition. – W.B. Saunders Company, 2009. – 2208 р.
10. Frances J. Barr , Lorrie Gaschen. BSAVA Manual of Canine and Feline Ultrasonography. – Publisher: British Small Animal Veterinary, 2011. – Р. 222.
11. Gough А. Differential Diagnosis in Small Animal Medicine. – Blackwell Publishing Ltd, First published, 2007. – 464 р.
12. Kenneth J. Drobatz, Merilee F. Costello. Feline Emergency and Critical Care Medicine, 2010. – 672 p.
13. Lo A. J., Holt D. E., Brown D. C., Schlicksup M. D., Orsher R. J., Agnello K. A. Treatment of Aldosterone-Secreting Adrenocortical Tumors in Cats by Unilateral Adrenalectomy: 10 Cases (2002–2012) // J Vet Intern Med. – 2014; № 28. – Р. 137–143.
14. Mooney C. T., Peterson M. E. Canine and Feline Endocrinology. – BSAVA, 2004. – 248 p.
15. de Morais H. A., Bach J. F., DiBartola S. P. Metabolic Acid-Base Disorders in the Critical Care Unit // Vet Clin Small Anim. – 2008; № 38. – Р. 559–574.
16. Norkus С. Veterinary Technician’s Manual for Small Animal Emergency and Critical Care. – Wiley-Blackwell, 2012. – 567 р.
17. Norsworthy G. D., Grace S. F., Crystal M. A., Tilley L. P. The feline patient / editor Gary D. Norsworthy. – Wiley-Blackwell, 4th Edition, 2011. – 1052 р.
18. Penninck D., d`Andre M. Small Animal Ultrasonography. – Blackwell Publishing Ltd, 2008. – 502 р.
19. Silverstein D. C., Hopper K. Small Animal Critical Care Medicine, 2nd Edition. Saunders. – 2009. – 1152 p.
20. Steinbach S. Die chronische Nierenerkrankung der Katze // Kompendium Kleintier. – 2014. – Р. 17–25.
21. Textbook of Small Animal Medicine / editor John K. Dunn. – W. B. Saunders, 1999. – 1065 p.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург