Болезнь Аддисона, или гипоадренокортицизм, представляет собой патологическое состояние, характеризующееся недостаточной выработкой гормонов корой надпочечников. В ветеринарной медицине гипоадренокортицизм чаще регистрируется у собак, чем у кошек. У кошек данное заболевание встречается реже, преимущественно в возрастной группе от 1,5 до 14 лет. Согласно ретроспективному исследованию, средний возраст кошек с гипоадренокортицизмом составляет 5,7 лет (диапазон: 2–13,8 лет). В выборке, включающей 41 кошку, 23 (56%) были самцами, а 18 (44%) – самками1.
По данным зарубежных исследований, кошки британской породы имеют предрасположенность к развитию болезни Аддисона2.
Этиология заболевания
Гипоадренокортицизм у кошек развивается вследствие аутоиммунного повреждения надпочечников, которое может быть опосредовано каким-либо инфекционным заболеванием. Опухолевые поражения надпочечниковой ткани, такие как лимфома надпочечников, также могут быть причиной развития данного заболевания: зарегистрировано 2 случая гипоадренокортицизма у кошек, который развился на фоне лимфомы1. В редких случаях гипоадренокортицизм возникает вследствие травмы надпочечников. Ятрогенный гипоадренокортицизм может развиться в результате длительного применения митотана, который вызывает деструкцию ткани надпочечников, а также при использовании трилостана, ингибирующего выработку стероидов надпочечниками вследствие некроза коры надпочечников, предположительно, вызванного воздействием адренокортикотропного гормона (АКТГ). Еще одна причина – резкое прекращение приема стероидных препаратов. Во время лечения стероидами надпочечники снижают синтез собственных гормонов, а при отмене препаратов не успевают восстановить выработку гормонов на уровне, необходимом для нормального функционирования организма. Описан случай развития гипоадренокортицизма и сахарного диабета у кошки уже через 12 часов после отмены метилпреднизолона3. Также зарегистрирован единичный случай болезни Аддисона у 18-месячного кота, вызванный некрозом коры надпочечников после эндоскопического удаления инородного тела под анестезией. Наличие данной патологии было подтверждено результатом цитологического исследования4. Некроз надпочечников после проведения анестезии также встречается в медицине человека.Физиология и патофизиология
Адренокортикотропный гормон (АКТГ) синтезируется и секретируется передней долей гипофиза под контролем гипоталамического кортикотропин-рилизинг-фактора. АКТГ действует на кору надпочечников, стимулируя секрецию глюкокортикостероидов, включая кортизол. Повышение уровня АКТГ в крови приводит к увеличению концентрации кортизола. При недостаточности коры надпочечников, несмотря на увеличение уровня АКТГ, уровень кортизола остается низким.Кора надпочечников состоит из трех гистологически различных слоев: клубочковой зоны (внешнего слоя), пучковой зоны (среднего слоя) и сетчатой зоны (внутреннего слоя). Каждый из этих слоев отвечает за синтез специфических гормонов: клубочковая зона секретирует минералокортикоиды, преимущественно альдостерон; пучковая зона синтезирует глюкокортикостероиды; сетчатая зона – половые гормоны. При развитии гипоадренокортицизма и атрофии паренхимы надпочечников может формироваться соответственно дефицит глюкокортикостероидов или сочетанный дефицит глюкокортикостероидов и минералокортикоидов.
У большинства животных при развитии гипоадренокортицизма обнаруживается как глюкокортикоидная, так и минералокортикоидная недостаточность, однако у 10% больных животных заболевание может протекать без минералокортикоидной недостаточности и электролитных нарушений.
Глюкокортикостероидный гормон кортизол выполняет в организме ряд важнейших функций: повышает уровень глюкозы крови (глюконеогенез печени), системное артериальное давление (задержка воды и натрия в организме), частоту сердечных сокращений (вазоконстрикция) и оказывает противовоспалительное действие (уменьшает активность лимфоцитов).
Минералокортикоидный гормон альдостерон регулирует водно-солевой баланс в организме, способствуя выведению калия с мочой и реабсорбции натрия в почечных канальцах.
Дефицит кортизола и альдостерона приводит к развитию неспецифических клинических симптомов.
Клинические признаки болезни Аддисона развиваются при потере функции 80% коры надпочечников и более5. Симптомы гипоадренокортицизма характеризуются многообразием и неспецифичностью, что затрудняет их своевременную диагностику и дифференциацию
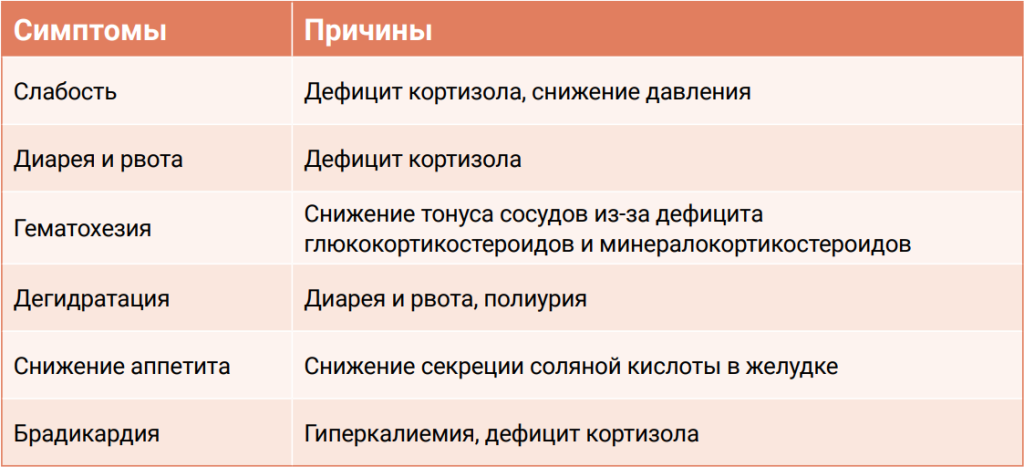
(табл. 1).
Одним из распространенных симптомов является мышечная слабость, обусловленная снижением артериального давления вследствие дефицита кортизола. Рвота и диарея также являются характерными проявлениями, связанными с потерей жидкости через желудочно-кишечный тракт, что приводит к дегидратации. Снижение синтеза соляной кислоты в желудке вследствие гипоадренокортицизма может приводить к ухудшению аппетита. Все вышеперечисленные симптомы приводят к потере веса. При клинически значимой гиперкалиемии развивается брадикардия, которая также может быть следствием дефицита кортизола. Даже при прогрессировании состояния до гиповолемического шока брадикардия остается характерным признаком. Согласно результатам исследования, кошки с гипонатриемией, гиперкалиемией или обоими нарушениями чаще демонстрируют гипотермию и дегидратацию без рвоты. Таким образом, отсутствие желудочно-кишечных симптомов не исключает наличия болезни Аддисона у кошек6.
Диагностика
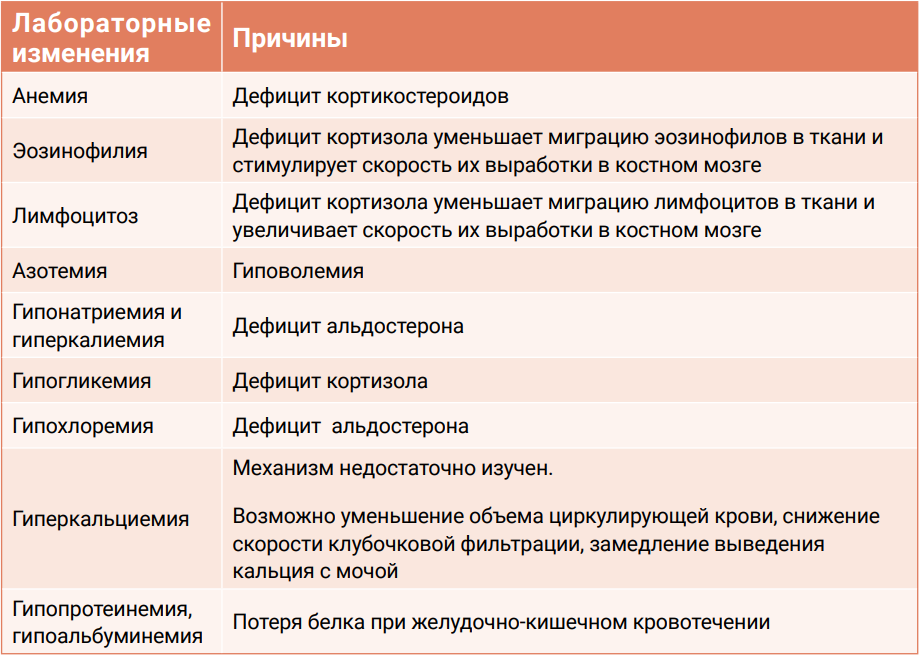
Заподозрить болезнь Аддисона по причине отсутствия патогномоничных симптомов сложно, клиницисту всегда необходимо включать данное заболевание в список дифференциальных диагнозов при выявлении клинических признаков, которые могут давать основание предполагать его наличие.Особое внимание следует уделять лабораторным исследованиям. В клиническом анализе крови часто обнаруживаются нерегенераторная анемия, лимфоцитоз и эозинофилия. В биохимическом профиле обычно выявляются преренальная азотемия, гипонатриемия, гиперкалиемия, гипогликемия, гипохлоремия, гиперкальциемия, гипоальбуминемия и гипопротеинемия. Гиповолемия может маскировать анемию, гипопротеинемию и гипоальбуминемию, что дополнительно усложняет диагностику. Согласно данным одного из исследований, частота гиперкальциемии у больных гипоадренокортицизмом кошек составляла 31,7%1. В таблице 2 представлена информация о возможных причинах изменений лабораторных показателей при болезни Аддисона.
Соотношение Na:К < 23:1 в сыворотке крови рассматривается как характерная особенность пациентов с болезнью Аддисона (особенно в состоянии криза).
Все вышеперечисленные отклонения могут присутствовать как вместе, так и по отдельности. При подозрении на гипоадренокортицизм для постановки окончательного диагноза необходимо проведение специфического теста на стимуляцию с АКТГ. В рамках этого теста проводится отбор крови натощак для определения уровня кортизола. Затем вводится АКТГ в дозе 5 мкг/кг внутривенно или внутримышечно, и через 60–90 минут повторно проводится отбор крови для определения уровня кортизола.
Если уровни кортизола до и после введения АКТГ ниже 55 нмоль/л, диагноз считается подтвержденным, поскольку в норме надпочечники реагируют на стимуляцию АКТГ повышением уровня кортизола. В случае отсутствия болезни Аддисона уровень кортизола после введения АКТГ значительно повышается, достигая 600 нмоль/л. Если же уровень кортизола выше 55 нмоль/л до проведения теста, диагноз «гипоадренокортицизм» можно исключить.
Ультразвуковое исследование надпочечников является вспомогательным методом диагностики болезни Аддисона, однако данный метод не позволяет поставить окончательный диагноз, поскольку при наличии данной болезни при проведении УЗИ могут определяться нормальные размеры надпочечников. Маленькие надпочечники (ширина < 2,7 мм) на УЗИ у кошек с подозрением на гипоадренокортицизм могут свидетельствовать о наличии заболевания2. Тем не менее нормальный размер надпочечников на УЗИ не исключает возможности наличия болезни Аддисона8. Также был опубликован случай болезни Аддисона у кошки с адреномегалией, возникшей вследствие некроза надпочечников4.
Дифференциальная диагностика. Болезнь Аддисона у кошек требует дифференциальной диагностики для исключения других заболеваний со схожей клинической картиной. К таким заболеваниям относятся хроническая энтеропатия, хронический панкреатит, экзокринная недостаточность поджелудочной железы и хроническая болезнь почек. Для проведения дифференциальной диагностики необходимо использовать специфические лабораторные тесты в сочетании с УЗИ.
При хронической энтеропатии (ХЭ) у кошек лабораторные изменения показателей крови могут быть схожи с отклонениями, характерными для болезни Аддисона. УЗИ при ХЭ у кошек может выявить изменения в соотношении слоев кишечной стенки: соотношение мышечного слоя к подслизистому > 1 указывает на патологические изменения участка кишечника, также могут быть выявлены точечные гиперэхогенные включения в слизистом слое, характерные для лимфангиэктазии. В связи с тем, что нормальные размеры надпочечников на УЗИ не исключают наличия болезни Аддисона, для дифференциальной диагностики необходимо провести тест на стимуляцию с АКТГ.
При панкреатите рутинные лабораторные изменения показателей крови также не позволяют провести дифференциальную диагностику. При подозрении на панкреатит проводят исследование сыворотки крови для определения уровня кошачьей специфической панкреатической липазы и ультразвуковое исследование поджелудочной железы; при подозрении на экзокринную недостаточность поджелудочной железы исследуют уровень трипсиноподобной иммунореактивности в сыворотке крови (исследование недоступно в РФ). Для проведения окончательной дифференциальной диагностики заболеваний поджелудочной железы и болезни Аддисона у кошек проводят тест на стимуляцию с АКТГ и УЗИ брюшной полости.
При хронической болезни почек маркеры уремии (креатинин, мочевина, фосфор) часто бывают повышены, что также характерно для болезни Аддисона. Однако при наличии болезни Аддисона повышение этих маркеров имеет преренальный характер. Для дифференциальной диагностики ХБП и болезни Аддисона рекомендуется провести ультразвуковое исследование почек и надпочечников. Окончательным этапом диагностики является тест на стимуляцию с АКТГ. Дополнительно может быть полезным проведение исследования сыворотки крови на симметричный диметиларгинин (СДМА) у кошек. Уровень СДМА менее подвержен влиянию потери мышечной массы по сравнению с креатинином, что делает его более информативным показателем при определении стадии ХБП.
Во всех случаях тяжелой гипогликемии у кошек болезнь Аддисона нужно включать в перечень дифференциальных диагнозов.
Согласно результатам многоцентрового ретроспективного исследования1, у больных гипоадренокортицизмом кошек выявляли экзокринную недостаточность поджелудочной железы (4/7 обследованных кошек); у всех четырех животных был обнаружен дефицит кобаламина, что может свидетельствовать о наличии сопутствующей хронической энтеропатии.
При проведении дифференциальной диагностики необходимо учитывать возможность одновременного течения заболеваний. Наиболее достоверным методом диагностики болезни Аддисона у кошек является тест на стимуляцию с АКТГ.
Лечение
Заместительную терапию надпочечниковой недостаточности у кошек и собак проводят пожизненно. Потребность в экзогенных минералокортикоидах и глюкокортикостероидах у кошек выше по сравнению с собаками при лечении гипоадренокортицизма. Согласно опубликованным данным, начальная доза дезоксикортикостерона (ДОКП, селективный минералокортикоидный препарат) составляет 2,2 мг/кг, поддерживающая доза преднизолона – 0,3 мг/кг/день с последующим титрованием в зависимости от индивидуальной потребности животного2. По рекомендациям Дж. Кэтрин Скотт-Монкрифф, длительная терапия минералокортикоидами включает применение флудрокортизона ацетата внутрь (0,05–0,10 мг дважды в сутки) или инъекционного ДОКП. Для заместительной глюкокортикоидной терапии при необходимости обычно используют преднизолон в начальной дозе 2,5–5 мг в сутки, которую постепенно снижают до минимальной дозы, позволяющей контролировать клинические симптомы7.Клинический случай
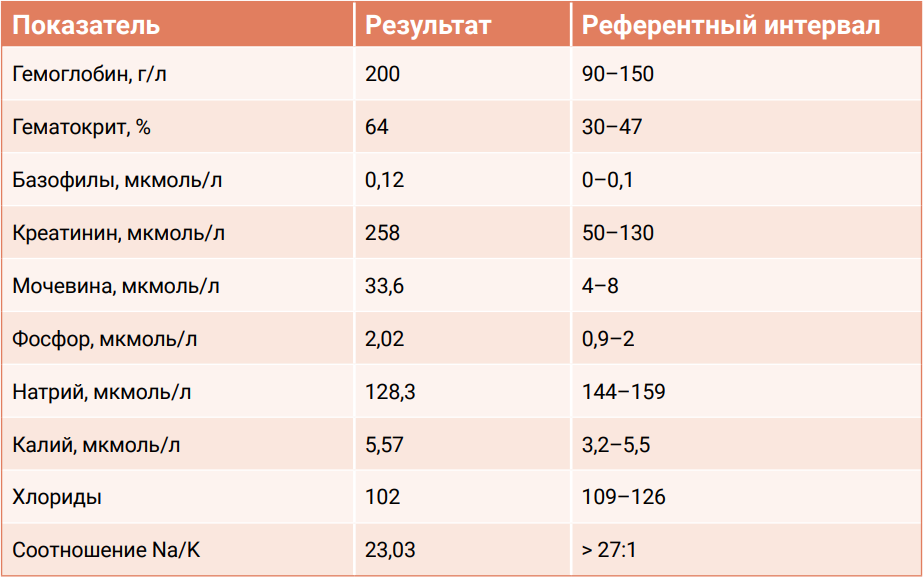
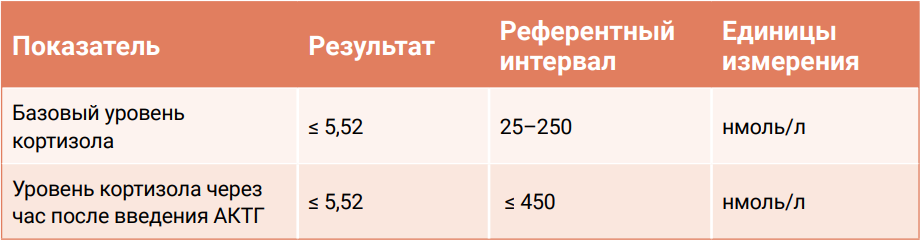
Пациент: 3-летняя кастрированная кошка абиссинской породы. Из анамнеза стало известно, что у кошки длительное время присутствовали симптомы рвоты и диареи. При физикальном осмотре животного были выявлены признаки дегидратации в пределах 8–10%, а также незначительная бледность слизистых оболочек.Лабораторные изменения (табл. 3) в сочетании с клиническими проявлениями давали основания предполагать наличие у пациента болезни Аддисона. Однако гемоконцентрация, вероятно, была вызвана дегидратацией, что могло маскировать анемию. Для уточнения диагноза был проведен тест на стимуляцию с АКТГ. Результаты теста соответствовали диагнозу «болезнь Аддисона»: после введения АКТГ стимуляция секреции кортизола надпочечниками отсутствовала (табл. 4).
Повышенный уровень СДМА в крови кошки (22,3 мкг/дл при референтном значении 0–14 мкг/дл) мог свидетельствовать о снижении скорости клубочковой фильтрации, развивающейся по причине гипоперфузии почек, вызванной болезнью Аддисона, а также о хронической болезни почек.
Дифференциальная диагностика указанных состояний не была проведена, поскольку последующее наблюдение за пациентом оказалось невозможным. К сожалению, данные о дальнейшей судьбе животного отсутствуют.
Заключение
Несмотря на то что не все лабораторные показатели (например, параметры красной крови в данном клиническом примере) могут быть специфичны для болезни Аддисона, клиницистам следует сохранять повышенную настороженность в отношении данного заболевания. Важно учитывать, что одно заболевание не исключает наличие другого, и они могут протекать одновременно. В связи с этим проведение теста на стимуляцию с АКТГ является обязательным при подозрении на болезнь Аддисона у кошек, особенно в сомнительных случаях.Болезнь Аддисона является редким заболеванием, и накопление клинического опыта по ее диагностике и лечению представляет собой актуальную задачу практической ветеринарной медицины.
Список литературы:
- Emma Roberts, Ian Keith Ramsey, Ruth Gostelow, et al. Clinical findings, treatment, and outcomes in cats with naturally occurring hypoadrenocorticism: 41 cases, 2024. DOI: 10.1111/jvim.17243
- Sieber-Ruckstuhl N. S., Harburger L., Hofer N., Kümmerle C., Müller C., et al. Clinical features and long-term management of cats with primary hypoadrenocorticism using desoxycorticosterone pivalate and prednisolone. J Vet Intern Med, 2023. DOI: 10.1111/jvim.16658
- Smith S. A., Freeman L. C., Bagladi-Swanson M. Hypercalcemia due to latrogenic secondary hypoadrenocorticism and diabetes mellitus in a cat. J Am Anim Hosp Assoc, 2002.
- Manson R. A., Hammond T. N., Callahan Clark J. E. Acute adrenal necrosis in a young female cat. J Vet Intern Med, 2024. DOI: 10.1111/jvim.16926
- Игнатенко Н. А. Клинические признаки, диагностика и лечение гипоадренокортицизма у собак. ссылка
- Marsilio S. Feline chronic enteropathy. Журнал «Ветеринарный Петербург» № 3, 2022.
- Feldman E. C., Nelson R. W., Reusch C., Scott-Moncrieff J. C. Canine and Feline Endocrinology, 4th Ed, 2015.
- Kasabalis D., Bodina E., Saridomichelakis M. N. Severe hypoglycaemia in a cat with primary hypoadrenocorticism. J Feline Med Surg, 14(10):755–8, Oct 2012.
- Смирнова О.О. Причины гипогликемии. Обзор. Современная ветеринарная медицина 2/2022.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург