1 Факультет ветеринарии, Болонский университет, Болонья, Италия
2 Практикующий врач, Монца, Италия
3 Факультет ветеринарии, Туринский университет, Турин, Италия
4 Практикующий врач, Турин, Италия
5 Кафедра клинических наук животных-компаньонов, факультет ветеринарной медицины, Утрехтский университет, Утрехт, Нидерланды
Эта статья была подготовлена и обработана Европейской редакцией (Международное общество медицины кошек [the International Society of Feline Medicine; ISFM]) для публикации в JFMS Open Reports.
Перевод: Малкова Татьяна.
Редактор перевода: Смирнова О. О., к.б.н., ветеринарный врач-терапевт, эндокринолог.
Краткое описание клинического случая. 14-летний кастрированный кот европейской короткошерстной породы был обследован в рамках планового ветеринарного осмотра. Владелец не сообщил о каких-либо клинических признаках за исключением стридора. Во время физикального осмотра основными выявленными нарушениями были широкая морда и увеличенные межзубные промежутки. Результат исследования крови показал легкую нерегенеративную анемию, тогда как результаты биохимического анализа сыворотки крови и анализа мочи не показали отклонений. В сыворотке крови концентрация глюкозы была в пределах нормы, концентрация инсулиноподобного фактора роста 1 (ИФР-1) была значительно повышена (> 1600 нг/мл), базальная концентрация гормона роста была повышена и лишь незначительно снизилась после введения соматостатина, базальная концентрация инсулина была высокой, а после нагрузки глюкозой концентрация инсулина существенно повысилась, что свидетельствовало о наличии инсулинорезистентности. Компьютерная томография (КТ) черепа показала увеличение гипофиза и утолщение костей черепа. Был поставлен окончательный диагноз «акромегалия».
Актуальность и новая информация. Полученные результаты показывают, что акромегалию необходимо подозревать и диагностировать у кошек, не имеющих сахарного диабета.
Введение
Хроническая гиперсекреция гормона роста (ГР), обусловленная гормонально-активной соматотропной аденомой, вызывает акромегалию – болезнь, характеризующуюся инсулинорезистентностью и прогрессирующим разрастанием соединительной ткани, ростом костей и внутренних органов. Клинические проявления болезни в основном обусловлены катаболическими эффектами гормона роста и анаболическими эффектами инсулиноподобного фактора роста 1 (ИФР-1)1,2. Избыток гормона роста вызывает гиперсекрецию ИФР-1 (преимущественно печенью), приводящую к повышенному синтезу протеина и избыточному разрастанию тканей. Кроме того, клинические признаки могут возникать из-за компрессии мозга большой соматотропной аденомой гипофиза.У кошек клинические признаки акромегалии включают выступание вперед нижней челюсти (прогнатию), широкую морду, увеличенные лапы, гипертрофическую кардиомиопатию, абдоминальную органомегалию, стридор и увеличение массы тела1–7. Эти признаки появляются постепенно, и часто единственным отклонением от нормы, выявляемым у кошек с акромегалией, является наличие сахарного диабета8.
Развитие сахарного диабета связано с катаболическими эффектами ГР, которые в основном обусловлены пострецепторным дефектом действия инсулина на клетки-мишени, приводящим к снижению утилизации углеводов, увеличению интенсивности глюконеогенеза и снижению чувствительности к инсулину. В результате катаболического действия ГР развивается гипергликемия. У людей гиперсекреция ГР вызывает инсулинорезистентность и непереносимость глюкозы в 16–78% случаев, а явный сахарный диабет развивается у 19–52% пациентов с акромегалией9. В то же время в ветеринарии, согласно опубликованным данным, у 100% кошек с акромегалией наблюдается сахарный диабет2. Однако в учебнике по ветеринарной медицине говорится о том, что не у всех кошек с акромегалией развивается сахарный диабет10, хотя в рецензируемых научных журналах статьи по данной теме отсутствуют.
В данной статье представлено описание клинического случая кота с акромегалией и инсулинорезистентностью, у которого не было сахарного диабета.
Описание клинического случая
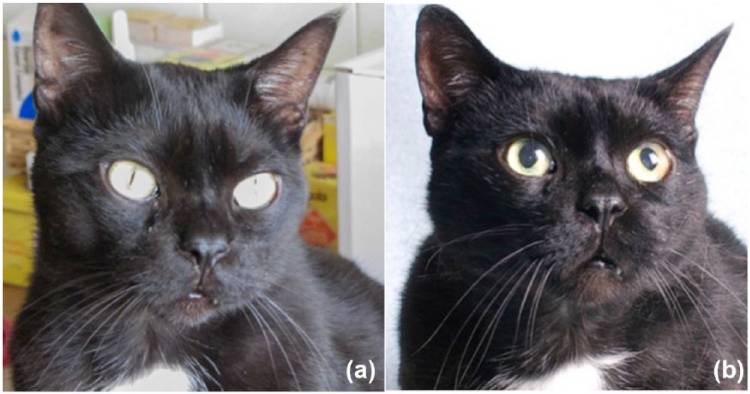
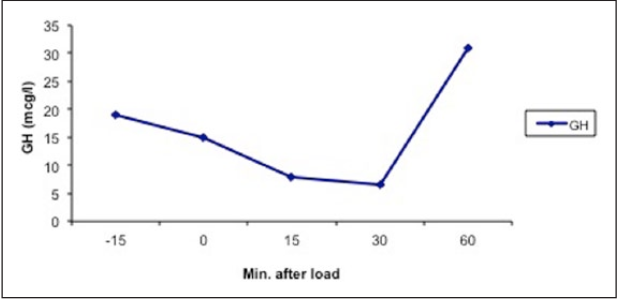
В ходе ежегодного планового ветеринарного осмотра было проведено обследование 14-летнего кастрированного кота европейской короткошерстной породы весом 6,5 кг. Владелец не отмечал наличия каких-либо клинических симптомов за исключением стридора, который появился у питомца несколько месяцев назад. При физикальном осмотре были отмечены морфологические изменения морды (широкая морда, рис. 1) и увеличенные межзубные промежутки. Эти аномалии не были заметны на фотографии кота, сделанной за 3 года до текущего осмотра (рис. 1). Также были выявлены систолический шум слева (степень 1/6), легкое обезвоживание и кератит левого глаза. Единственным отклонением от нормы в результатах рутинного лабораторного исследования была нерегенеративная анемия легкой степени (гематокрит 0,26 л/л; референтный интервал 0,30–0,45 л/л). Показатели уровней мочевины, креатинина, общего белка, альбумина, щелочной фосфатазы, аспартатаминотрансферазы, аланинаминотрансферазы, гамма-глутамилтрансферазы, креатинкиназы, холестерина, желчных кислот, натрия, калия, общего кальция, фосфатов и общего тироксина находились в пределах соответствующих референтных интервалов. Концентрация глюкозы в сыворотке крови составляла 6,0 ммоль/л (референтный интервал 4,7–6,4 ммоль/л), а концентрация фруктозамина – 352 мкмоль/л (референтный интервал 228–356 мкмоль/л). Отклонений в результате общего анализа мочи не было выявлено.Концентрация ИФР-1 в сыворотке крови, которая измерялась с помощью коммерчески доступной системы для выполнения радиоиммунологических исследований (RIA; Cambridge Specialist Laboratories Services), разработанной для применения в медицине человека и ранее уже валидированной для применения у кошек11, была значительно выше нормы (> 1600 нг/мл; референтный интервал < 800 нг/мл). Базальные концентрации ГР в сыворотке крови, которые измерялись с использованием коммерчески доступной системы RIA (PGH-46HK; Linco Research), предназначенной для измерения уровней ГР у свиней, собак и кошек, были значительно повышены в двух образцах крови, взятых с интервалом в 15 минут (15 и 19 нг/мл соответственно; референтный интервал 0,8–7,2 нг/мл)12. Эти значения были первыми двумя результатами теста на подавление секреции гормонов соматостатином, который включал сбор образцов крови для измерения концентрации ГР с интервалами -15, 0, 15, 30 и 60 минут после внутривенного введения соматостатина (Somatostatina; IBP Pharma) в дозе 5 мкг/кг массы тела12. Уровень ГР в сыворотке крови незначительно снизился в процессе проведения теста на подавление секреции гормонов соматостатином, однако остался выше 5 нг/мл (рис. 2).
Глюкозотолерантный тест был выполнен посредством внутривенного введения 50%-го раствора глюкозы (0,5 г/кг массы тела) и измерения концентраций инсулина и глюкозы с интервалами – 0, 60 и 120 минут после введения глюкозы. Концентрации глюкозы в сыворотке крови составили 7,3 ммоль/л, 15,7 ммоль/л и 5,0 ммоль/л до и через 60 и 120 минут после нагрузки глюкозой соответственно. Базальная концентрация инсулина в сыворотке крови была высокой (85 мкМЕ/мл; референтный интервал 3,7–11,4 мкМЕ/мл), а концентрация инсулина значительно выросла спустя 60 минут после нагрузки глюкозой (141 мкМЕ/мл) и снизилась через 120 минут после нагрузки глюкозой (31 мкМЕ/мл). Показатели соотношения уровней инсулина и глюкозы в сыворотке крови составили 11,6 (референтный интервал 0,24–4,76), 9,0 (референтный интервал 1,04–7,04) и 6,2 (референтный интервал 0,84–5,62) до и спустя 60 и 120 минут после нагрузки глюкозой соответственно13. Эти результаты указывают на нарушение переносимости глюкозы, несмотря на отсутствие сахарного диабета.
На рентгенограммах и эхокардиограммах грудной полости не было выявлено никаких отклонений.
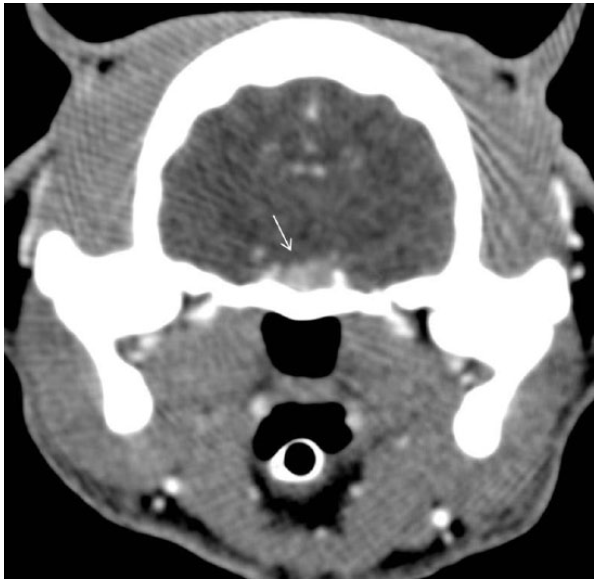
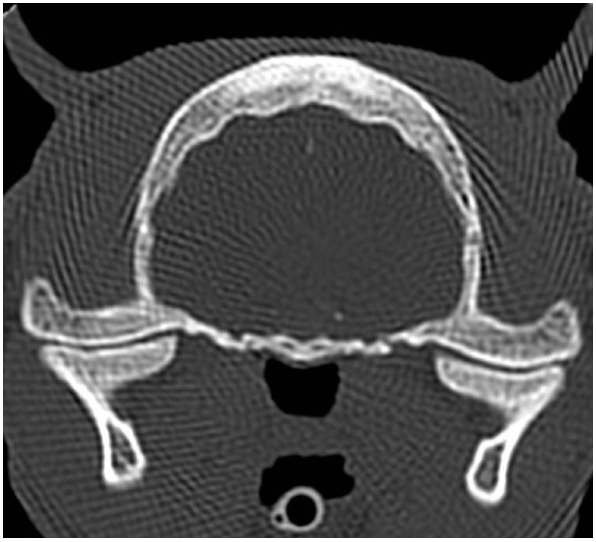
Компьютерная томография (КТ) проводилась с использованием устройства для выполнения спиральной компьютерной томографии с получением одного среза (GE Fx/i). Исследование осуществлялось в стернальном положении пациента под общей анестезией. Были получены поперечные КТ-срезы костей и мягких тканей от кончика носа до второго шейного позвонка (C2) с толщиной срезов 3 мм, а сканирование области гипофиза было выполнено с толщиной срезов 1 мм до и после введения контрастного вещества. КТ-исследование выявило увеличение размеров гипофиза (высота – 4,0 мм, ширина – 6,6 мм, длина – 4,5 мм) (рис. 3). Также наблюдалось утолщение костей черепа: теменная кость – 6,4 мм (референтный интервал 2,3–3,5), лобная кость – 4,0 мм (референтный интервал 0,2–2,6) и глубина черепа – 3,2 (референтный интервал 2,1–2,7) (рис. 4); более того, поверхность нижнечелюстного мыщелка была немного вогнута с обеих сторон. Результаты КТ-сканирования остальных участков тела не показали отклонений от нормы.
После постановки окончательного диагноза «акромегалия без сахарного диабета» концентрация глюкозы в сыворотке крови измерялась не реже двух раз в год и всегда находилась в пределах референтного интервала. Спустя два года после постановки диагноза у кота по-прежнему не был выявлен сахарный диабет и животное не получало никакого лечения.
Обсуждение
У представленного в данной статье кота все показатели многократных измерений базальной концентрации глюкозы в сыворотке находились в пределах референтного интервала. Более того, глюкозурия отсутствовала, а уровень фруктозамина также соответствовал норме. Эти данные свидетельствуют об отсутствии у животного сахарного диабета. Однако повышенные показатели соотношения уровней инсулина и глюкозы в сыворотке крови и значительное увеличение концентрации инсулина в сыворотке крови во время проведения глюкозотолерантного теста свидетельствовали об инсулинорезистентности.Инсулинорезистентность у данного пациента может быть связана, по крайней мере частично, с акромегалией. Концентрация ИФР-1 в сыворотке крови была очень высокой.
При этом сообщалось о повышении концентрации ИФР-1 в сыворотке крови у кошек с диабетом, не страдающих акромегалией14,15, и, следовательно, повышение концентрации ИФР-1 в сыворотке крови не считается достаточным основанием для постановки окончательного диагноза. Диагноз у этого кота был подтвержден на основании клинических признаков, высокого уровня гормона роста (ГР) в сыворотке крови, который лишь незначительно снизился после введения соматостатина, а также наличия опухоли гипофиза и аномалии костей, выявленных при проведении компьютерной томографии (КТ).
Внутривенное введение соматостатина привело к снижению в сыворотке крови концентрации ГР, которая все же не достигла нормальных значений. Аналогичные результаты были получены в исследованиях популяции кошек с акромегалией, у которых введение соматостатина в дозе 5 мкг/кг приводило к снижению концентрации ГР в плазме крови, однако не достигало нормализации этого показателя12.
КТ подтвердила наличие опухоли гипофиза. Помимо изменений в структуре гипофиза, акромегалия у кошек сопровождается рядом характерных признаков, обнаруживаемых при КТ-исследовании. У кота, описанного в данном клиническом отчете, наблюдались типичные проявления заболевания, такие как утолщение лобных и теменных костей, что согласуется с результатами ранее проведенных исследований8,16.
Выводы
Акромегалия у кошек встречается не так редко, как считалось раньше, и может наблюдаться у 30% кошек с плохо регулируемым или инсулинорезистентным диабетом1,7. В соответствии с этим наблюдением подозрение на акромегалию обычно возникает в отношении кошек с инсулинорезистентным сахарным диабетом. Кроме того, в исследованиях, посвященных акромегалии кошек, оценивались только популяции кошек с диабетом.Данный случай показывает, что наличие акромегалии следует предполагать не только у кошек, больных сахарным диабетом, и распространенность акромегалии может в действительности быть выше, если в будущие исследования включать кошек без сахарного диабета.
Авторы заявили об отсутствии потенциального конфликта интересов в отношении исследований, авторства и/или публикаций данной статьи.
Авторы не получали финансовую поддержку, связанную с исследованиями, авторством и/или публикацией данной статьи.
Список литературы:
- Niessen S. J., Petrie G., Gaudiano F., et al. Feline acromegaly: an underdiagnosed endocrinopathy? J Vet Intern Med, 21: 899–905, 2007.
- Greco D. S. Feline acromegaly. Top Companion Anim Med, 27: 31–35, 2012.
- Peterson M. E., Taylor R. S., Greco D. S., et al. Acromegaly in 14 cats. J Vet Intern Med, 4: 192–201, 1990.
- Elliott D. A., Feldman E. C., Koblik P. D., et al. Prevalence of pituitary tumors among diabetic cats with insulin resistance. J Am Vet Med Assoc, 216: 1765–1768, 2000.
- Peterson M. E. Acromegaly in cats: are we only diagnosing the tip of the iceberg? J Vet Intern Med, 21: 889–891, 2007.
- Berg R. I., Nelson R. W., Feldman E. C., et al. Serum insulin-like growth factor-I concentration in cats with diabetes mellitus and acromegaly. J Vet Intern Med, 21: 892–898, 2007.
- Niessen S. J. Feline acromegaly: an essential differential diagnosis for the difficult diabetic. J Feline Med Surg, 12: 15–23, 2010.
- Lamb C. R., Ciasca T. C., Mantis P., et al. Computed tomographic signs of acromegaly in 68 diabetic cats with hypersomatotropism. J Feline Med Surg, 16: 99–108, 2014.
- Dreval A. V., Trigolosova I. V., Misnikova I. V., et al. Prevalence of diabetes mellitus in patients with acromegaly. Endocr Connect, 3: 93–98, 2014.
- Feldman E. C. and Nelson R. W. Disorders of growth hormone. In: Canine and feline endocrinology and reproduction. Feldman E. C. and Nelson R. W. (eds). St Louis, MO: Saunders, pp 45–84, 2004.
- Lewitt M. S., Hazel S. J., Church D. B., et al. Regulation of insulin-like growth factor-binding protein-3 ternary complex in feline diabetes mellitus. J Endocrinol, 166: 21–27, 2000.
- Slingerland L. I., Voorhout G., Rijnberk A., et al. Growth hormone excess and the effect of octreotide in cats with diabetes mellitus. Domest Anim Endocrinol, 35: 352–361, 2008.
- Appleton D. J., Rand J. S. and Sunvold G. D. Basal plasma insulin and homeostasis model assessment (HOMA) are indicators of insulin sensitivity in cats. J Feline Med Surg, 7: 183–193, 2005.
- Starkey S. R., Tan K. and Church D. B. Investigation of serum IGF-I levels amongst diabetic and non-diabetic cats. J Feline Med Surg, 6: 149–155, 2004.
- Reusch C. E., Kley S., Casella M., et al. Measurements of growth hormone and insulin-like growth factor 1 in cats with diabetes mellitus. Vet Rec, 158: 195–200, 2006.
- Fischetti A. J., Gisselman K. and Peterson M. E. CT and MRI evaluation of skull bones and soft tissues in six cats with presumed acromegaly versus 12 unaffected cats. Vet Radiol Ultrasound, 53: 535–539, 2012.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург